摘要:下列物质的化学式错误的是 A.重晶石:BaSO4 B.熟石膏:CaSO4·2H2O C.皓矾:ZnSO4·7H2O D.明矾:KAl(SO4)2·12H2O
网址:http://m.1010jiajiao.com/timu3_id_50497[举报]
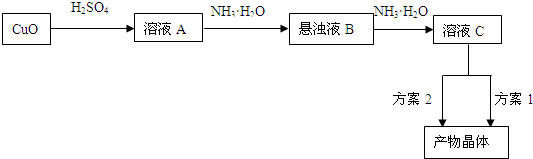
一水硫酸四氨合铜(Ⅱ)的化学式为[ Cu( NH3)4]SO4·H2O,是一种重要的染料及农药中间体。某学习小组在实验室以氧化铜为主要原料合成该物质,设计的合成路线为:

相关信息如下: ①[Cu( NH3)4]SO4·H2O在溶液中存在以下电离(解离)过程:
[ Cu(NH3)4]SO4·H2O=[ Cu( NH3)4]2++SO42-+H2O
[Cu(NH3)4]2+ Cu2++4NH3②(NH4)·SO4在水中可溶,在乙醇中难溶。
Cu2++4NH3②(NH4)·SO4在水中可溶,在乙醇中难溶。
③[ Cu( NH3)4]SO4·H2O在乙醇一水混合溶剂中的溶解度随乙醇体积分数的变化曲线示意图如下
[ Cu(NH3)4]SO4·H2O=[ Cu( NH3)4]2++SO42-+H2O
[Cu(NH3)4]2+
 Cu2++4NH3②(NH4)·SO4在水中可溶,在乙醇中难溶。
Cu2++4NH3②(NH4)·SO4在水中可溶,在乙醇中难溶。③[ Cu( NH3)4]SO4·H2O在乙醇一水混合溶剂中的溶解度随乙醇体积分数的变化曲线示意图如下

请根据相关信息回答下列问题:
方案l的实验步骤为: a.加热蒸发,b.冷却结晶,c.抽滤,d.洗涤,e.干燥
(1)①步骤c的抽滤装置如下图所示,该装置中的错误之处是____;抽滤完毕或中途需停止抽滤时,应先______,然后________。
②该方案存在明显缺陷,因为得到的产物晶体中往往含有____杂质,产生该杂质可能的原因是______ 。
方案l的实验步骤为: a.加热蒸发,b.冷却结晶,c.抽滤,d.洗涤,e.干燥
(1)①步骤c的抽滤装置如下图所示,该装置中的错误之处是____;抽滤完毕或中途需停止抽滤时,应先______,然后________。
②该方案存在明显缺陷,因为得到的产物晶体中往往含有____杂质,产生该杂质可能的原因是______ 。
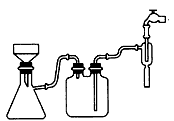
方案2的实验步骤为:
(2)a向溶液C中加入适量______,b_______,c.洗涤,d.干燥。
①请在上述空格内填写合适的试剂或操作名称。
(3) ②下列选项中,最适合作为步骤c的洗涤液是____。
A.乙醇 B.蒸馏水 C.乙醇和水的混合液 D.饱和硫酸钠溶液
③步骤d不宜采用加热干燥的方法,可能的原因是__________。
查看习题详情和答案>>
(2)a向溶液C中加入适量______,b_______,c.洗涤,d.干燥。
①请在上述空格内填写合适的试剂或操作名称。
(3) ②下列选项中,最适合作为步骤c的洗涤液是____。
A.乙醇 B.蒸馏水 C.乙醇和水的混合液 D.饱和硫酸钠溶液
③步骤d不宜采用加热干燥的方法,可能的原因是__________。
一水硫酸四氨合铜(Ⅱ)的化学式为[Cu(NH3)4]SO4?H2O是一种重要的染料及农药中间体.某学习小组在实验室以氧化铜为主要原料合成该物质,设计的合成路线为:
相关信息如下以下电离(解离)过程:
[Cu(NH3)4]SO4?H2O=[Cu(NH3)4]2++SO42-+H2O
[Cu(NH3)4]2+
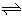
Cu2++4NH3
②(NH4)2SO4在水中可溶,在乙醇中难溶.
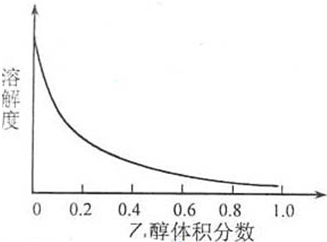
③[Cu(NH3)4]SO4?H2O在乙醇?水混合溶剂中的溶解度随乙醇体积分数的变化曲线示意图如下:
请根据以下信息回答下列问题:
(1)方案1的实验步骤为:
a.加热蒸发 b.冷却结晶 c.抽滤 d.洗涤 e.干燥
①步骤1的抽滤装置如下图所示,该装置中的错误之处是______;抽滤完毕或中途停止抽滤时,应先______,然后______.
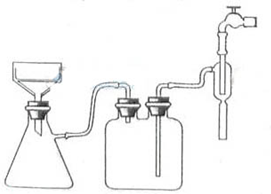
②该方案存在明显缺陷,因为得到的产物晶体中往往含有______杂质,产生该杂质的原因是______.
(2)方案2的实验步骤为:
a.向溶液C加入适量______b.______c.洗涤,d.干燥
①请在上述内填写合适的试剂或操作名称.
②下列选项中,最适合作为步骤c的洗涤液是______.
A.乙醇 B.蒸馏水 C.乙醇和水的混合液 D.饱和硫酸钠溶液
③步骤d不宜采用加热干燥的方法,可能的原因是______.
查看习题详情和答案>>

相关信息如下以下电离(解离)过程:
[Cu(NH3)4]SO4?H2O=[Cu(NH3)4]2++SO42-+H2O
[Cu(NH3)4]2+
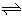
Cu2++4NH3
②(NH4)2SO4在水中可溶,在乙醇中难溶.
③[Cu(NH3)4]SO4?H2O在乙醇?水混合溶剂中的溶解度随乙醇体积分数的变化曲线示意图如下:

请根据以下信息回答下列问题:
(1)方案1的实验步骤为:
a.加热蒸发 b.冷却结晶 c.抽滤 d.洗涤 e.干燥
①步骤1的抽滤装置如下图所示,该装置中的错误之处是______;抽滤完毕或中途停止抽滤时,应先______,然后______.

②该方案存在明显缺陷,因为得到的产物晶体中往往含有______杂质,产生该杂质的原因是______.
(2)方案2的实验步骤为:
a.向溶液C加入适量______b.______c.洗涤,d.干燥
①请在上述内填写合适的试剂或操作名称.
②下列选项中,最适合作为步骤c的洗涤液是______.
A.乙醇 B.蒸馏水 C.乙醇和水的混合液 D.饱和硫酸钠溶液
③步骤d不宜采用加热干燥的方法,可能的原因是______.
一水硫酸四氨合铜(Ⅱ)的化学式为[Cu(NH3)4]SO4?H2O是一种重要的染料及农药中间体.某学习小组在实验室以氧化铜为主要原料合成该物质,设计的合成路线为:
相关信息如下以下电离(解离)过程:
[Cu(NH3)4]SO4?H2O=[Cu(NH3)4]2++SO42-+H2O
[Cu(NH3)4]2+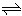 Cu2++4NH3
Cu2++4NH3
②(NH4)2SO4在水中可溶,在乙醇中难溶.
③[Cu(NH3)4]SO4?H2O在乙醇?水混合溶剂中的溶解度随乙醇体积分数的变化曲线示意图如下:
请根据以下信息回答下列问题:
(1)方案1的实验步骤为:
a.加热蒸发 b.冷却结晶 c.抽滤 d.洗涤 e.干燥
①步骤1的抽滤装置如下图所示,该装置中的错误之处是______;抽滤完毕或中途停止抽滤时,应先______,然后______.

②该方案存在明显缺陷,因为得到的产物晶体中往往含有______杂质,产生该杂质的原因是______.
(2)方案2的实验步骤为:
a.向溶液C加入适量______b.______c.洗涤,d.干燥
①请在上述内填写合适的试剂或操作名称.
②下列选项中,最适合作为步骤c的洗涤液是______.
A.乙醇 B.蒸馏水 C.乙醇和水的混合液 D.饱和硫酸钠溶液
③步骤d不宜采用加热干燥的方法,可能的原因是______.
查看习题详情和答案>>

相关信息如下以下电离(解离)过程:
[Cu(NH3)4]SO4?H2O=[Cu(NH3)4]2++SO42-+H2O
[Cu(NH3)4]2+
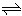 Cu2++4NH3
Cu2++4NH3②(NH4)2SO4在水中可溶,在乙醇中难溶.
③[Cu(NH3)4]SO4?H2O在乙醇?水混合溶剂中的溶解度随乙醇体积分数的变化曲线示意图如下:

请根据以下信息回答下列问题:
(1)方案1的实验步骤为:
a.加热蒸发 b.冷却结晶 c.抽滤 d.洗涤 e.干燥
①步骤1的抽滤装置如下图所示,该装置中的错误之处是______;抽滤完毕或中途停止抽滤时,应先______,然后______.

②该方案存在明显缺陷,因为得到的产物晶体中往往含有______杂质,产生该杂质的原因是______.
(2)方案2的实验步骤为:
a.向溶液C加入适量______b.______c.洗涤,d.干燥
①请在上述内填写合适的试剂或操作名称.
②下列选项中,最适合作为步骤c的洗涤液是______.
A.乙醇 B.蒸馏水 C.乙醇和水的混合液 D.饱和硫酸钠溶液
③步骤d不宜采用加热干燥的方法,可能的原因是______.
查看习题详情和答案>>
二氧化硫和氮氧化物(NOx)对大气污染日趋严重,研究消除大气污染的方法是化学工作者的重要课题,目前有很多种方法消除大气污染.

(1)可利用甲烷催化还原NOx的方法处理NOx,反应如下:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g);△H=-574kJ?mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);△H=-1160kJ?mol-1
则CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g);△H=
(2)汽车尾气中的主要污染物有CO、NOx、碳氢化合物等,降低汽车尾气的方法之一是在排气管上安装催化转化器,发生如下反应:
2NO(g)+2CO(g)?N2(g)+2CO2(g);△H<0.
生成无毒物质,减少汽车尾气污染.若在一定温度下,将2molNO、1molCO充入1L固定容积的容器中,15分钟后达到平衡,反应过程中各物质的浓度变化如图1所示,则
①前15s内的平均反应速率v (N2)=
②该反应平衡常数K=
③若保持温度不变,20min时再向容器中充入CO、N2各0.6mol,平衡将
a 加入催化剂 b 降低温度 c 缩小容器体积 d 增加CO2的量
④该可逆反应△S
(3)CO分析仪以燃料电池为工作原理,其装置如图2所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动.下列说法错误的是
A.负极的电极反应式为:CO+O2--2e-=CO2
B.工作时电极b作正极,O2-由电极a流向电极b
C.工作时电子由电极a通过传感器流向电极b
D.传感器中通过的电流越大,尾气中CO的含量越高
(4)利用Fe2+、Fe3+的催化作用,常温下将SO2转化为SO42- 而实现对SO2的处理目的.其中Fe3+的最外层电子排布式为
(5)N2O5是重要的硝化剂和氧化剂,可用电解法制备N2O5,如图3所示,N2O5在电解池的
查看习题详情和答案>>

(1)可利用甲烷催化还原NOx的方法处理NOx,反应如下:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g);△H=-574kJ?mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);△H=-1160kJ?mol-1
则CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g);△H=
-867 kJ/mol
-867 kJ/mol
;(2)汽车尾气中的主要污染物有CO、NOx、碳氢化合物等,降低汽车尾气的方法之一是在排气管上安装催化转化器,发生如下反应:
2NO(g)+2CO(g)?N2(g)+2CO2(g);△H<0.
生成无毒物质,减少汽车尾气污染.若在一定温度下,将2molNO、1molCO充入1L固定容积的容器中,15分钟后达到平衡,反应过程中各物质的浓度变化如图1所示,则
①前15s内的平均反应速率v (N2)=
0.013 mol/(L?s)
0.013 mol/(L?s)
(小数点保留3位);②该反应平衡常数K=
0.035
0.035
(小数点保留3位);③若保持温度不变,20min时再向容器中充入CO、N2各0.6mol,平衡将
不移动
不移动
移动(填“向左”、“向右”或“不”);20min时,若改变反应条件,导致N2浓度发生如图1所示的变化,则改变的条件可能是b
b
(填序号);a 加入催化剂 b 降低温度 c 缩小容器体积 d 增加CO2的量
④该可逆反应△S
<
<
0(填“>”、“<”或“=”),在低温
低温
(填“高温”、“低温”或“任何温度”)下能自发进行.(3)CO分析仪以燃料电池为工作原理,其装置如图2所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动.下列说法错误的是
B
B
A.负极的电极反应式为:CO+O2--2e-=CO2
B.工作时电极b作正极,O2-由电极a流向电极b
C.工作时电子由电极a通过传感器流向电极b
D.传感器中通过的电流越大,尾气中CO的含量越高
(4)利用Fe2+、Fe3+的催化作用,常温下将SO2转化为SO42- 而实现对SO2的处理目的.其中Fe3+的最外层电子排布式为
3s23p63d5
3s23p63d5
;SO2的VSEPR模型名称为平面三角形
平面三角形
;与SO2互为等电子体的离子有NO2-
NO2-
.(5)N2O5是重要的硝化剂和氧化剂,可用电解法制备N2O5,如图3所示,N2O5在电解池的
阳极
阳极
(填“阳极”或“阴极”)区生成,其电极反应式为N2O4-2e-+2HNO3=2N2O5+2H+
N2O4-2e-+2HNO3=2N2O5+2H+
.
二氧化硫和氮氧化物(NOx)对大气污染日趋严重,研究消除大气污染的方法是化学工作者的重要课题,目前有很多种方法消除大气污染.

(1)可利用甲烷催化还原NOx的方法处理NOx,反应如下:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g);△H=-574kJ?mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);△H=-1160kJ?mol-1
则CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g);△H=______;
(2)汽车尾气中的主要污染物有CO、NOx、碳氢化合物等,降低汽车尾气的方法之一是在排气管上安装催化转化器,发生如下反应:
2NO(g)+2CO(g)?N2(g)+2CO2(g);△H<0.
生成无毒物质,减少汽车尾气污染.若在一定温度下,将2molNO、1molCO充入1L固定容积的容器中,15分钟后达到平衡,反应过程中各物质的浓度变化如图1所示,则
①前15s内的平均反应速率v (N2)=______(小数点保留3位);
②该反应平衡常数K=______(小数点保留3位);
③若保持温度不变,20min时再向容器中充入CO、N2各0.6mol,平衡将______移动(填“向左”、“向右”或“不”);20min时,若改变反应条件,导致N2浓度发生如图1所示的变化,则改变的条件可能是______(填序号);
a 加入催化剂 b 降低温度 c 缩小容器体积 d 增加CO2的量
④该可逆反应△S______0(填“>”、“<”或“=”),在______(填“高温”、“低温”或“任何温度”)下能自发进行.
(3)CO分析仪以燃料电池为工作原理,其装置如图2所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动.下列说法错误的是______
A.负极的电极反应式为:CO+O2--2e-=CO2
B.工作时电极b作正极,O2-由电极a流向电极b
C.工作时电子由电极a通过传感器流向电极b
D.传感器中通过的电流越大,尾气中CO的含量越高
(4)利用Fe2+、Fe3+的催化作用,常温下将SO2转化为SO42- 而实现对SO2的处理目的.其中Fe3+的最外层电子排布式为______;SO2的VSEPR模型名称为______;与SO2互为等电子体的离子有______.
(5)N2O5是重要的硝化剂和氧化剂,可用电解法制备N2O5,如图3所示,N2O5在电解池的______(填“阳极”或“阴极”)区生成,其电极反应式为______.
查看习题详情和答案>>

(1)可利用甲烷催化还原NOx的方法处理NOx,反应如下:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g);△H=-574kJ?mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);△H=-1160kJ?mol-1
则CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g);△H=______;
(2)汽车尾气中的主要污染物有CO、NOx、碳氢化合物等,降低汽车尾气的方法之一是在排气管上安装催化转化器,发生如下反应:
2NO(g)+2CO(g)?N2(g)+2CO2(g);△H<0.
生成无毒物质,减少汽车尾气污染.若在一定温度下,将2molNO、1molCO充入1L固定容积的容器中,15分钟后达到平衡,反应过程中各物质的浓度变化如图1所示,则
①前15s内的平均反应速率v (N2)=______(小数点保留3位);
②该反应平衡常数K=______(小数点保留3位);
③若保持温度不变,20min时再向容器中充入CO、N2各0.6mol,平衡将______移动(填“向左”、“向右”或“不”);20min时,若改变反应条件,导致N2浓度发生如图1所示的变化,则改变的条件可能是______(填序号);
a 加入催化剂 b 降低温度 c 缩小容器体积 d 增加CO2的量
④该可逆反应△S______0(填“>”、“<”或“=”),在______(填“高温”、“低温”或“任何温度”)下能自发进行.
(3)CO分析仪以燃料电池为工作原理,其装置如图2所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动.下列说法错误的是______
A.负极的电极反应式为:CO+O2--2e-=CO2
B.工作时电极b作正极,O2-由电极a流向电极b
C.工作时电子由电极a通过传感器流向电极b
D.传感器中通过的电流越大,尾气中CO的含量越高
(4)利用Fe2+、Fe3+的催化作用,常温下将SO2转化为SO42- 而实现对SO2的处理目的.其中Fe3+的最外层电子排布式为______;SO2的VSEPR模型名称为______;与SO2互为等电子体的离子有______.
(5)N2O5是重要的硝化剂和氧化剂,可用电解法制备N2O5,如图3所示,N2O5在电解池的______(填“阳极”或“阴极”)区生成,其电极反应式为______.
查看习题详情和答案>>