摘要:10.某温度下.10gNaNO3溶解在40g水中.形成饱和溶液.则该温度下.NaNO3的溶解度为 A. 10g B. 20g C. 25g D. 40g 本资料由 提供!
网址:http://m.1010jiajiao.com/timu3_id_50195[举报]
在某温度下,将H2(g)和I2(g)各0.1mol的气体混合物充入10L的密闭容器中,充分反应,达到平衡时,测得c(H2)=0.0080mol/L,求:
(1)求该反应的平衡常数.
(2)在上述温度下,该容器中若充入的H2(g)和I2(g)各0.2mol,求达到化学平衡时HI(g)的平衡浓度.
查看习题详情和答案>>
(1)求该反应的平衡常数.
(2)在上述温度下,该容器中若充入的H2(g)和I2(g)各0.2mol,求达到化学平衡时HI(g)的平衡浓度.
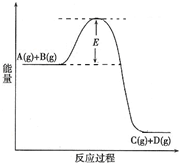 (2010?陕西模拟)已知A(g)+B(g)?C(g)+D(g) 反应过程中的能量变化如图所示,回答下列问题.
(2010?陕西模拟)已知A(g)+B(g)?C(g)+D(g) 反应过程中的能量变化如图所示,回答下列问题.(1)该反应是
放热
放热
反应(填“吸热”、“放热”).当反应达到平衡时,升高温度,A的转化率减小
减小
(填“增大”、“减小”或“不变”),(2)在反应体系中加入催化剂,反应速率增大,E的变化是
减小
减小
,(填“增大”、“减小”或“不变”)理由是催化剂改变了反应的历程使活化能E降低
催化剂改变了反应的历程使活化能E降低
; E的大小对该反应的反应热有无影响?无影响
无影响
.(3)一定条件下,向体积为2L的恒容密闭容器中充入1mol A(g) 和3mol B(g),判断该反应达到平衡状态的依据是(填序号)
④
④
.①c (A)=c (C) ②容器中压强不变
③混合气体的平均相对分子质量不变 ④v(逆)(D)=v (正)(B)
(4)在某温度下,反应物的起始浓度分别为:c(A)=1mol?L-1,c(B)=2.4mol?L-1,达到平衡后,A的转化率为60%,此时B 的转化率为
25%
25%
.(5)若反应温度不变,反应物的起始浓度分别为:c(A)=4mol?L-1,c(B)=amol?L-1,达到平衡后,c(C)=2mol?L-1,列出计算式并求出a值.
(2013?崇明县一模)甲醇是重要的化学工业基础原料和清洁液体燃料,它广泛用于有机合成、医药、农药、涂料、染料、汽车和国防等工业中.工业上一般在恒容密闭容器中采用下列反应合成甲醇:CO(g)+2H2(g)
CH3OH(g)+Q
下表所列数据是反应在不同温度下的化学平衡常数(K).
(1)判断反应达到平衡状态的依据是
A.混合气体的密度不变
B.混合气体的平均相对分子质量不变
C.生成CH3OH的速率与消耗CO的速率相等
D.CH3OH、CO、H2的浓度都不再发生变化
(2)由表中数据判断Q
A.加入催化剂B.充入COC.充入H2D.升温
(3)某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应10min后,达到平衡时测得c(CO)=0.2mol/L,则以CH3OH表示的反应速率v(CH3OH)=
CO的转化率为
(4)原料CO和H2可以由C和H2O反应制取,涉及的反应方程式如下:
C(s)+CO2(g)═2CO(g)平衡常数K1
C(s)+H2O(g)═CO(g)+H2(g)平衡常数K2
CO(g)+H2O(g)═H2(g)+CO2(g)平衡常数K3
则K1、K2、K3之间的关系是:
查看习题详情和答案>>
| 催化剂 |
| 加热 |
下表所列数据是反应在不同温度下的化学平衡常数(K).
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
BD
BD
A.混合气体的密度不变
B.混合气体的平均相对分子质量不变
C.生成CH3OH的速率与消耗CO的速率相等
D.CH3OH、CO、H2的浓度都不再发生变化
(2)由表中数据判断Q
>
>
0 (填“>”、“=”或“<”),要提高CO转化率,可采取的措施是C
C
A.加入催化剂B.充入COC.充入H2D.升温
(3)某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应10min后,达到平衡时测得c(CO)=0.2mol/L,则以CH3OH表示的反应速率v(CH3OH)=
0.08
0.08
mol/(L?min),CO的转化率为
80%
80%
.(4)原料CO和H2可以由C和H2O反应制取,涉及的反应方程式如下:
C(s)+CO2(g)═2CO(g)平衡常数K1
C(s)+H2O(g)═CO(g)+H2(g)平衡常数K2
CO(g)+H2O(g)═H2(g)+CO2(g)平衡常数K3
则K1、K2、K3之间的关系是:
K2=K1?K3
K2=K1?K3
.(2011?上海模拟)超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层.科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO+2CO?2CO2+N2
为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)在上述条件下反应能够自发进行,则反应是
(2)前2s内的平均反应速度v(N2)=
(3)此反应的平衡常数表达式为K=
.
(4)假设在容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积.
查看习题详情和答案>>
为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol?L-1 | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol?L-1 | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
(1)在上述条件下反应能够自发进行,则反应是
放热
放热
反应(填写“吸热”、“放热”).(2)前2s内的平均反应速度v(N2)=
1.875×10-4mol/L?s
1.875×10-4mol/L?s
.(3)此反应的平衡常数表达式为K=
| c(N2)c2(CO2) |
| c2(CO)c2(NO) |
| c(N2)c2(CO2) |
| c2(CO)c2(NO) |
(4)假设在容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是
CD
CD
.A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积.