网址:http://m.1010jiajiao.com/timu3_id_49927[举报]
 [化学--物质结构与性质
[化学--物质结构与性质 Ⅰ.(1)原子数相同,价电子数也相同的微粒,称为等电子体.等电子体具有相似的化学键特征,性质相似.CO的结构式为
Ⅱ.(2)钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、航天航空材料,被誉为“未来世界的金属”. 钛的基态原子的电子排布式为
(3)偏钛酸钡在小型变压器、话筒和扩音器中都有●Ti应用.偏钛酸钡为离子晶体,晶胞的结构如图 所示,它的化学式是
(4)现有含Ti3+的配合物,化学式为TiCl3(H2O)6,将1mol该物质溶于水,加入足量硝酸银溶液,立即沉淀的氯化银为l mol,已知该配合物的配位数为6,则该配合物的配位体是
(11分)1866年H. Rithausen从谷胶的硫酸分解产物中分离出谷氨酸(![]() )。1890年L. Wollf合成并确定了它的结构,1908年池田菊苗从海带的热水提取物中分离出谷氨酸的钠盐(
)。1890年L. Wollf合成并确定了它的结构,1908年池田菊苗从海带的热水提取物中分离出谷氨酸的钠盐(![]() ),它才是具有鲜味的成分,即味精。
),它才是具有鲜味的成分,即味精。
10-1 谷氨酸的电离常数Ka1=6.46×10-3,Ka2=5.62×10-5,Ka3=2.14×10-10;pKa= -lgKa,所以pKa1=2.19,pKa2 = 4.25,pKa3 = 9.67。
目前工业上生产味精的方法有水解法、糖蜜提取法、淀粉发酵法及合成法等。当前我国生产的味精主要采用淀粉发酵法。
以发酵法生产的工艺流程如下:淀粉![]() 葡萄糖
葡萄糖![]() 发酵
发酵![]() 谷氨酸铵
谷氨酸铵![]() L-谷氨酸
L-谷氨酸![]() 谷氨酸-钠盐。
谷氨酸-钠盐。
若生成谷氨酸二钠盐,则不具有鲜味,所以工业生产中控制各阶段的pH是一项关键。
(1)Ka1、Ka2、Ka3相对应的基团各是哪个?
(2)计算谷氨酸等电点的pH(所谓等电点,就是谷氨酸呈电中性时所处环境的pH)。在下面正确的选项上画圈。
A.2.19 B.3.22 C.4.25 D.6.96
(3)中和、脱色、结晶时的pH应保持在多少?在下面正确的选项上画圈。
A.3.22 B.4.25 C.6.96 D.9.67
(4)用什么物质脱色?
10-2 味精中有效成分是谷氨酸钠,可用沙伦逊甲醛滴定法测定其含量。准确称取味精1.000g,加蒸馏水溶解后稀释到10.0mL;从中取2.0mL放入100mL锥形瓶中,加入2.0mL 36%的甲醛溶液,加入20mL水。以酚酞为指示剂,用0.1000mol/L的标准NaOH溶液进行滴定,消耗10.80mL。
(1)谷氨酸钠与甲醛反应得到化学式为C6H8NO4Na,写出结构简式。
(2)加入甲醛的目的是什么?
10-3 味精中往往会加入食盐,某学生设计如下实验方案测定NaCl含量:取味精样品5.0g,并溶于蒸馏水;加入足量用稀硝酸酸化的硝酸银溶液,使沉淀完全;过滤;用蒸馏水反复洗涤沉淀多次;将沉淀低温烘干、称量;重复操作3次,计算NaCl含量。
另一学生觉得这个实验方案的误差较大,且测定沉淀的质量很不方便。于是他设计了另一个实验方案来测定NaCl的含量。已知AgSCN是难溶于水的沉淀。
请简要写出测定NaCl含量的新方案。
查看习题详情和答案>>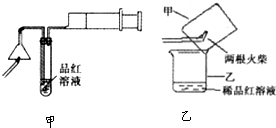
(1)检验火柴头中含有硫将两根火柴放在如图甲所示实验装置中漏斗下面,用一根燃着的火柴点燃它,慢慢拉动注射器活塞抽气,让火柴燃烧产生的气体通过稀品红溶液,观察到品红溶液褪色.
①燃烧产生的气体中一定含有
②可用于替代试管中品红溶液的试剂有
A.稀高锰酸钾酸性溶液 B.饱和石灰水
C.稀溴水 D.烧碱溶液
③某同学提出用图乙所示方法进行实验更为简便.他的操作是:
i.当图乙中所示火柴头燃烧完时,立即移出火柴;
ii.
(2)证明火柴中的氯元素是以氯酸钾的形式存在,而不是以氯化钾的形式存在,请完成下列操作:
①取3~4根火柴,摘下火柴头,浸入水中,片刻后,取少量溶液于试管中,加入少量的硝酸银溶液,没有白色沉淀生成;
②再往上述溶液中加入稀硝酸和NaNO2溶液,观察到有白色沉淀生成.反应的离子方程式是
③将燃尽的火柴头浸泡在少量水中,片刻后取少量溶液于试管中,滴加AgNO3和稀硝酸,可观察到白色沉淀产生,说明将燃尽的火柴头浸泡在少量水中,会有
(3)测定火柴头中KClO3的含量主要实验步骤如下:
(i)刮取火柴头,小心研碎,称得质量为2.45g;
(ii)用适量蒸馏水充分浸泡后过滤、洗涤残渣;
(iii)往装有滤液和洗涤液的烧杯中加入过量的NaNO2溶液、AgNO3溶液和稀硝酸,搅拌,充分反应后,过滤、洗涤沉淀;
(iv)干燥沉淀物,称得其质量为1.435g.
①反应中NaNO2、AgNO3均需要过量的原因是
②实验测得火柴头中KClO3的质量分数为
③如果第ii步中未洗涤沉淀残渣,测得KC1O3的质量分数将
已知粗铜中含有少量的锌、铁、银、金等金属和少量矿物杂质(与酸不反应)。某化学兴趣小组在实验室条件下用以硫酸铜溶液为电解液,用电解的方法实现了粗铜的提纯,并对阳极泥中金属进行回收。
步骤一:电解精制:
请回答以下问题:
(1)电解时,粗铜应与电源的 极相连。阴极上的电极反应式为
电解过程中,硫酸铜溶液的浓度会一定程度的 (选填:变大、不变、变小)
步骤二:电解完成后,该小组同学按以下流程对电解液进行处理:

(2)阳极泥的综合利用:
 稀硝酸处理阳极泥得到硝酸银稀溶液,请你写出该步反应的离子方程式:
稀硝酸处理阳极泥得到硝酸银稀溶液,请你写出该步反应的离子方程式:
残渣含有极少量的黄金,如何回收金,他们查阅了有关资料,了解到了一些有关金的知识,以下是他们获取的一些信息:
| 序号 | 反应 | 平衡常数 |
| 1 | Au + 6HNO3(浓)== Au(NO3)3 + 3NO2↑+ 3H2O | << 1 |
| 2 | Au3+ + 4Cl— == AuCl4— | K |
从中可知,金很难与硝酸反应,但实验发现金却可溶于王水(浓硝酸与盐酸按体积比1∶3的混合物),请你先猜测表格中第二个反应的平衡常数K特点并简要解释金能够溶于王水的原因:
(3)若在0.10mol·L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c (Cu2+)== mol·L-1(Ksp[Cu(OH)2]==2.2×10-20)。
(4)初中我们学到的知识:铜是一种比较稳定的金属,请你以现在的知识设计一套简单实验装置使铜与稀硫酸反应(要求:画出简图并进行适当的标注)
查看习题详情和答案>>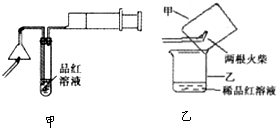
(1)检验火柴头中含有硫将两根火柴放在如图甲所示实验装置中漏斗下面,用一根燃着的火柴点燃它,慢慢拉动注射器活塞抽气,让火柴燃烧产生的气体通过稀品红溶液,观察到品红溶液褪色.
①燃烧产生的气体中一定含有______.
②可用于替代试管中品红溶液的试剂有______(填标号).
A.稀高锰酸钾酸性溶液 B.饱和石灰水
C.稀溴水D.烧碱溶液
③某同学提出用图乙所示方法进行实验更为简便.他的操作是:
i.当图乙中所示火柴头燃烧完时,立即移出火柴;
ii.______.
(2)证明火柴中的氯元素是以氯酸钾的形式存在,而不是以氯化钾的形式存在,请完成下列操作:
①取3~4根火柴,摘下火柴头,浸入水中,片刻后,取少量溶液于试管中,加入少量的硝酸银溶液,没有白色沉淀生成;
②再往上述溶液中加入稀硝酸和NaNO2溶液,观察到有白色沉淀生成.反应的离子方程式是______;
③将燃尽的火柴头浸泡在少量水中,片刻后取少量溶液于试管中,滴加AgNO3和稀硝酸,可观察到白色沉淀产生,说明将燃尽的火柴头浸泡在少量水中,会有______物质被浸出,说明火柴头燃烧时其中含有的______转化为该物质.
(3)测定火柴头中KClO3的含量主要实验步骤如下:
(i)刮取火柴头,小心研碎,称得质量为2.45g;
(ii)用适量蒸馏水充分浸泡后过滤、洗涤残渣;
(iii)往装有滤液和洗涤液的烧杯中加入过量的NaNO2溶液、AgNO3溶液和稀硝酸,搅拌,充分反应后,过滤、洗涤沉淀;
(iv)干燥沉淀物,称得其质量为1.435g.
①反应中NaNO2、AgNO3均需要过量的原因是______;
②实验测得火柴头中KClO3的质量分数为______;
③如果第ii步中未洗涤沉淀残渣,测得KC1O3的质量分数将______(填“偏大”、“偏小”、或“无影响”,下同);如果第Ⅲ步中未洗涤AgCl沉淀,测得KClO3的质量分数将______.