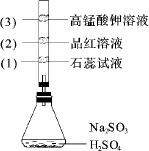
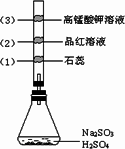
摘要:7.如图所示.锥形瓶中加入亚硫酸钠固体和1:1的硫酸.玻璃管内装入分别滴有不同溶液的棉球.反应一段时间后.对图中指定部位颜色描述正确的是
网址:http://m.1010jiajiao.com/timu3_id_49838[举报]
如图所示,锥形瓶中加入亚硫酸钠固体和1∶1的硫酸,玻璃管内装入分别滴有不同溶液的棉球,反应一段时间后,对图中指定部位颜色描述正确的是
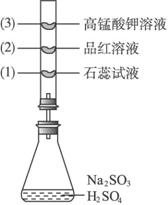
序号 | (1) | (2) | (3) |
A | 褪色 | 褪色 | 变红 |
B | 变红 | 变红 | 褪色 |
C | 变红 | 褪色 | 褪色 |
D | 褪色 | 变红 | 褪色 |
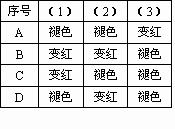
如图所示,锥形瓶中加入亚硫酸钠固体和1:1的硫酸,玻璃管内装入分别滴有不同溶液的棉球,反应一段时间后,对图中指定部位颜色描述正确的是
查看习题详情和答案>>
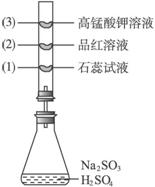
| (1) | (2) | (3) |
A | 褪色 | 褪色 | 变红 |
B | 变红 | 变红 | 褪色 |
C | 变红 | 褪色 | 褪色 |
D | 褪色 | 变红 | 褪色 |
亚硫酸钠和硫代硫酸钠(Na2S2O3)都是重要的含硫化合物.某化学兴趣小组进行以下有关实验,填写下列空白.
实验Ⅰ证明Na2SO3中硫元素的价态能发生
→
转化
(1)实验中,不需要用到的试剂有
A.稀硫酸 B.H2O2溶液 C.稀盐酸 D.淀粉碘化钾溶液 E.BaCl2溶液
观察到的现象是
实验Ⅱ制取硫代硫酸钠晶体
利用如图所示装置进行实验.已知:①硫代硫酸钠能与酸发生反应
②装置d中发生反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2

(2)装置b中发生反应的化学方程式为
(3)装置c的作用是
(4)装置d中的反应结束后,先关闭分液漏斗旋塞,接下来的操作是
实验Ⅲ测定某硫代硫酸钠样品的纯度(设:样品中只含Na2SO3杂质)设计如下方案,并进行实验:
①准确称取该硫代硫酸钠样品m g,配制成250mL待测溶液.
②移取25.00mL待测溶液于锥形瓶中,加入适量甲醛(防止Na2SO3与I2反应)和少量淀粉溶液,用n mol?L-1 I2标准溶液滴定(发生反应:2S2O32-+I2=S4O62-+2I-),至滴定终点.
(5)②中消耗I2标准溶液VmL,样品中Na2S2O3的百分含量为
(用代数式表示).
(6)该实验方案存在的一个明显缺陷是
查看习题详情和答案>>
实验Ⅰ证明Na2SO3中硫元素的价态能发生
| +4 |
| S |
| +6 |
| S |
(1)实验中,不需要用到的试剂有
AD
AD
(填标号).A.稀硫酸 B.H2O2溶液 C.稀盐酸 D.淀粉碘化钾溶液 E.BaCl2溶液
观察到的现象是
溶液中出现不溶于盐酸的白色沉淀
溶液中出现不溶于盐酸的白色沉淀
.实验Ⅱ制取硫代硫酸钠晶体
利用如图所示装置进行实验.已知:①硫代硫酸钠能与酸发生反应
②装置d中发生反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2

(2)装置b中发生反应的化学方程式为
Na2SO3+H2SO4=Na2SO4+SO2↑+H2O
Na2SO3+H2SO4=Na2SO4+SO2↑+H2O
.(3)装置c的作用是
防止倒吸
防止倒吸
.(4)装置d中的反应结束后,先关闭分液漏斗旋塞,接下来的操作是
打开K1关闭K2
打开K1关闭K2
,待d中溶液冷却后,倒入蒸发皿,蒸发浓缩,冷却、结晶…获得硫代硫酸钠晶体.实验Ⅲ测定某硫代硫酸钠样品的纯度(设:样品中只含Na2SO3杂质)设计如下方案,并进行实验:
①准确称取该硫代硫酸钠样品m g,配制成250mL待测溶液.
②移取25.00mL待测溶液于锥形瓶中,加入适量甲醛(防止Na2SO3与I2反应)和少量淀粉溶液,用n mol?L-1 I2标准溶液滴定(发生反应:2S2O32-+I2=S4O62-+2I-),至滴定终点.
(5)②中消耗I2标准溶液VmL,样品中Na2S2O3的百分含量为
| 3.16nv |
| m |
| 3.16nv |
| m |
(6)该实验方案存在的一个明显缺陷是
缺少平行实验
缺少平行实验
.