摘要:21. A.B.C.D.E都是短周期元素.原子序数依次增大.A.B处于同周期.C.D.E同处另一周期.C.A可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙.B是最活泼的非金属元素.D是地壳中含量最高的金属元素.E的最高价氧化物对应的水化物是最强的含氧酸之一. (1). B在周期表中的位置:第 周期.第 族.E的元素符号为 , (2). 物质乙可用于潜艇或航天飞机作供氧剂.写出乙与CO2反应的化学方程式: , (3). 单质D与C的最高价氧化物对应水化物溶液反应的离子方程式: , (4)1 mol 单质B的气体与1 mol C的氢氧化物在一定条件下恰好完全反应.生成一种盐.水及另一种气体.则所得气体的化学式为: .
网址:http://m.1010jiajiao.com/timu3_id_49327[举报]
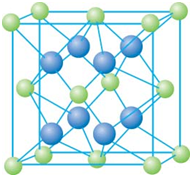 已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大.A与其他4种元素既不在同一周期又不在同一主族.B和C属同一主族,D和E属同一周期,又知E是周期表中1-18列中的第7列元素.D的原子序数比E小5,D跟B形成的晶体其晶胞结构如图,图中小球代表D,大球代表B.请回答:
已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大.A与其他4种元素既不在同一周期又不在同一主族.B和C属同一主族,D和E属同一周期,又知E是周期表中1-18列中的第7列元素.D的原子序数比E小5,D跟B形成的晶体其晶胞结构如图,图中小球代表D,大球代表B.请回答:(1)A元素的名称是
氢
氢
;(2)B元素的轨道表示式是
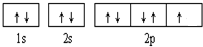

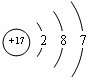

氟化氢分子间存在氢键,氯化氢分子间没有氢键
氟化氢分子间存在氢键,氯化氢分子间没有氢键
;(3)E属于元素周期表中第
四
四
周期,第VIIB
VIIB
族的元素,其元素名称是锰
锰
;属于元素周期表中的d
d
区(填元素分区),它的+2价离子的电子排布式为1s22s22p63s23p63d5
1s22s22p63s23p63d5
;(4)从图中可以看出,D跟B形成的离子化合物的化学式为
CaF2
CaF2
;该离子化合物晶体的密度为a g?cm-3,则晶胞的体积是| 4×78g/mol |
| ag/cm3×6.02×1023/mol |
| 4×78g/mol |
| ag/cm3×6.02×1023/mol |
(2011?西安模拟)[化学一选修物质结构与性质]
A、B、C、D、E都是短周期主族元素,原子序数依次增大,B、C同周期,A、D同主族,E的单质既可溶于稀硫酸又可溶于氢氧化钠溶液.a、b能形成两种在常温下呈液态的化合物甲和乙,原子个数比分别为2:1和1:1.根据以上信息回答下列1-3问:
(1)C和D的离子中,半径较小的是
(2)实验室在测定C的气态氢化物的相对分子质量时,发现实际测定值比理论值大出许多,其原因是
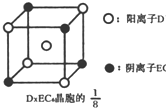
(3)C、D、E可组成离子化合物DxE6其晶胞(晶胞是在晶体中具有代表性的最小重复单元)结构如图所示,阳离子D+(用0表示)位于正方体的棱的中点和正方体内部;阴离子EC6x-(用 示)位于该正方体的顶点和面心,该化合物的化学式是
示)位于该正方体的顶点和面心,该化合物的化学式是
(4)Mn、Fe均为第四周期过渡元素,两元素的部分电离能数据列于下表:
回答下列问题:
Mn元素价电子层的电子排布式为
(5)Fe原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物.
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是
②六氰合亚铁离子(Fe(CN)64-)中的配体CN-中c原子的杂化轨遣类型是
写出一种与CN-互为等电子体的单质分子的路易斯结构式
查看习题详情和答案>>
A、B、C、D、E都是短周期主族元素,原子序数依次增大,B、C同周期,A、D同主族,E的单质既可溶于稀硫酸又可溶于氢氧化钠溶液.a、b能形成两种在常温下呈液态的化合物甲和乙,原子个数比分别为2:1和1:1.根据以上信息回答下列1-3问:
(1)C和D的离子中,半径较小的是
Na+
Na+
(填离子符号).(2)实验室在测定C的气态氢化物的相对分子质量时,发现实际测定值比理论值大出许多,其原因是
由于HF中含有氢键相结合的聚合氟化氢分子(HF)n
由于HF中含有氢键相结合的聚合氟化氢分子(HF)n
.(3)C、D、E可组成离子化合物DxE6其晶胞(晶胞是在晶体中具有代表性的最小重复单元)结构如图所示,阳离子D+(用0表示)位于正方体的棱的中点和正方体内部;阴离子EC6x-(用
 示)位于该正方体的顶点和面心,该化合物的化学式是
示)位于该正方体的顶点和面心,该化合物的化学式是Na3AlF6
Na3AlF6
.
(4)Mn、Fe均为第四周期过渡元素,两元素的部分电离能数据列于下表:
| 元素 | Mn | Fe | |
| 电离 能/kJ?mol-1 |
Ⅰ1 | 717 | 759 |
| Ⅱ2 | 1509 | 1561 | |
| Ⅲ3 | 3248 | 2957 |
Mn元素价电子层的电子排布式为
3d54s2
3d54s2
,比较两元素的I2J3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难.对此的解释是由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转为不稳定的3d4状态需要的能量较多;而Fe2+到Fe3+时,3d能级由不稳定的3d6到稳定的3d5半充满状态,需要的能量相对要少
由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转为不稳定的3d4状态需要的能量较多;而Fe2+到Fe3+时,3d能级由不稳定的3d6到稳定的3d5半充满状态,需要的能量相对要少
;(5)Fe原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物.
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是
具有弧对电子
具有弧对电子
.②六氰合亚铁离子(Fe(CN)64-)中的配体CN-中c原子的杂化轨遣类型是
sp
sp
;写出一种与CN-互为等电子体的单质分子的路易斯结构式
N≡N
N≡N
.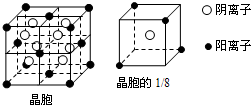 【选修-物质结构与性质】A、B、C、D、E都是元素周期表中前20号元素,其原子序数依次增大.B、C、D同周期,A、D同主族,E和其它元素既不在同周期也不在同主族.B、C、D的最高价氧化物的水化物均能互相反应生成盐和水.A和E可形成离子化合物,其晶胞结构如下图所示:
【选修-物质结构与性质】A、B、C、D、E都是元素周期表中前20号元素,其原子序数依次增大.B、C、D同周期,A、D同主族,E和其它元素既不在同周期也不在同主族.B、C、D的最高价氧化物的水化物均能互相反应生成盐和水.A和E可形成离子化合物,其晶胞结构如下图所示:(1)A和E所形成的化合物的电子式是
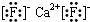
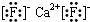
(2)A、B、C、D四种元素的原子半径由小到大的顺序为
F<Cl<Al<Na
F<Cl<Al<Na
(用元素符号表示)(3)A和D的氢化物中,后者沸点较低,原因是
由于HF分子间存在氢键
由于HF分子间存在氢键
(4)A和E的化合物晶体中,每个阳离子的周围与它最近且等距离的阳离子共有
12
12
个(5)已知A和E所形成的化合物晶体的晶胞体积为1.6×10-22cm3,则A和E组成的离子化合物的密度为(结果保留一位小数)
3.2g/cm3
3.2g/cm3
.Ⅰ.上表中的实线是元素周期表部分边界,请在表中用实线补全元素周期表边界,并画出金属和非金属的分界线,用阴影画出铁元素所在的族.
Ⅱ.A、B、C、D、E都是短周期元素,原子序数依次增大,A、B处于同一周期,C、D、E同处另一周期.C、B可按原子个数比2:l和1:1分别形成两种离子化合物甲和乙.A原子的最外层电子数比次外层电子层多3个.E是地壳中含量最高的金属元素.根据以上信息回答下列问题:

(1)D元素在周期表中的位置是
 ,乙物质的电子式是
,乙物质的电子式是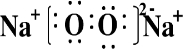
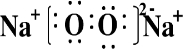
(2)A、B、C、D、E五种元素的原子半径由小到大的顺序是(用元素符号填写)
(3)E的单质加入到C的最高价氧化物对应的水化物的溶液中,发生反应的离子方程式是
(4)简述比较D与E金属性强弱的实验方法:
(5)E的单质、石墨和二氧化钛(TiO2)按比例混合,高温下反应得到的两种化合物均由两种元素组成,且都是新型陶瓷材料(在火箭和导弹上有重要应用)其反应方程式为
查看习题详情和答案>>
Ⅱ.A、B、C、D、E都是短周期元素,原子序数依次增大,A、B处于同一周期,C、D、E同处另一周期.C、B可按原子个数比2:l和1:1分别形成两种离子化合物甲和乙.A原子的最外层电子数比次外层电子层多3个.E是地壳中含量最高的金属元素.根据以上信息回答下列问题:

(1)D元素在周期表中的位置是
第三周期IIA族
第三周期IIA族
,画出B元素简单离子结构示意图

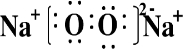
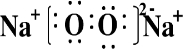
(2)A、B、C、D、E五种元素的原子半径由小到大的顺序是(用元素符号填写)
O<N<Al<Mg<Na
O<N<Al<Mg<Na
(3)E的单质加入到C的最高价氧化物对应的水化物的溶液中,发生反应的离子方程式是
2Al+2OH-+2H2O=2AlO2-+3H2↑
2Al+2OH-+2H2O=2AlO2-+3H2↑
(4)简述比较D与E金属性强弱的实验方法:
镁与热水可以反应生成氢氧化镁和氢气,但铝和热水不反应
镁与热水可以反应生成氢氧化镁和氢气,但铝和热水不反应
(5)E的单质、石墨和二氧化钛(TiO2)按比例混合,高温下反应得到的两种化合物均由两种元素组成,且都是新型陶瓷材料(在火箭和导弹上有重要应用)其反应方程式为
4Al+3C+3TiO2
2Al2O3+3TiC
| ||
4Al+3C+3TiO2
2Al2O3+3TiC
.
| ||