摘要: E是CH3OH.CH3OH形成分子间氢键 (2)V形. (3)N2O4 + 2N2H4 = 3N2 + 4H2O (4)CO中第一个π键的键能比N2的小很多.CO的第一个键容易断. (6)3d84s2.CO. 28(A)下表为长式周期表的一部分.其中的编号代表对应的元素. ① ② ③ ④ ⑤ ⑥ ⑦ ⑧ ⑨ ⑩ 请回答下列问题: (1)表中属于d区的元素是 . (2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为 ,③和⑦形成的常见化合物的晶体类型是 . (3)某元素的特征电子排布式为nsnnpn+1.该元素原子的核外最外层电子的孤对电子数为 ,该元素与元素①形成的分子X的空间构形为 (4)某些不同族元素的性质也有一定的相似性.如上表中元素⑤与元素②的氢氧化物有相似的性质.请写出元素②的氢氧化物与NaOH溶液反应的化学方程式: . (5) 1183 K以下⑨元素形成的晶体的基本结构单元如图1所示.1183 K以上转变为图2所示结构的基本结构单元.在两种晶体中最邻近的原子间距离相同. 在1183 K以下的晶体中.与⑨原子等距离且最近的⑨原子数为 个.在1183 K以上的晶体中.与⑨原子等距离且最近的⑨原子数为 . 转变温度前后两者的密度比(1183 K以下与1183 K以上之比) . 28 苯 三角锥形 2+2NaOH=Na2BeO2+2H2O 12
网址:http://m.1010jiajiao.com/timu3_id_49310[举报]
(8分) ABCDE五种物质中含有同一种元素,其相互转化关系如图所示。C是空气污染物。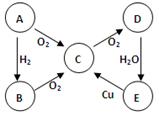
(1)如果A是淡黄色固体单质:(以下均写化学式)则C是 E是 。
写出:E→C的化学方程式
(2)如果A是无色气体: E→C的化学方程式为
(8分) ABCDE五种物质中含有同一种元素,其相互转化关系如图所示。C是空气污染物。

(1)如果A是淡黄色固体单质:(以下均写化学式)则C是 E是 。
写出:E→C的化学方程式
(2)如果A是无色气体: E→C的化学方程式为
查看习题详情和答案>>
根据下图中所表示的变化关系,写出各物质的化学式。
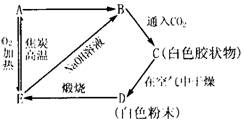
A是______________ B是______________
C是______________ D是______________
E是______________
查看习题详情和答案>> 海水中可提取多种化工原料,下面是工业上对海水的几项综合利用示意图.
海水中可提取多种化工原料,下面是工业上对海水的几项综合利用示意图.按要求回答问题:
(1)浩瀚的海洋是一个巨大的宝库,蕴含有80多种元素,可供提取利用的有50多种.下列物质不需要通过化学变化就能够从海水中获得的是
AC
AC
.A.食盐 B.金属钠 C.淡水
(2)以电解食盐水为基础制取Cl2、
H2、NaOH
H2、NaOH
等产品的工业称为“氯碱工业”.(3)实验室制取氯气的反应原理为:MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O;根据上述实验原理,从下列装置中选择合适的发生装置用于实验室制取少量氯气
b
b
(填写装置的序号). 
(4)实验室中模拟Br-→Br2的转化,可以通过在KBr溶液中滴加少量新制氯水的实验进行实现.写出Br-→Br2的转化离子方程式为:
2Br-+Cl2=2Cl-+Br2
2Br-+Cl2=2Cl-+Br2
;氯水不稳定,要现用现配,下列吸收氯气制备氯水的装置最合理的是d
d
(选填下列选项的编号字母).
(5)电解熔融氯化镁所得的镁蒸气冷却后即为固体镁.下列气体中,镁蒸气可以在其氛围中冷却的是
Ar、H2
Ar、H2
(选填下列选项的编号字母).A.Cl2 B.N2 C.Ar D.空气 E.H2.
硫元素可以形成多种物质如SCl
、SO2、SO
、SO
等.
(1)SCl
中S原子的轨道杂化类型是
的空间构型是
(2)向[Cu(NH3)4]SO4溶液中通入SO2至微酸性,有白色沉淀生成.分析表明该沉淀中Cu、S、N的物质的量之比为1:1:1,经测定该沉淀的晶体里有一种三角锥型的阴离子和一种正四面体型的阳离子.
①[Cu(NH3)4]SO4中Cu2+的电子排布式为
②[Cu(NH33)4]SO4中存在的化学键类型有
A.共价键 B.氢键 C.离子键 D.配位键 E.分子间作用力
③写出与SO
互为等电子体的一种分子:
④上述白色沉淀的化学式为
查看习题详情和答案>>
+ 3 |
2- 3 |
2- 4 |
(1)SCl
+ 3 |
sp3
sp3
,SCl+ 3 |
三角锥型
三角锥型
.(2)向[Cu(NH3)4]SO4溶液中通入SO2至微酸性,有白色沉淀生成.分析表明该沉淀中Cu、S、N的物质的量之比为1:1:1,经测定该沉淀的晶体里有一种三角锥型的阴离子和一种正四面体型的阳离子.
①[Cu(NH3)4]SO4中Cu2+的电子排布式为
[Ar]3d9
[Ar]3d9
.②[Cu(NH33)4]SO4中存在的化学键类型有
ACD
ACD
(填字母).A.共价键 B.氢键 C.离子键 D.配位键 E.分子间作用力
③写出与SO
2- 4 |
SiCl4或SiF4
SiCl4或SiF4
.④上述白色沉淀的化学式为
(NH4)CuSO3
(NH4)CuSO3
.