网址:http://m.1010jiajiao.com/timu3_id_48756[举报]
某实验小组为探究ClO-、I2、SO![]() 在酸性条件下的氧化性强弱,设计实验如下:
在酸性条件下的氧化性强弱,设计实验如下:
实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;
实验②:向实验①的溶液中加入4 mL 0.5 mol/L的亚硫酸钠溶液,蓝色恰好完全褪去.
(1)写出实验①中发生反应的离子方程式________.
(2)实验②中化学反应转移电子的物质的量是________.
(3)以上实验说明,在酸性条件下ClO-、I2、SO![]() 的氧化性由弱到强的顺序是________.
的氧化性由弱到强的顺序是________.
某实验小组为探究ClO-、I2、SO42-在酸性条件下的氧化性强弱,设计实验如下:
实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;
实验②:向实验①的溶液中加入4 mL 0.5 mol/L的亚硫酸钠溶液,蓝色恰好完全褪去.
(1)写出实验①中发生反应的离子方程式________.
(2)实验②中化学反应转移电子的物质的量是________.
(3)以上实验说明,在酸性条件下ClO-、I2、SO42-的氧化性由弱到强的顺序是________.
某实验小组为探究ClO-、I2、SO42-在酸性条件下的氧化性强弱,设计实验如下:
实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;
实验②:向实验①的溶液中加入4 mL 0.5 mol/L的亚硫酸钠溶液,蓝色恰好完全褪去.
(1)写出实验①中发生反应的离子方程式________.
(2)实验②中化学反应转移电子的物质的量是________.
(3)以上实验说明,在酸性条件下ClO-、I2、SO42-的氧化性由弱到强的顺序是________.
(1)铜在一定条件下也能被腐蚀.下列装置中,铜腐蚀的速度最慢的是(填装置序号)
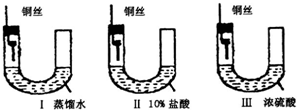
(2)金属铜长期暴露在潮湿空气中往往被腐蚀.生成的“铜锈”受热易分解为氧化铜、二氧化碳和水.为验证“铜锈”分解的部分产物,某同学设计了下图装置:
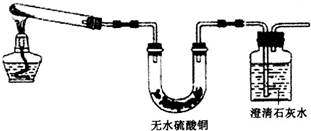
该装置可初步验证“铜锈”分解产物中的
(3)为了从“铜锈”中制得铜并测定“铜锈”的组成,设计实验装置如下:
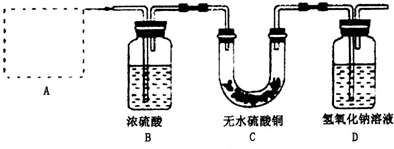
请回答下列问题:
①A处是“铜锈”与氢气反应的装置,应选用下图中的
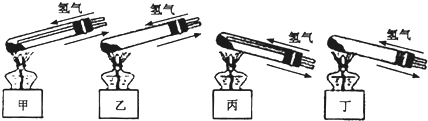
②反应进行时,应先
③要准确测定“铜锈”的组成,实验时C中现象应为
④上述装置还有不完善之处,应将D装置中排出的气体
I、(10分)过氧化氢H2O2,(氧的化合价为-1价),俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。对于下列A~F涉及H2O2的反应,回答相关问题:
A.2 H2O2=2 H2O+O2↑ B.Na2O2 +2HCl= 2NaCl+H2O2
C.Ag2O+ H2O2=2Ag+O2↑+ H2O
D.3 H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8 H2O
E.H2O2+MnSO4 = MnO2 + H2SO4 F.H2O2 +2Fe2++2H+== 2Fe3++2H2O
(1)上述反应不属于氧化还原反应的是(填代号)_____________。
(2)H2O2仅体现还原性的反应是(填代号) 。
(3)H2O2既体现氧化性又体现还原性的反应是(填代号) 。
(4)通过以上反应分析,H2O2常称为绿色氧化剂,原因是___________________
(5)上述反应说明H2O2、Ag2O、MnO2氧化性由强到弱的顺序是:
II、(6分)某实验小组为探究ClO-、I2、SO![]() 在酸性条件下的氧化性强弱,设计实验如下:实验①:在淀粉碘化钾溶液中加入少量次氯酸钠(NaClO)溶液,并加入少量的稀硫酸,只发现溶液立即变蓝;(已知I2遇淀粉变蓝)
在酸性条件下的氧化性强弱,设计实验如下:实验①:在淀粉碘化钾溶液中加入少量次氯酸钠(NaClO)溶液,并加入少量的稀硫酸,只发现溶液立即变蓝;(已知I2遇淀粉变蓝)
实验②:向实验①的溶液中加入4 mL 0.5 mol/L的亚硫酸钠(Na2SO3)溶液,蓝色恰好完全褪去。
(1)写出实验①中发生反应的离子方程式
(2)实验②的化学反应中转移电子的物质的量是____________。
(3)以上实验说明,在酸性条件下ClO-、I2、SO![]() 的氧化性由弱到强的顺序是________。
的氧化性由弱到强的顺序是________。