题目内容
(2013?乐山二模)某实验小组为探究铜及其化合物的性质进行如下实验:
(1)铜在一定条件下也能被腐蚀.下列装置中,铜腐蚀的速度最慢的是(填装置序号)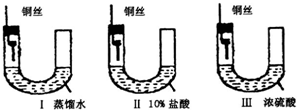
(2)金属铜长期暴露在潮湿空气中往往被腐蚀.生成的“铜锈”受热易分解为氧化铜、二氧化碳和水.为验证“铜锈”分解的部分产物,某同学设计了下图装置:
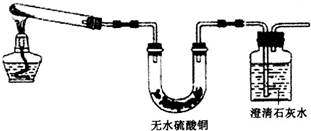
该装置可初步验证“铜锈”分解产物中的
(3)为了从“铜锈”中制得铜并测定“铜锈”的组成,设计实验装置如下:
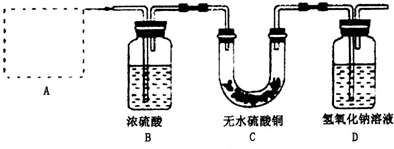
请回答下列问题:
①A处是“铜锈”与氢气反应的装置,应选用下图中的
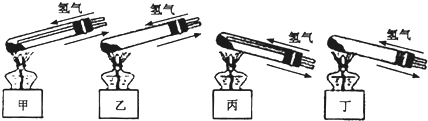
②反应进行时,应先
③要准确测定“铜锈”的组成,实验时C中现象应为
④上述装置还有不完善之处,应将D装置中排出的气体
(1)铜在一定条件下也能被腐蚀.下列装置中,铜腐蚀的速度最慢的是(填装置序号)
Ⅲ
Ⅲ
.
(2)金属铜长期暴露在潮湿空气中往往被腐蚀.生成的“铜锈”受热易分解为氧化铜、二氧化碳和水.为验证“铜锈”分解的部分产物,某同学设计了下图装置:

该装置可初步验证“铜锈”分解产物中的
水、二氧化碳
水、二氧化碳
,为验证分解的其它产物需要做补充,方法是将反应后的试管中的黑色固体溶液质量的稀硫酸中,黑色固体溶解变为蓝色溶液
将反应后的试管中的黑色固体溶液质量的稀硫酸中,黑色固体溶解变为蓝色溶液
.(3)为了从“铜锈”中制得铜并测定“铜锈”的组成,设计实验装置如下:

请回答下列问题:
①A处是“铜锈”与氢气反应的装置,应选用下图中的
丙
丙
(填写编号);
②反应进行时,应先
通入氢气排净装置内空气后
通入氢气排净装置内空气后
再点燃酒精灯加热;③要准确测定“铜锈”的组成,实验时C中现象应为
白色的无水硫酸铜不变色
白色的无水硫酸铜不变色
,需测定的数据有;样品质量、CO2、H2O、Cu
CO2、H2O、Cu
(填化学式)的质量;④上述装置还有不完善之处,应将D装置中排出的气体
点燃或用气球收集
点燃或用气球收集
(填处理的方法)分析:(1)金属生锈的条件是:与氧气接触,有水参加,根据金属的吸氧腐蚀条件来判断;
(2)无水硫酸铜是检验水的、澄清石灰水是检验二氧化碳的;检验氧化铜,可以用稀硫酸溶解黑色固体,溶液会变成蓝色;
(3)①、固体加热分解装置中的大试管要向下倾斜,并且氢气通入到药品的上方位置;
②反应进行时,应先通气体再点灯,防止空气的干扰;
③C装置中的无水硫酸铜不变色,说明铜锈完全分解;要测定“铜绿”的组成,需要知道样品质量以及CO2、H2O和Cu的质量;
④实验中要注意对尾气进行处理,选择合适的处理装置.
(2)无水硫酸铜是检验水的、澄清石灰水是检验二氧化碳的;检验氧化铜,可以用稀硫酸溶解黑色固体,溶液会变成蓝色;
(3)①、固体加热分解装置中的大试管要向下倾斜,并且氢气通入到药品的上方位置;
②反应进行时,应先通气体再点灯,防止空气的干扰;
③C装置中的无水硫酸铜不变色,说明铜锈完全分解;要测定“铜绿”的组成,需要知道样品质量以及CO2、H2O和Cu的质量;
④实验中要注意对尾气进行处理,选择合适的处理装置.
解答:解:(1)金属生锈的条件是:与氧气接触,有水参加,图Ⅲ中浓硫酸具有吸水性,能减少水蒸气的量,可以减慢金属铜腐蚀的速率;
故答案为:Ⅲ;
(2)用无水硫酸铜和澄清石灰水分别检验水和二氧化碳的存在情况;还有一种分解产物氧化铜,可以利用稀硫酸溶解,根据溶液变成蓝色溶液判断黑色固体是氧化铜;
故答案为:水、二氧化碳; 将反应后的试管中的黑色固体溶液质量的稀硫酸中,黑色固体溶解变为蓝色溶液;
(3)①给试管中的固体加热时,为了防止冷凝水倒流入试管底,使试管骤然遇冷而炸裂,大试管的管口应略向下倾斜,并且氢气通入到药品的上方位置,丙正确;
故答案为:丙;
②反应进行时,为了防止空气中氧气的干扰,应先通氢气再点燃酒精灯;
故答案为:通入氢气排净装置内空气后;
③实验时C中无水硫酸铜不再变色,证明铜锈分解完毕;要测定“铜绿”的组成,需要知道样品质量以及CO2、H2O和Cu的质量;
故答案为:白色的无水硫酸铜不变色; CO2、H2O、Cu;
④在实验过程中要注意尾气的处理问题,对于剩余的氢气,可以点燃,或用气球收集;
故答案为:点燃或用气球收集.
故答案为:Ⅲ;
(2)用无水硫酸铜和澄清石灰水分别检验水和二氧化碳的存在情况;还有一种分解产物氧化铜,可以利用稀硫酸溶解,根据溶液变成蓝色溶液判断黑色固体是氧化铜;
故答案为:水、二氧化碳; 将反应后的试管中的黑色固体溶液质量的稀硫酸中,黑色固体溶解变为蓝色溶液;
(3)①给试管中的固体加热时,为了防止冷凝水倒流入试管底,使试管骤然遇冷而炸裂,大试管的管口应略向下倾斜,并且氢气通入到药品的上方位置,丙正确;
故答案为:丙;
②反应进行时,为了防止空气中氧气的干扰,应先通氢气再点燃酒精灯;
故答案为:通入氢气排净装置内空气后;
③实验时C中无水硫酸铜不再变色,证明铜锈分解完毕;要测定“铜绿”的组成,需要知道样品质量以及CO2、H2O和Cu的质量;
故答案为:白色的无水硫酸铜不变色; CO2、H2O、Cu;
④在实验过程中要注意尾气的处理问题,对于剩余的氢气,可以点燃,或用气球收集;
故答案为:点燃或用气球收集.
点评:本题考查了金属铜的腐蚀以及金属铜的化学性质,结合试验进行考察,本题难度中等.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案
相关题目