网址:http://m.1010jiajiao.com/timu3_id_48416[举报]
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯。回答下列问题:
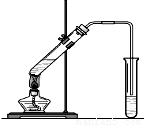
⑴装置中导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止 。
⑵该反应属于哪类反应类型 。
A.加成反应 B.取代反应 C.水解反应 D.酯化反应 E.可逆反应
⑶酯化反应的断键特点是:
⑷写出制取乙酸乙酯的化学反应方程式:
⑸为了证明浓硫酸的作用,某同学进行了以下4个实验。实验开始先用酒精灯微热3 min,再加热使之微微沸腾3 min。实验结束后充分振荡小试管Ⅱ再测有机物的厚度,实验记录如表:
实验编号 试管Ⅰ中试剂 试管Ⅱ中试剂 有机层厚度/cm
A 3 mL乙醇、2 mL乙酸、1 mL 18 mol/L浓硫酸 饱和Na2CO3溶液 5.0
B 3 mL乙醇、2 mL乙酸 饱和Na2CO3溶液 0.1
C 3 mL乙醇、2 mL乙酸、6 mL 3 mol/L硫酸 饱和Na2CO3溶液 1.2
D 3 mL乙醇、2 mL乙酸、一定浓度的盐酸 饱和Na2CO3溶液 1.2
实验D的目的是与实验C对照,证明H+对该反应的催化作用。实验D中加入盐酸的体积和浓度分别是 mL和 mol/L。
查看习题详情和答案>>
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯。回答下列问题:

⑴装置中导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止 。
⑵该反应属于哪类反应类型 。
A加成反应 B取代反应 C水解反应 D酯化反应 E可逆反应
⑶酯化反应的断键特点是:
⑷写出制取乙酸乙酯的化学反应方程式:
⑸为了证明浓硫酸的作用,某同学进行了以下4个实验。实验开始先用酒精灯微热3 min,再加热使之微微沸腾3 min。实验结束后充分振荡小试管Ⅱ再测有机物的厚度,实验记录如表:
实验编号 试管Ⅰ中试剂 试管Ⅱ中试剂 有机层厚度/cm
A 3 mL乙醇、2 mL乙酸、1 mL 18 mol/L浓硫酸 饱和Na2CO3溶液 5.0
B 3 mL乙醇、2 mL乙酸 饱和Na2CO3溶液 0.1
C 3 mL乙醇、2 mL乙酸、6 mL 3 mol/L硫酸 饱和Na2CO3溶液 1.2
D 3 mL乙醇、2 mL乙酸、一定浓度的盐酸 饱和Na2CO3溶液 1.2
实验D的目的是与实验C对照,证明H+对该反应的催化作用。实验D中加入盐酸的体积和浓度分别是 mL和 mol/L。
查看习题详情和答案>>
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯。回答下列问题:
⑴装置中导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止 。
⑵该反应属于哪类反应类型 。
A加成反应 B取代反应 C水解反应 D酯化反应 E可逆反应
⑶酯化反应的断键特点是:
⑷写出制取乙酸乙酯的化学反应方程式:
⑸为了证明浓硫酸的作用,某同学进行了以下4个实验。实验开始先用酒精灯微热3 min,再加热使之微微沸腾3 min。实验结束后充分振荡小试管Ⅱ再测有机物的厚度,实验记录如表:
| 实验编号 | 试管Ⅰ中试剂 | 试管Ⅱ中试剂 | 有机层厚度/cm |
| A | 3 mL乙醇、2 mL乙酸、1 mL 18 mol/L浓硫酸 | 饱和Na2CO3溶液 | 5.0 |
| B | 3 mL乙醇、2 mL乙酸 | 饱和Na2CO3溶液 | 0.1 |
| C | 3 mL乙醇、2 mL乙酸、6 mL 3 mol/L硫酸 | 饱和Na2CO3溶液 | 1.2 |
| D | 3 mL乙醇、2 mL乙酸、一定浓度的盐酸 | 饱和Na2CO3溶液 | 1.2 |
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯。回答下列问题: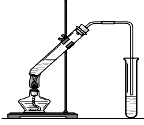
⑴装置中导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止 。
⑵该反应属于哪类反应类型 。
| A.加成反应 | B.取代反应 | C.水解反应 | D.酯化反应 E.可逆反应 |
⑷写出制取乙酸乙酯的化学反应方程式:
⑸为了证明浓硫酸的作用,某同学进行了以下4个实验。实验开始先用酒精灯微热3 min,再加热使之微微沸腾3 min。实验结束后充分振荡小试管Ⅱ再测有机物的厚度,实验记录如表:
| 实验编号 | 试管Ⅰ中试剂 | 试管Ⅱ中试剂 | 有机层厚度/cm |
| A | 3 mL乙醇、2 mL乙酸、1 mL 18 mol/L浓硫酸 | 饱和Na2CO3溶液 | 5.0 |
| B | 3 mL乙醇、2 mL乙酸 | 饱和Na2CO3溶液 | 0.1 |
| C | 3 mL乙醇、2 mL乙酸、6 mL 3 mol/L硫酸 | 饱和Na2CO3溶液 | 1.2 |
| D | 3 mL乙醇、2 mL乙酸、一定浓度的盐酸 | 饱和Na2CO3溶液 | 1.2 |
(8分)
乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。实验室利用右图的装置制备乙酸乙酯。
(1)与教材采用的实验装置不同,此装置中采用了球形干燥管,其作
用是: 。

(2)为证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上图所示装置进行了以下4个实验。实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡小试管II再测有机层的厚度,实验记录如下:
|
实验编号 |
试管Ⅰ中试剂 |
试管Ⅱ中试剂 |
测得有机层的厚度/cm |
|
A |
3 mL乙醇、2 mL乙酸、1mL18mol·L-1 浓硫酸 |
饱和Na2CO3溶液[来源:学,科,网Z,X,X,K][来源:学#科#网] |
5.0[来源:Z§xx§k.Com] |
|
B[来源:学。科。网] |
3 mL乙醇、2 mL乙酸 |
0.1 |
|
|
C |
3 mL乙醇、2 mL乙酸、6 mL 3mol·L-1 H2SO4 |
1.2 |
|
|
D |
3 mL乙醇、2 mL乙酸、盐酸 |
1.2 |
① 实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是__________mL和__________mol·L-1 。
② 分析实验 (填实验编号)的数据,可以推测出浓H2SO4的吸水性提高了乙酸乙酯的产率。
③ 加热有利于提高乙酸乙酯的产率,但实验发现温度过高乙酸乙酯的产率反而降低,可能的原因是 。
查看习题详情和答案>>