摘要:19.对于以下给出的可逆反应:A+2B 2C.已知C是气体.达平衡后同时升高温度并降低压强.又达到新的平衡.若第二次平衡时混和物中C的含量与第一次平衡相同.则下列推断正确的是 A.A不一定是气态物质 B.A一定是气态物质 C.B一定不是气态物质 D.B一定是气态物质
网址:http://m.1010jiajiao.com/timu3_id_45982[举报]
1.分析图1-2后,判断下列E值最大的是( )?

图1-2
A.Mg B.S? C.C D.He?
2.Mg、S、He的E值可由小到大排列为__________。
3.19号元素E值较小的原因是__________。
4.根据以下给出的价电子构型:?
①3s23p1? ②3s23p2 ③3s23p3? ④3s23p4
判断原子的第一电离能的大小顺序。????????
5.Na的第一电离能__________Mg的第一电离能,Na的第二电离能__________Mg的第二电离能。
查看习题详情和答案>>(2009?东城区二模)某化学课外活动小组设计实验探究氮的化合物的性质,装置如图所示(A装置未画出),其中A为气体发生装置.A中所用试剂从下列固体物质中选取:a.NH4HCO3、b.NH4Cl、c.Ca(OH)2、d.NaOH
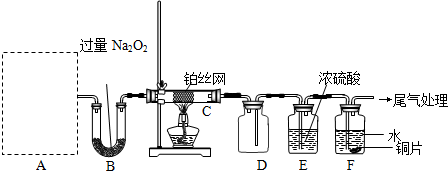
检查装置气密性后,先将C处铂丝网加热至红热,再将A处产生的气体通过B装置片刻后,撤去C处酒精灯.部分实验现象如下:铂丝继续保持红热,F处铜片逐渐溶解.
(1)实验室制取A中气体时若只用一种试剂,该试剂是
(2)A中产生的物质被B中Na2O2充分吸收,写出任意一个B中发生反应的化学方程式:
(3)对于C中发生的可逆反应,下列说法正确的是
a.增大一种反应物的浓度可以提高另一种反应物的转化率
b.工业上进行该反应时,可采取高压的条件提高反应物转化率
c.该反应在一定条件下达到平衡时,反应物的平衡浓度之比一定是4:5
(4)请在下图坐标中画出C装置中反应发生过程中的能量变化示意图,并在虚线上分别标出反应物和生成物的化学式
 .
.
(5)待实验结束后,将B中固体混合物溶于500mL1mol?L-1 盐酸中,产生无色混合气体甲,溶液呈中性,则实验前B中原有Na2O2的物质的量是
查看习题详情和答案>>

检查装置气密性后,先将C处铂丝网加热至红热,再将A处产生的气体通过B装置片刻后,撤去C处酒精灯.部分实验现象如下:铂丝继续保持红热,F处铜片逐渐溶解.
(1)实验室制取A中气体时若只用一种试剂,该试剂是
a
a
(填备选试剂的字母);此时A中主要的玻璃仪器有试管、酒精灯
试管、酒精灯
(填名称).(2)A中产生的物质被B中Na2O2充分吸收,写出任意一个B中发生反应的化学方程式:
2Na2O2+2H2O=4NaOH+O2 或2Na2O2+2CO2=2Na2CO3+O2
2Na2O2+2H2O=4NaOH+O2 或2Na2O2+2CO2=2Na2CO3+O2
.(3)对于C中发生的可逆反应,下列说法正确的是
a
a
.a.增大一种反应物的浓度可以提高另一种反应物的转化率
b.工业上进行该反应时,可采取高压的条件提高反应物转化率
c.该反应在一定条件下达到平衡时,反应物的平衡浓度之比一定是4:5
(4)请在下图坐标中画出C装置中反应发生过程中的能量变化示意图,并在虚线上分别标出反应物和生成物的化学式



(5)待实验结束后,将B中固体混合物溶于500mL1mol?L-1 盐酸中,产生无色混合气体甲,溶液呈中性,则实验前B中原有Na2O2的物质的量是
0.25
0.25
mol,甲在标准状况下是2.8
2.8
L(忽略气体的溶解).I.工业上用CO生产燃料甲醇.一定条件下发生反应:CO(g)+2H2(g)?CH3OH(g).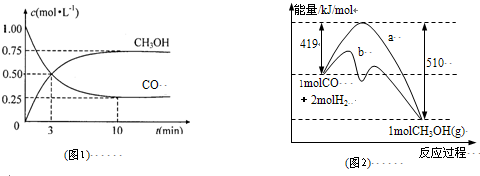
(1)图1是反应时CO和CH3OH(g)的浓度随时间变化情况.从反应开始到平衡,用CO浓度变化表示平均反应速率v(CO)=
(2)图2表示该反应进行过程中能量的变化.曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化.该反应是
(3)该反应平衡常数K的表达式为
(4)恒容条件下,下列措施中能使
增大的有
a.升高温度; b.充入He气 c.再充入1molCO和2molH2 d.使用催化剂
II.(13分)某化学课外活动小组设计实验探究氮的化合物的性质,装置如下图所示(A装置未画出),其中A为气体发生装置.A中所用试剂从下列固体物质中选取:a.NH4HCO3、b.NH4Cl、c.Ca(OH)2、d.NaOH.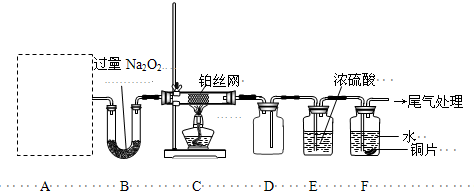
检查装置气密性后,先将C处铂丝网加热至红热,再将A处产生的气体通过B装置片刻后,撤去C处酒精灯.部分实验现象如下:铂丝继续保持红热,F处铜片逐渐溶解.
(1)实验室制取A中气体时若只用一种试剂,该试剂是
(2)A中产生的物质被B中Na2O2充分吸收,写出任意一个B中发生反应的化学方程式:
(3)对于C中发生的可逆反应,下列说法正确的是
a.增大一种反应物的浓度可以提高另一种反应物的转化率
b.工业上进行该反应时,可采取高压的条件提高反应物转化率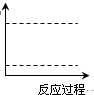
c.该反应在一定条件下达到平衡时,反应物的平衡浓度之比一定是4:5
(4)请在图坐标中画出C装置中反应发生过程中的能量变化示意图,并在虚线上分别标出反应物和生成物的化学式.
(5)待实验结束后,将B中固体混合物溶于500mL1mol?L-1 盐酸中,产生无色混合气体甲,溶液呈中性,则实验前B中原有Na2O2的物质的量是
查看习题详情和答案>>

(1)图1是反应时CO和CH3OH(g)的浓度随时间变化情况.从反应开始到平衡,用CO浓度变化表示平均反应速率v(CO)=
0.075mol?L-1?min-1
0.075mol?L-1?min-1
;(2)图2表示该反应进行过程中能量的变化.曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化.该反应是
放热
放热
(选填“吸热”或“放热”)反应,写出反应的热化学方程式CO(g)+2H2(g)═CH3OH(g)△H=-91KJ/mol
CO(g)+2H2(g)═CH3OH(g)△H=-91KJ/mol
;选择适宜的催化剂,不能
不能
(填“能”或“不能”)改变该反应的反应热;(3)该反应平衡常数K的表达式为
K=
| c(CH3OH) |
| c(CO)×c2(H2) |
K=
,温度升高,平衡常数K| c(CH3OH) |
| c(CO)×c2(H2) |
减小
减小
(填“增大”、“不变”或“减小”);(4)恒容条件下,下列措施中能使
| n(CH3OH) |
| n(CO) |
c
c
.a.升高温度; b.充入He气 c.再充入1molCO和2molH2 d.使用催化剂
II.(13分)某化学课外活动小组设计实验探究氮的化合物的性质,装置如下图所示(A装置未画出),其中A为气体发生装置.A中所用试剂从下列固体物质中选取:a.NH4HCO3、b.NH4Cl、c.Ca(OH)2、d.NaOH.

检查装置气密性后,先将C处铂丝网加热至红热,再将A处产生的气体通过B装置片刻后,撤去C处酒精灯.部分实验现象如下:铂丝继续保持红热,F处铜片逐渐溶解.
(1)实验室制取A中气体时若只用一种试剂,该试剂是
a
a
(填备选试剂的字母);此时A中主要的玻璃仪器有试管、酒精灯(导管)
试管、酒精灯(导管)
(填名称).(2)A中产生的物质被B中Na2O2充分吸收,写出任意一个B中发生反应的化学方程式:
2Na2O2+2H2O=4NaOH+O2↑或2Na2O2+2CO2=2Na2CO3+O2
2Na2O2+2H2O=4NaOH+O2↑或2Na2O2+2CO2=2Na2CO3+O2
.(3)对于C中发生的可逆反应,下列说法正确的是
a
a
.a.增大一种反应物的浓度可以提高另一种反应物的转化率
b.工业上进行该反应时,可采取高压的条件提高反应物转化率

c.该反应在一定条件下达到平衡时,反应物的平衡浓度之比一定是4:5
(4)请在图坐标中画出C装置中反应发生过程中的能量变化示意图,并在虚线上分别标出反应物和生成物的化学式.
(5)待实验结束后,将B中固体混合物溶于500mL1mol?L-1 盐酸中,产生无色混合气体甲,溶液呈中性,则实验前B中原有Na2O2的物质的量是
0.25
0.25
mol,甲在标准状况下是2.8
2.8
L(忽略气体的溶解).类比是化学学习中常用的方法之一,已知硝酸能把铁氧化成Fe(NO3)3,但当铁过量时,产物是Fe(NO3)2.某同学受此启发,提出一个相似的观点:氯气与铁粉反应,当Cl2足量时生成FeCl3,当铁粉过量时产物是FeCl2.为验证该观点是否正确,该同学将一根细的纯铁丝分别在足量和少量的Cl2中点燃,取其表面生成物并分别编号为A、B,然后通过实验确定其成分.探究过程如下:
(1)提出假设:A是FeCl3,B是FeCl2.
(2)设计实验方案:
分别取A、B的溶液均进行以下实验,但实验现象相同.请填写下表中的相应空格.
(3)根据上述实验结论,写出Cl2与铁粉加热时发生反应的化学方程式: .
(4)为进一步探究FeCl3溶液的性质,他又利用A溶液做了如下一些实验,其中明显错误的是: .
A.将A溶液滴入沸水中,并继续加热得到红褐色液体,该液体能产生丁达尔现象
B.向A溶液中加入少量铁粉,铁粉溶解,溶液颜色加深
C.在A溶液中滴加NaOH浓溶液,出现红褐色沉淀
D.将A溶液加热蒸干并灼烧,得到FeCl3固体
(5)实际应用:
①半导体、多媒体行业要用FeCl3溶液做印刷电路铜板腐蚀剂,请写出FeCl3溶液腐蚀印刷电路铜板的离子方程式: .
②腐蚀铜板后的混合溶液中,若Cu2+和Fe3+的浓度均为0.1mol/L,则溶液中Fe2+的浓度为 mol/L,原FeCl3溶液中Fe3+的浓度为 mol/L.
③请参照下表给出的数据和药品,简述除去CuCl2溶液中Fe3+和Fe2+的实验步骤: .
④某科研人员发现劣质不锈钢在酸中腐蚀缓慢,但在某些盐溶液中腐蚀现象明显.请从上表提供的药品中选择两种(水可任选),设计最佳实验,验证劣质不锈钢易被腐蚀.
有关反应的化学方程式 、 .劣质不锈钢腐蚀的实验现象 .
查看习题详情和答案>>
(1)提出假设:A是FeCl3,B是FeCl2.
(2)设计实验方案:
分别取A、B的溶液均进行以下实验,但实验现象相同.请填写下表中的相应空格.
| 实验方法 | 实验现象 | 结 论 |
| 分别向A、B溶液中加 KSCN溶液 |
固体物质中有FeCl3 | |
| 分别向KMnO4溶液中 加适量A、B溶液 |
KMnO4溶液颜色无明显变化 | 固体物质中不含 |
(4)为进一步探究FeCl3溶液的性质,他又利用A溶液做了如下一些实验,其中明显错误的是:
A.将A溶液滴入沸水中,并继续加热得到红褐色液体,该液体能产生丁达尔现象
B.向A溶液中加入少量铁粉,铁粉溶解,溶液颜色加深
C.在A溶液中滴加NaOH浓溶液,出现红褐色沉淀
D.将A溶液加热蒸干并灼烧,得到FeCl3固体
(5)实际应用:
①半导体、多媒体行业要用FeCl3溶液做印刷电路铜板腐蚀剂,请写出FeCl3溶液腐蚀印刷电路铜板的离子方程式:
②腐蚀铜板后的混合溶液中,若Cu2+和Fe3+的浓度均为0.1mol/L,则溶液中Fe2+的浓度为
③请参照下表给出的数据和药品,简述除去CuCl2溶液中Fe3+和Fe2+的实验步骤:
| 氢氧化物 开始沉淀时的pH |
氢氧化物 沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Cu2+ | 4.7 | 6.7 |
| 提供的药品:Cl2、浓H2SO4、NaOH溶液、CuO、Cu | ||
有关反应的化学方程式
按以下步骤可从 合成
合成 (部分试剂和反应条件已略去).
(部分试剂和反应条件已略去).

请回答下列问题:
(1)B、F的结构简式为:B
 F
F
 .
.
(2)反应①~⑦中属于消去反应的是
(3)根据反应 ,写出在同样条件下CH2=CH-CH=CH2与等物质的量Br2发生加成反应的化学方程式:
,写出在同样条件下CH2=CH-CH=CH2与等物质的量Br2发生加成反应的化学方程式:
 .
.
(4)写出第④步C→ 的化学方程式(有机物写结构简式,注明反应条件).
的化学方程式(有机物写结构简式,注明反应条件).
 .
.
(5)与4个不同的原子或原子团相连的碳原子称为手性碳原子;A-G这七种有机物分子中含有手性碳原子的是(填序号)
(6)核磁共振谱是测定有机物分子结构最有用的工具之一.在有机物分子中,不同位置的氢原子在质子核磁共振谱(PMR)中给出的峰值(信号)也不同,根据峰(信号)可以确定有机物分子中氢原子的种类和数目.例如:乙醛的结构式为: ,其PMR谱中有2个信号峰,其强度之比为3:1.则下列有机物分子中,在质子核磁共振谱中能给出三种峰(信号)且强度之比为1:1:2的是
,其PMR谱中有2个信号峰,其强度之比为3:1.则下列有机物分子中,在质子核磁共振谱中能给出三种峰(信号)且强度之比为1:1:2的是
A. B.
B. C.
C. D.
D.
查看习题详情和答案>>
 合成
合成 (部分试剂和反应条件已略去).
(部分试剂和反应条件已略去).
请回答下列问题:
(1)B、F的结构简式为:B




(2)反应①~⑦中属于消去反应的是
②④
②④
(填代号).(3)根据反应
 ,写出在同样条件下CH2=CH-CH=CH2与等物质的量Br2发生加成反应的化学方程式:
,写出在同样条件下CH2=CH-CH=CH2与等物质的量Br2发生加成反应的化学方程式:

(4)写出第④步C→
 的化学方程式(有机物写结构简式,注明反应条件).
的化学方程式(有机物写结构简式,注明反应条件).

(5)与4个不同的原子或原子团相连的碳原子称为手性碳原子;A-G这七种有机物分子中含有手性碳原子的是(填序号)
CE
CE
.(6)核磁共振谱是测定有机物分子结构最有用的工具之一.在有机物分子中,不同位置的氢原子在质子核磁共振谱(PMR)中给出的峰值(信号)也不同,根据峰(信号)可以确定有机物分子中氢原子的种类和数目.例如:乙醛的结构式为:
 ,其PMR谱中有2个信号峰,其强度之比为3:1.则下列有机物分子中,在质子核磁共振谱中能给出三种峰(信号)且强度之比为1:1:2的是
,其PMR谱中有2个信号峰,其强度之比为3:1.则下列有机物分子中,在质子核磁共振谱中能给出三种峰(信号)且强度之比为1:1:2的是BD
BD
.A.
 B.
B. C.
C. D.
D.