网址:http://m.1010jiajiao.com/timu3_id_44805[举报]
| A、气态氢化物的稳定性:乙<丁 | B、原子半径:甲<乙 | C、丙的两种氧化物都是离子化合物 | D、甲、乙、丁的最高价氧化物对应的水化物酸性依次增强 |
| A.气态氢化物的稳定性:乙<丁 |
| B.原子半径:甲<乙 |
| C.丙的两种氧化物都是离子化合物 |
| D.甲、乙、丁的最高价氧化物对应的水化物酸性依次增强 |
短周期元素甲、乙、丙、丁的原子序数依次增大。甲的最高价氧化物与乙的气态氢化物同时通入水中,得到的生成物既可与酸反应又可与碱反应。丙位于第ⅠA族,丁原子的核外电子总数是其最外层电子数的3倍,则 ( )。
| A.气态氢化物的稳定性:乙<丁 |
| B.原子半径:甲<乙 |
| C.丙的两种氧化物都是离子化合物 |
| D.甲、乙、丁的最高价氧化物对应的水化物酸性依次增强 |
(14分)某短周期元素的原子最外层电子数为次外层的2倍,其单质甲可发生如下反应:
甲 + 乙丙 + 丁 + 水。
(1)若丙为NO2。
①甲与乙反应的化学方程式为 。
②火箭常用NO2的二聚体N2O4作氧化剂,肼(N2H4)作燃料,已知:
N2(g)+2O2(g)=2NO2(g) △H =-67.7kJ·mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=-534.0kJ·mol-1
2NO2(g)N2O4(g) △H =-52.7kJ·mol-1
试写出气态肼(N2H4)在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式:
___________________________________________________。
③肼又称联氨,广泛用于火箭推进剂、有机合成及燃料电池。肼燃料电池原理如右图所示,右边电极为 (填“正极”、“负极”),左边电极上发生的电极反应式为 。
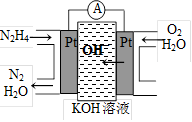
(2)若丙为SO2。
①把乙滴入硫酸铜晶体中,观察到的现象是 。
②SO2气体有毒,多余的SO2气体常用足量的NaOH溶液吸收,写出吸收液中离子浓度由大到小的顺序: 。
③在氧化还原反应的过程中,氧化反应和还原反应同时发生,有关反应:
SO2-2e-+2H2O =SO42-+4H+反应的说法错误的是 。
A.该反应为氧化反应
B.上述反应中若转移电子物质的量为0.05mol,则生成溶液的PH值为1
C.Fe2(SO4)3、品红两种溶液都能使上述反应进行
D.通入Cl2会降低SO2的漂白作用
查看习题详情和答案>>
(14分)某短周期元素的原子最外层电子数为次外层的2倍,其单质甲可发生如下反应:
甲 + 乙 丙 + 丁 + 水。
丙 + 丁 + 水。
(1)若丙为NO2。
①甲与乙反应的化学方程式为 。
②火箭常用NO2的二聚体N2O4作氧化剂,肼(N2H4)作燃料,已知:
N2(g)+2O2(g)=2NO2(g) △H =-67.7kJ·mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H =-534.0kJ·mol-1
2NO2(g) N2O4(g) △H =-52.7kJ·mol-1
N2O4(g) △H =-52.7kJ·mol-1
试写出气态肼(N2H4)在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式:
___________________________________________________。
③肼又称联氨,广泛用于火箭推进剂、有机合成及燃料电池。肼燃料电池原理如右图所示,右边电极为 (填“正极”、“负极”),左边电极上发生的电极反应式为 。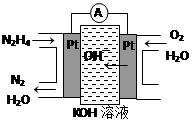
(2)若丙为SO2。
①把乙滴入硫酸铜晶体中,观察到的现象是 。
②SO2气体有毒,多余的SO2气体常用足量的NaOH溶液吸收,写出吸收液中离子浓度由大到小的顺序: 。
③在氧化还原反应的过程中,氧化反应和还原反应同时发生,有关反应:
SO2-2e-+2H2O = SO42-+4H+反应的说法错误的是 。
| A.该反应为氧化反应 |
| B.上述反应中若转移电子物质的量为0.05mol,则生成溶液的PH值为1 |
| C.Fe2(SO4)3、品红两种溶液都能使上述反应进行 |
| D.通入Cl2会降低SO2的漂白作用 |