摘要:某厂废液中含有大量...用下列图示方法进行分离: (1)写出下列物质的化学式: 试剂x .试剂z . 晶体E .固体G (2)写出下列反应的离子方程式: 沉淀A+试剂y: 滤液D+过量:
网址:http://m.1010jiajiao.com/timu3_id_43628[举报]
某工厂废液中含有大量 ![]() 、
、 ![]() 、
、 ![]() ,用下列图示方法进行分离利用(部分反应条件省略):(已知试剂z是医药工业中常用的有甜味的白色晶体)
,用下列图示方法进行分离利用(部分反应条件省略):(已知试剂z是医药工业中常用的有甜味的白色晶体)
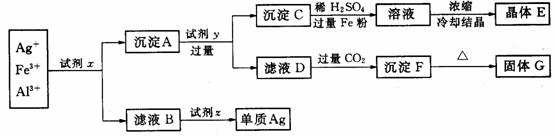
(1)写出下列物质的化学式:试剂x________、试剂z________、晶体E________、固体G________.
(2)写出下列反应的离子方程式:
沉淀A+试剂y:___________;滤液D+过量 ![]() :_______________________
:_______________________
某厂废液中含有大量Ag+、Fe3+、Al3+,用下列图示方法进行分离(部分反应条件省略).
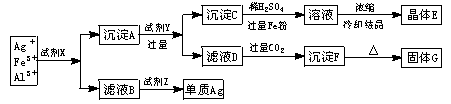
(1)写出下列物质的化学式:
试剂X_______. 试剂Z_______.
晶体E_______. 固体G_______.
(2)写出下列反应的离子方程式:
沉淀A+试剂Y:___________________.
滤液D+过量CO2:__________________.
查看习题详情和答案>>
海水资源丰富,海水中主要含有Na+、K+、Mg2+、Cl-、SO2-4、Br-、CO2-3、HCO-3等离子.合理利用海水资源和保护环境是我国可持续发展的重要保证.
Ⅰ.火力发电燃烧煤排放的SO2会造成一系列环境和生态问题.利用海水脱硫是一种有效的方法,其工艺流程如下图所示:
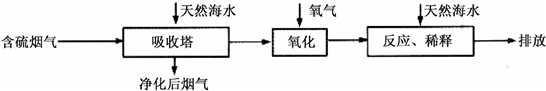
(1)天然海水的pH≈8,呈弱碱性.用离子方程式解释原因______.
(2)天然海水吸收了含硫烟气后,要用O2进行氧化处理,其反应的化学方程式是______;氧化后的“海水”需要用大量的天然海水与之混合后才能排放,该操作的主要目的是______.
Ⅱ.重金属离子对河流及海洋造成严重污染.某化工厂废水(pH=2.0,ρ≈1g?mL-1)中含有Ag+、Pb2+等重金属离子,其浓度各约为0.1mol?L-1.排放前拟用沉淀法除去这两种离子,查找有关数据如下:
(3)你认为往废水中投入______(填字母序号),沉淀效果最好.
A.NaOH B.Na2S C.KID.Ca(OH)2
(4)如果用生石灰处理上述废水,使溶液的pH=8.0,处理后的废水中c(Pb2+)=______.
(5)如果用食盐处理其只含Ag+的废水,测得处理后的废水中NaCl的质量分数为0.117%.若环境要求排放标准为c(Ag+)低于1.0×10-8mol?L-1,问该工厂处理后的废水中c(Ag+)=______,是否符合排放标准______(填“是”或“否”).
已知KSP(AgCl)=1.8×1-10mol?L2.
查看习题详情和答案>>
Ⅰ.火力发电燃烧煤排放的SO2会造成一系列环境和生态问题.利用海水脱硫是一种有效的方法,其工艺流程如下图所示:

(1)天然海水的pH≈8,呈弱碱性.用离子方程式解释原因______.
(2)天然海水吸收了含硫烟气后,要用O2进行氧化处理,其反应的化学方程式是______;氧化后的“海水”需要用大量的天然海水与之混合后才能排放,该操作的主要目的是______.
Ⅱ.重金属离子对河流及海洋造成严重污染.某化工厂废水(pH=2.0,ρ≈1g?mL-1)中含有Ag+、Pb2+等重金属离子,其浓度各约为0.1mol?L-1.排放前拟用沉淀法除去这两种离子,查找有关数据如下:
| 难溶电解质 | AgI | AgOH | Ag2S | pbI2 | Pb(OH)2 | PbS |
| Ksp | 8.3×10-17 | 5.6×10-8 | 6.3×10-50 | 7.1×10-9 | 1.2×10-15 | 3.4×10-28 |
A.NaOH B.Na2S C.KID.Ca(OH)2
(4)如果用生石灰处理上述废水,使溶液的pH=8.0,处理后的废水中c(Pb2+)=______.
(5)如果用食盐处理其只含Ag+的废水,测得处理后的废水中NaCl的质量分数为0.117%.若环境要求排放标准为c(Ag+)低于1.0×10-8mol?L-1,问该工厂处理后的废水中c(Ag+)=______,是否符合排放标准______(填“是”或“否”).
已知KSP(AgCl)=1.8×1-10mol?L2.
海水资源丰富,海水中主要含有Na+、K+、Mg2+、Cl-、SO2-4、Br-、CO2-3、HCO-3等离子.合理利用海水资源和保护环境是我国可持续发展的重要保证.
Ⅰ.火力发电燃烧煤排放的SO2会造成一系列环境和生态问题.利用海水脱硫是一种有效的方法,其工艺流程如下图所示:
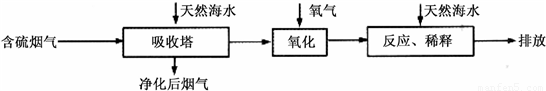
(1)天然海水的pH≈8,呈弱碱性.用离子方程式解释原因______.
(2)天然海水吸收了含硫烟气后,要用O2进行氧化处理,其反应的化学方程式是______;氧化后的“海水”需要用大量的天然海水与之混合后才能排放,该操作的主要目的是______.
Ⅱ.重金属离子对河流及海洋造成严重污染.某化工厂废水中含有Ag+、Pb2+等重金属离子,其浓度各约为0.1mol?L-1.排放前拟用沉淀法除去这两种离子,查找有关数据如下:
(3)你认为往废水中投入______(填字母序号),沉淀效果最好.
A.NaOH B.Na2S C.KID.Ca(OH)2
(4)如果用生石灰处理上述废水,使溶液的pH=8.0,处理后的废水中c(Pb2+)=______.
(5)如果用食盐处理其只含Ag+的废水,测得处理后的废水中NaCl的质量分数为0.117%.若环境要求排放标准为c(Ag+)低于1.0×10-8mol?L-1,问该工厂处理后的废水中c(Ag+)=______,是否符合排放标准______(填“是”或“否”).
已知KSP(AgCl)=1.8×1-10mol?L2.
查看习题详情和答案>>
Ⅰ.火力发电燃烧煤排放的SO2会造成一系列环境和生态问题.利用海水脱硫是一种有效的方法,其工艺流程如下图所示:

(1)天然海水的pH≈8,呈弱碱性.用离子方程式解释原因______.
(2)天然海水吸收了含硫烟气后,要用O2进行氧化处理,其反应的化学方程式是______;氧化后的“海水”需要用大量的天然海水与之混合后才能排放,该操作的主要目的是______.
Ⅱ.重金属离子对河流及海洋造成严重污染.某化工厂废水中含有Ag+、Pb2+等重金属离子,其浓度各约为0.1mol?L-1.排放前拟用沉淀法除去这两种离子,查找有关数据如下:
| 难溶电解质 | AgI | AgOH | Ag2S | pbI2 | Pb(OH)2 | PbS |
| Ksp | 8.3×10-17 | 5.6×10-8 | 6.3×10-50 | 7.1×10-9 | 1.2×10-15 | 3.4×10-28 |
A.NaOH B.Na2S C.KID.Ca(OH)2
(4)如果用生石灰处理上述废水,使溶液的pH=8.0,处理后的废水中c(Pb2+)=______.
(5)如果用食盐处理其只含Ag+的废水,测得处理后的废水中NaCl的质量分数为0.117%.若环境要求排放标准为c(Ag+)低于1.0×10-8mol?L-1,问该工厂处理后的废水中c(Ag+)=______,是否符合排放标准______(填“是”或“否”).
已知KSP(AgCl)=1.8×1-10mol?L2.
查看习题详情和答案>>
海水资源丰富,海水中主要含有Na+、K+、Mg2+、Cl-、SO2-4、Br-、CO2-3、HCO-3等离子.合理利用海水资源和保护环境是我国可持续发展的重要保证.
Ⅰ.火力发电燃烧煤排放的SO2会造成一系列环境和生态问题.利用海水脱硫是一种有效的方法,其工艺流程如下图所示:
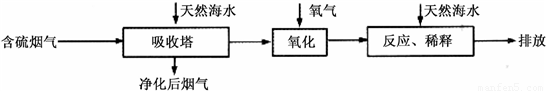
(1)天然海水的pH≈8,呈弱碱性.用离子方程式解释原因______.
(2)天然海水吸收了含硫烟气后,要用O2进行氧化处理,其反应的化学方程式是______;氧化后的“海水”需要用大量的天然海水与之混合后才能排放,该操作的主要目的是______.
Ⅱ.重金属离子对河流及海洋造成严重污染.某化工厂废水中含有Ag+、Pb2+等重金属离子,其浓度各约为0.1mol?L-1.排放前拟用沉淀法除去这两种离子,查找有关数据如下:
(3)你认为往废水中投入______(填字母序号),沉淀效果最好.
A.NaOH B.Na2S C.KID.Ca(OH)2
(4)如果用生石灰处理上述废水,使溶液的pH=8.0,处理后的废水中c(Pb2+)=______.
(5)如果用食盐处理其只含Ag+的废水,测得处理后的废水中NaCl的质量分数为0.117%.若环境要求排放标准为c(Ag+)低于1.0×10-8mol?L-1,问该工厂处理后的废水中c(Ag+)=______,是否符合排放标准______(填“是”或“否”).
已知KSP(AgCl)=1.8×1-10mol?L2.
查看习题详情和答案>>
Ⅰ.火力发电燃烧煤排放的SO2会造成一系列环境和生态问题.利用海水脱硫是一种有效的方法,其工艺流程如下图所示:

(1)天然海水的pH≈8,呈弱碱性.用离子方程式解释原因______.
(2)天然海水吸收了含硫烟气后,要用O2进行氧化处理,其反应的化学方程式是______;氧化后的“海水”需要用大量的天然海水与之混合后才能排放,该操作的主要目的是______.
Ⅱ.重金属离子对河流及海洋造成严重污染.某化工厂废水中含有Ag+、Pb2+等重金属离子,其浓度各约为0.1mol?L-1.排放前拟用沉淀法除去这两种离子,查找有关数据如下:
| 难溶电解质 | AgI | AgOH | Ag2S | pbI2 | Pb(OH)2 | PbS |
| Ksp | 8.3×10-17 | 5.6×10-8 | 6.3×10-50 | 7.1×10-9 | 1.2×10-15 | 3.4×10-28 |
A.NaOH B.Na2S C.KID.Ca(OH)2
(4)如果用生石灰处理上述废水,使溶液的pH=8.0,处理后的废水中c(Pb2+)=______.
(5)如果用食盐处理其只含Ag+的废水,测得处理后的废水中NaCl的质量分数为0.117%.若环境要求排放标准为c(Ag+)低于1.0×10-8mol?L-1,问该工厂处理后的废水中c(Ag+)=______,是否符合排放标准______(填“是”或“否”).
已知KSP(AgCl)=1.8×1-10mol?L2.
查看习题详情和答案>>