摘要: 在100mL硝酸的物质的量浓度为0.4mol/L.硫酸的物质的量浓度为0.1mol/L.加人1.92g铜粉.微热.待充分反应后放出NO气体为 ( ) (B)0.3g (C)0.015mol (D)无法计算
网址:http://m.1010jiajiao.com/timu3_id_435092[举报]
(2010?南通模拟)合成氨是人类科学技术发展史上的一项重大突破,目前工业上用氢气和氮气直接合成氨,制得的氨通过催化氧化可生产硝酸.在一定条件下,若N2和H2以体积比1:3的比例充入一体积不变的密闭容器中反应,达到平衡状态时,测得混合气体中氨的体积分数为20.0%,则:
(1)合成氨反应达到平衡的标志
A.容器内气体压强保持不变
B.容器内各物质的浓度不随时间变化
C.当υ(H2,正)=0.3mol?L-1?min-1,υ(NH3,逆)=0.2mol?L-1?min-1时
D.1个N≡N键断裂的同时,有3个H-H键形成
(2)达到平衡时,N2和H2的转化率分别为
(3)用氨催化氧化可生产硝酸,取所生产的硝酸溶液100mL,与足量的铜反应,生成的NO2和NO混合气体在标准状况下体积为6.72L,物质的量之比为2:1,求所生产硝酸的物质的量浓度?(请写出该小题的计算过程)
(4)某厂用NH3生产硝酸,然后再制硝酸铵,其过程如下:
其中反应②为:4NO+3O2+2H2O=4HNO3,原料气为氨气和空气的混合物.若实际生产中,反应①、②、③的转化率(或利用率)分别为a、b、c,则生产硝酸的氨气占所用氨气总量的体积分数为
.
查看习题详情和答案>>
(1)合成氨反应达到平衡的标志
ABCD
ABCD
.A.容器内气体压强保持不变
B.容器内各物质的浓度不随时间变化
C.当υ(H2,正)=0.3mol?L-1?min-1,υ(NH3,逆)=0.2mol?L-1?min-1时
D.1个N≡N键断裂的同时,有3个H-H键形成
(2)达到平衡时,N2和H2的转化率分别为
33.3%
33.3%
.(3)用氨催化氧化可生产硝酸,取所生产的硝酸溶液100mL,与足量的铜反应,生成的NO2和NO混合气体在标准状况下体积为6.72L,物质的量之比为2:1,求所生产硝酸的物质的量浓度?(请写出该小题的计算过程)
8mol/L
8mol/L
.(4)某厂用NH3生产硝酸,然后再制硝酸铵,其过程如下:

其中反应②为:4NO+3O2+2H2O=4HNO3,原料气为氨气和空气的混合物.若实际生产中,反应①、②、③的转化率(或利用率)分别为a、b、c,则生产硝酸的氨气占所用氨气总量的体积分数为
| 1 |
| 1+ab |
| 1 |
| 1+ab |
硫酸和硝酸是中学阶段常见的强酸.根据二者与金属的反应情况,回答下列问题:
(1)①在100mL 18mol?L-1的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是
②若向上述反应①的体系中再加入硝酸钠,有什么现象出现?用必要的文字和离子方程式加以说明
(2)若将过量铜粉与一定量浓硝酸反应,当反应完全停止时,共收集气体1.12L(标准状况),则该气体的成分是
查看习题详情和答案>>
(1)①在100mL 18mol?L-1的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是
D
D
.A.33.6L B.22.4L C.20.16L D.6.72L②若向上述反应①的体系中再加入硝酸钠,有什么现象出现?用必要的文字和离子方程式加以说明
铜片继续溶解,有无色气体生成(无色气体后变为红棕色),有关离子方程式为:
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
铜片继续溶解,有无色气体生成(无色气体后变为红棕色),有关离子方程式为:
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
.3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
(2)若将过量铜粉与一定量浓硝酸反应,当反应完全停止时,共收集气体1.12L(标准状况),则该气体的成分是
NO2、NO
NO2、NO
,反应中所消耗的硝酸的物质的量可能为下列数据中的B
B
.A.0.1mol B.0.15mol C.0.2mol D.0.25mol.某课外活动小组设计了以下实验方案验证Ag与浓HNO3反应的过程中可能产生NO.其实验流程图如下:

(1)测定硝酸的物质的量反应结束后,从如图B装置中所得100mL溶液中取出25.00mL溶液,用0.1mol?L-1的NaOH溶液滴定,用酚酞作指示剂,滴定前后的滴定管中液面的位置如图所示.
在B容器中生成硝酸的物质的量为
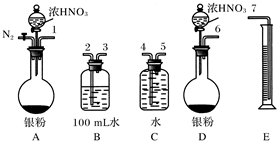
(2)测定NO的体积
①从图所示的装置中,你认为应选用
②选用图所示仪器组合一套可用来测定生成NO体积的装置,其合理的连接顺序是
③在读取量筒内液体体积之前,应进行的操作
(3)气体成分分析
若实验测得NO的体积为112.0mL(已折算到标准状况),则Ag与浓硝酸反应的过程中
查看习题详情和答案>>

(1)测定硝酸的物质的量反应结束后,从如图B装置中所得100mL溶液中取出25.00mL溶液,用0.1mol?L-1的NaOH溶液滴定,用酚酞作指示剂,滴定前后的滴定管中液面的位置如图所示.
在B容器中生成硝酸的物质的量为
0.008mol
0.008mol
,则Ag与浓硝酸反应过程中生成的NO2的物质的量为0.012mol
0.012mol
.
(2)测定NO的体积
①从图所示的装置中,你认为应选用
A
A
装置进行Ag与浓硝酸反应实验,选用的理由是因为A装置可以通入N2将装置中的空气排尽,防止NO被空气中O2氧化
因为A装置可以通入N2将装置中的空气排尽,防止NO被空气中O2氧化
.②选用图所示仪器组合一套可用来测定生成NO体积的装置,其合理的连接顺序是
123547
123547
(填各导管口编号).③在读取量筒内液体体积之前,应进行的操作
等液体冷却到室温,并使集气瓶和量筒内液面相平
等液体冷却到室温,并使集气瓶和量筒内液面相平
.(3)气体成分分析
若实验测得NO的体积为112.0mL(已折算到标准状况),则Ag与浓硝酸反应的过程中
有
有
(填“有”或“没有”)NO产生,作此判断的依据是因为NO2与水反应生成的NO的体积小于收集到的NO的体积(89.6<112.0)
因为NO2与水反应生成的NO的体积小于收集到的NO的体积(89.6<112.0)
.盐酸、硫酸和硝酸是中学阶段常见的三种强酸.请就三者与金属铜的反应情况,回答下列问题:
(1)①在100mL 18mol?L-1的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是
A.40.32L B. 6.72L C.20.16L D.30.24L
②若使上述反应①中剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式
(2)若将过量铜粉与一定量浓硝酸反应,当反应完全停止时,共收集到的气体1.12L(标准状况),则该气体的成分是
A. 0.25mol B. 0.2mol C.0.15mol D.0.1mol
(3)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,并且该反应的产物只有氯化铜和水.该反应的化学方程式为
查看习题详情和答案>>
(1)①在100mL 18mol?L-1的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是
B
B
A.40.32L B. 6.72L C.20.16L D.30.24L
②若使上述反应①中剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
.(2)若将过量铜粉与一定量浓硝酸反应,当反应完全停止时,共收集到的气体1.12L(标准状况),则该气体的成分是
NO2、NO
NO2、NO
,反应中所消耗的硝酸的物质的量可能为C
C
.A. 0.25mol B. 0.2mol C.0.15mol D.0.1mol
(3)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,并且该反应的产物只有氯化铜和水.该反应的化学方程式为
Cu+H2O2+2HCl=CuCl2+2H2O
Cu+H2O2+2HCl=CuCl2+2H2O
.盐酸、硫酸和硝酸是中学阶段常见的三种强酸.
Ⅰ.请就三者与金属铜的反应情况,回答下列问题:
(1)在100mL、18mol?L-1 的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准情况下的体积可能是
A.40.32L B.30.24L C.20.16L D.6.72L
(2)若将过量铜粉与一定量浓硝酸反应,当反应完全停止时,共收集到的气体1.12L(标准状况),则该气体的成分是
A.0.1mol B.0.15mol C.0.2mol D.0.25mol
(3)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,并且该反应的产物只有氯化铜和水.该反应的化学方程式为
Ⅱ.用如下装置可以完成HCl的制取及后续一系列的性质实验(图中夹持装置已略去).
请回答下列问题:
(1)装置A选用浓硫酸和浓盐酸混合制取HCl气体,p中盛装试剂为
(2)装置B中的四处棉花依次做了如下处理:①包有某潮湿的固体物质 ②蘸有KI溶液③蘸有石蕊溶液 ④蘸有浓NaOH溶液.反应开始后,观察到②处有棕黄色物质产生,写出②处发生反应的离子方程式
a.MnO2 b.KmnO4 C.KCl d.Cu
(3)在整个实验过程中,在③处能观察到的现象是
查看习题详情和答案>>
Ⅰ.请就三者与金属铜的反应情况,回答下列问题:
(1)在100mL、18mol?L-1 的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准情况下的体积可能是
D
D
A.40.32L B.30.24L C.20.16L D.6.72L
(2)若将过量铜粉与一定量浓硝酸反应,当反应完全停止时,共收集到的气体1.12L(标准状况),则该气体的成分是
NO2、NO
NO2、NO
,反应中所消耗的硝酸的物质的量可能为B
B
.A.0.1mol B.0.15mol C.0.2mol D.0.25mol
(3)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,并且该反应的产物只有氯化铜和水.该反应的化学方程式为
Cu+H2O2+2HCl=CuCl2+2H2O
Cu+H2O2+2HCl=CuCl2+2H2O
.Ⅱ.用如下装置可以完成HCl的制取及后续一系列的性质实验(图中夹持装置已略去).

请回答下列问题:
(1)装置A选用浓硫酸和浓盐酸混合制取HCl气体,p中盛装试剂为
浓硫酸
浓硫酸
.(2)装置B中的四处棉花依次做了如下处理:①包有某潮湿的固体物质 ②蘸有KI溶液③蘸有石蕊溶液 ④蘸有浓NaOH溶液.反应开始后,观察到②处有棕黄色物质产生,写出②处发生反应的离子方程式
CI2+2I-=2Cl-+I2
CI2+2I-=2Cl-+I2
.在①处包有的固体物质可能是a.MnO2 b.KmnO4 C.KCl d.Cu
(3)在整个实验过程中,在③处能观察到的现象是
先变红后褪色
先变红后褪色
.