摘要:39.方程式配平后.Br-/ClO3-是多少? (A) 1/1 (B) 2/1 (C) 3/1 (D) 5/1
网址:http://m.1010jiajiao.com/timu3_id_434948[举报]
六种短周期元素aA、bB、cC、dD、eE、fF,已知原子序数大小关系是:a<e<c<b<f<d,且a+b=
;六种元素在周期表中的位置关系是:A、B同主族,C、D也同主族;C、E相邻,B、F也相邻.
(1)E、F形成的化合物甲的电子式为
 ,该化合物与A2C反应的化学方程式:
,该化合物与A2C反应的化学方程式:
(2)写出分别由A、B、C、D四种元素所形成的两种化合物的水溶液相互反应的离子方程式:
(3)已知B+BEC3-B2C+E2,请将方程式配平后用双线桥表示电子的转移情况
 .
.
(4)A、E形成的四原子核化合物丙容易液化,其原因是:
(5)经检测,某固体粉末中仅含有B、C两种元素组成的化合物,请设计实验方案探究该固体粉末的成分
查看习题详情和答案>>
| (c+d) | 2 |
(1)E、F形成的化合物甲的电子式为


Mg3N2+6H2O=3Mg(OH)2+2NH3↑
Mg3N2+6H2O=3Mg(OH)2+2NH3↑
.(2)写出分别由A、B、C、D四种元素所形成的两种化合物的水溶液相互反应的离子方程式:
H++HSO3-=SO2↑+H2O
H++HSO3-=SO2↑+H2O
.(3)已知B+BEC3-B2C+E2,请将方程式配平后用双线桥表示电子的转移情况


(4)A、E形成的四原子核化合物丙容易液化,其原因是:
氨分子之间易形成氢键
氨分子之间易形成氢键
.由A、C、E三种元素形成的离子化合物溶液中,离子浓度由大到小顺序为NO3->NH4+>H+>OH-
NO3->NH4+>H+>OH-
.(5)经检测,某固体粉末中仅含有B、C两种元素组成的化合物,请设计实验方案探究该固体粉末的成分
可能的组成为Na2O2,Na2O或两个都有.将粉末加入水中,若无气体生成,则为Na2O,若有气体生成,可根据一定量该固体粉末产生气体的量确定其全部为Na2O2或是两者的混合物
可能的组成为Na2O2,Na2O或两个都有.将粉末加入水中,若无气体生成,则为Na2O,若有气体生成,可根据一定量该固体粉末产生气体的量确定其全部为Na2O2或是两者的混合物
.(2009?吉林模拟)根据下表信息,下列叙述中正确的是( )
|
查看习题详情和答案>>
 (1)环境专家认为可以用铝将水中的NO3- 转化为N2,从而清除污染.该反应中涉及的粒子有:H2O、Al、OH-、Al(OH)3、NO3-、N2,请将各粒子分别填入以下空格(请将整个方程式配平后写在答题纸上).
(1)环境专家认为可以用铝将水中的NO3- 转化为N2,从而清除污染.该反应中涉及的粒子有:H2O、Al、OH-、Al(OH)3、NO3-、N2,请将各粒子分别填入以下空格(请将整个方程式配平后写在答题纸上).NO3-+
10Al
10Al
+18H2O
18H2O
→10Al(OH)3
10Al(OH)3
+3N2
3N2
+6OH-
6OH-
该反应过程中,被氧化与被还原的元素的物质的量之比为5:3
5:3
.(2)若4Al(s)+3O2(g)=2Al2O3(s)△H=-a KJ/mol
Fe2O3(s)+
| 3 |
| 2 |
| 3 |
| 2 |
C(s)+O2(g)=CO2(g)△H=-c KJ/mol
写出Al与氧化铁发生铝热反应的热化学方程式:
2Al(s)+Fe2O3(s)=2Fe(s)+Al2O3(s)△H=-(
a-b-
c)KJ/mol
| 1 |
| 2 |
| 3 |
| 2 |
2Al(s)+Fe2O3(s)=2Fe(s)+Al2O3(s)△H=-(
a-b-
c)KJ/mol
.| 1 |
| 2 |
| 3 |
| 2 |
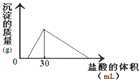
(3)将一定质量的钠铝合金置于水中,合金全部溶解,得到20mL PH=14的溶液,然后用2mol/L的盐酸滴定,可得到沉淀量与消耗的盐酸体积关系如图:则反应过程中产生氢气的总体积为
2.016
2.016
L(标准状况).(11分).下表是某食用碘盐包装袋上的部分说明:
| 配 料 | 食盐、碘酸钾、抗结剂 |
| 碘含量 | 35±15mg/kg |
| 储藏方法 | 密封、避光、防潮 |
| 食用方法 | 烹饪时,待食品熟后加入碘盐 |
(1)下列说法正确的是 。
A.碘酸钾易挥发 B.高温会导致碘的损失
C.用淀粉就能直接检验碘盐中的碘酸钾 D.碘酸钾可氧化氯化钠
(2)碘酸钾与碘化钾在酸性条件下发生如下反应:KIO3+KI+H2SO4→K2SO4+I2+H2O(未配平),该化学方程式配平后系数依次为 。
w.该反应的还原剂为 ;1mol KIO3完全反应转移的电子总数为 。
(3)碘不能多也不能少。已知:I2+2S2O32-=2I-+S4O62-,我校化学兴趣小组测定某食用碘盐中碘的含量。其步骤为:
①准确称取w g食盐,加适量蒸馏水使其完全溶解;②用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;③以淀粉为指示剂,逐滴加入物质的量浓度为1.0×11-3mol·L-1的Na2S2O3溶液20.0mL,恰好反应完全。则所测盐中碘的含量是(以含w的代数式表示) mg/kg。 查看习题详情和答案>>
(1)环境专家认为可以用铝将水中的NO3﹣ 转化为N2,从而清除污染.该反应中涉及的粒子有:H2O、Al、OH﹣、Al(OH)3、NO3﹣、N2,请将各粒子分别填入以下空格(请将整个方程式配平后写在答题纸上).
NO3﹣+ + → + + ﹣ 该反应过程中,被氧化与被还原的元素的物质的量之比为 .
(2)若4Al(s)+3O2(g)=2Al2O3(s)△H=﹣a KJ/mol
Fe2O3(s)+C(s)=CO2(g)+2Fe (s)△H=+b KJ/mol
C(s)+O2(g)=CO2(g)△H=﹣c KJ/mol
写出Al与氧化铁发生铝热反应的热化学方程式: .
(3)将一定质量的钠铝合金置于水中,合金全部溶解,得到20mL PH=14的溶液,然后用2mol/L的盐酸滴定,可得到沉淀量与消耗的盐酸体积关系如图:则反应过程中产生氢气的总体积为 L(标准状况)

查看习题详情和答案>>