网址:http://m.1010jiajiao.com/timu3_id_434853[举报]
(1)甲醛溶液可用于浸制生物标本,这主要是利用了甲醛的何种化学性质
(2)由生物质能获得的CO和H2,可以合成多种有机物.当CO和H2以物质的量1:1催化反应,其原子利用率达100%,合成的物质可能是
a.汽油 b.甲醇 c.甲醛 d.乙酸
(3)工业上合成甲醇的反应:CO(g)+2H2(g)?CH3OH(g)△H=-90.8kJ/mol.
若在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得
反应达到平衡时的有关数据如下:
| 1.容器 | 2.甲 | 3.乙 | 4.丙 |
| 5.反应物投入量 | 6.1molCO、2molH2 | 7.l molCH3OH | 8.2molCO、4molH2 |
| 9.CH30H昀浓度(mol/L) | 10.cl | 11.c2 | 12.c3 |
| 13.反应的能量变化 | 14.放出Q1kJ | 15.吸收Q2kJ | 16.放出Q3kJ |
| 17.平衡常数 | 18.Kl | 19.K2 | 20.K3 |
| 21.反应物转化率 | 22.al | 23.a2 | 24.a3 |
A.cl=c2 B.2Q1=Q3 C.KI=K3 D.a2+a3<100%
(4)一定温度和压强下,CO和H2催化合成二甲醚的反应为:
3H2 (g)+3CO (g) CH3OCH3 (g)+CO2(g)
若一体积可变的密闭容器中充入3mol H2、3molCO、l mol CH3OCH3、l mol CO2,经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍.平衡时
n(CH3OCH3)=
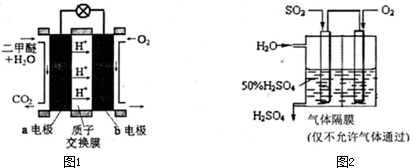
(5)如图1为绿色电源“直接二甲醚燃料电池”的工作原理示意图.b电极是
(6)利用生物质资源过程中会产生SO2,可利用如图2所示装置,用电化学原理生产硫酸为稳定持续生产,硫酸溶液的浓度应维持不变,则通入SO2和水的质量比为
下列离子方程式中正确的是______________
(1)氢氧化亚铁溶于稀硝酸中:Fe(OH)2 + 2H+ = Fe2+ + 2H2O
(2)过量的NaHSO4与Ba(OH)2溶液反应: Ba2++2OH-+2H++SO42-= BaSO4↓+2H2O
(3)向Ba(OH)2溶液中滴加NH4HSO4溶液至刚好沉淀完全:
Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3·H2O+ H2O
(4)过量氯气通入溴化亚铁溶液中3C12 +2Fe2++4Br一=6C1一+2Fe3++2Br2
(5)H218O中投入Na2O2固体:2H218O+2O22-=4OH-+18O2
(6)NH4HCO3溶液中加足量NaAlO2溶液:NH4++AlO2-+2H2O= NH3·H2O+ Al(OH)3↓
(7)0.1mol/L CuCl2溶液中加入0.1mol/L NaHS溶液:Cu2++2HS-+2H2O=Cu(OH)2↓+2H2S
(8)等物质的量的KHCO3和Ba(OH)2的溶液混合:HCO3-+Ba2++OH-= BaCO3↓+H2O
(9)向明矾溶液中逐滴加入Ba(OH)2溶液至Al3+刚好沉淀完全:
Al3+ +SO42—+Ba2+ +3OH—==BaSO4↓+Al(OH)3↓
(10)NaHCO3溶液水解:HCO3-+ H2O  CO32-+ H3O+
CO32-+ H3O+
(11)硫化钠水溶液呈碱性的原因:S2-+2H2O  H2S↑+2OH-
H2S↑+2OH-
(12)在碳酸氢镁溶液中加入足量Ca(OH)2溶液:
Mg2++HCO3-+Ca2++2OH–="=" MgCO3↓+CaCO3↓+2H2O
(13)用石墨作电极电解AlCl3溶液:2Cl-+2H2O  Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
(14)向饱和碳酸钠溶液通入过量的二氧化碳气体:CO32-+CO2+H2O=2HCO3-
(1)氢氧化亚铁溶于稀硝酸中:Fe(OH)2 + 2H+ = Fe2+ + 2H2O
(2)过量的NaHSO4与Ba(OH)2溶液反应: Ba2++2OH-+2H++SO42-= BaSO4↓+2H2O
(3)向Ba(OH)2溶液中滴加NH4HSO4溶液至刚好沉淀完全:
Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3·H2O+ H2O
(4)过量氯气通入溴化亚铁溶液中3C12 +2Fe2++4Br一=6C1一+2Fe3++2Br2
(5)H218O中投入Na2O2固体:2H218O+2O22-=4OH-+18O2
(6)NH4HCO3溶液中加足量NaAlO2溶液:NH4++AlO2-+2H2O= NH3·H2O+ Al(OH)3↓
(7)0.1mol/L CuCl2溶液中加入0.1mol/L NaHS溶液:Cu2++2HS-+2H2O=Cu(OH)2↓+2H2S
(8)等物质的量的KHCO3和Ba(OH)2的溶液混合:HCO3-+Ba2++OH-= BaCO3↓+H2O
(9)向明矾溶液中逐滴加入Ba(OH)2溶液至Al3+刚好沉淀完全:
Al3+ +SO42—+Ba2+ +3OH—==BaSO4↓+Al(OH)3↓
(10)NaHCO3溶液水解:HCO3-+ H2O
 CO32-+ H3O+
CO32-+ H3O+(11)硫化钠水溶液呈碱性的原因:S2-+2H2O
 H2S↑+2OH-
H2S↑+2OH-(12)在碳酸氢镁溶液中加入足量Ca(OH)2溶液:
Mg2++HCO3-+Ca2++2OH–="=" MgCO3↓+CaCO3↓+2H2O
(13)用石墨作电极电解AlCl3溶液:2Cl-+2H2O
 Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-(14)向饱和碳酸钠溶液通入过量的二氧化碳气体:CO32-+CO2+H2O=2HCO3-
副题下列离子方程式中正确的是 ______________
(1)氢氧化亚铁溶于稀硝酸中:Fe(OH)2 + 2H+ = Fe2+ + 2H2O
(2)过量的NaHSO4与Ba(OH)2溶液反应: Ba2++2OH-+2H++SO42-= BaSO4↓+2H2O
(3)向Ba(OH)2溶液中滴加NH4HSO4溶液至刚好沉淀完全:
Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3·H2O+ H2O
(4)过量氯气通入溴化亚铁溶液中3C12 +2Fe2++4Br一=6C1一+2Fe3++2Br2
(5)H218O中投入Na2O2固体:2H218O+2O22-=4OH-+18O2
(6)NH4HCO3溶液中加足量NaAlO2溶液:NH4++AlO2-+2H2O= NH3·H2O+ Al(OH)3↓
(7)0.1mol/L CuCl2溶液中加入0.1mol/L NaHS溶液:Cu2++2HS-+2H2O=Cu(OH)2↓+2H2S
(8)等物质的量的KHCO3和Ba(OH)2的溶液混合:HCO3-+Ba2++OH- = BaCO3↓+H2O
(9)向明矾溶液中逐滴加入Ba(OH)2溶液至Al3+刚好沉淀完全:
Al3+ +SO42—+Ba2+ +3OH—==BaSO4↓+Al(OH)3↓
(10)NaHCO3溶液水解:HCO3-+ H2O ![]() CO32-+ H3O+
CO32-+ H3O+
(11)硫化钠水溶液呈碱性的原因:S2-+2H2O ![]() H2S↑+2OH-
H2S↑+2OH-
(12)在碳酸氢镁溶液中加入足量Ca(OH)2溶液:
Mg2++HCO3-+Ca2++2OH–== MgCO3↓+CaCO3↓+2H2O
(13)用石墨作电极电解AlCl3溶液:2Cl-+2H2O ![]() Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
(14)向饱和碳酸钠溶液通入过量的二氧化碳气体:CO32-+CO2+H2O=2HCO3-
查看习题详情和答案>>|
1 |
|
2 |
|||||
|
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
从核外电子层数和最外层电子数分析:
(1)核电荷数为6和14的一组原子,它们的______相同,_____不同;而核电荷数为15和16的一组原子,它们的______相同,_______不同。
(2)表中核电荷数为12的元素能分别与核电荷数为______的元素形成AB型化合物,而核电荷数为13的元素与核电荷数为8的元素形成化合物的化学式是_______。
(3)上表中核电荷数为_______元素,其氢氧化物的碱性最强;核电荷数为______的元素,其最高正价氧化物的水化物酸性最强。它们的化学式分别是_______和________。
(4)某元素的原子核外有三个电子层,最外层电子数是核外电子总数的1/6,该元素的元素符号是______,原子结构示意图是________,阳离子结构示意图是________。
(5)在第三周期元素中,置换氢能力最强的元素符号是________。形成的单质氧化性最强的元素是_______。在第二周期中化学性质最稳定的单质是_______。第13号元素的氢氧化物具有________性,能说明这一性质的离子方程式为_________。
查看习题详情和答案>>