摘要:21.某人买了两瓶消毒液.不小心将两种液体混在一起.结果产生大量氯气而中毒.经测定: (a)用pH试纸测量:甲瓶中消毒液pH=12.乙瓶中消毒液pH=2.且都能很快使pH试纸白. (b)向乙中加入MnO2粉末.产生大量氧气.并闻到一股醋酸气味. (c)向甲中加入硝酸酸化的AgNO3溶液.向乙中加入盐酸酸化的BaCl2溶液.均有白色沉淀产生. (1)甲瓶中的消毒剂一定含有的阴离子是 和 .乙瓶中的消毒剂的合成反应在一定条件下是可逆反应.此反应方程式为 . (2)甲液与乙液混合时.产生氯气的离子方程式为 甲液与乙液混合时还产生了氧气.生成氧气的离子方程式为 .
网址:http://m.1010jiajiao.com/timu3_id_434800[举报]
某同学将两瓶消毒液混合使用时,结果产生了氯气。该同学为进一步确定两种消毒液的成分,进行了如下实验探究:
(a)用pH试纸测量:甲瓶中消毒液pH=12,乙瓶中消毒液pH=2,且都能很快使pH试纸褪色。
(b)取少量乙瓶中的溶液,向其中加入MnO2粉末,产生大量氧气,并闻到一股醋酸气味。
(c)取少量甲瓶中的溶液,向其中加入硝酸酸化的AgNO3溶液;取少量乙瓶中的溶液,向其中加入盐酸酸化的BaCl2溶液,均有白色沉淀产生。
根据以上实验现象,回答下列问题:
(1)甲瓶中的消毒剂一定含有的阴离子是OH-和_________、_________,乙瓶中的消毒剂一定含有H+、OH-(少量)、![]() (少量)、CH3COO-、_________离子和H2O、CH3COOH、________________分子。
(少量)、CH3COO-、_________离子和H2O、CH3COOH、________________分子。
(2)将甲瓶和乙瓶溶液混合时还产生了氧气,试写出该反应的离子方程式:___________________________________________________________________。
查看习题详情和答案>>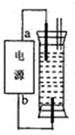 (2009?江门一模)某研究性学习小组设计了一个环保型消毒液发生器,如图所示装置,用一石墨作电极电解饱和NaCl溶液,请你完成以下实验探究过程:
(2009?江门一模)某研究性学习小组设计了一个环保型消毒液发生器,如图所示装置,用一石墨作电极电解饱和NaCl溶液,请你完成以下实验探究过程:已知25℃H2CO3K1=4.4×10-7、K2=4.7×10-11、HClO K=2.9×10-8
(1)推断电源电极名称:a为
负
负
极,电解过程中,与电源正极相连的电极反应式为2Cl--2e-=Cl2↑
2Cl--2e-=Cl2↑
.与电源负极相连的电极附近溶液pH升高
升高
.(填“不变,“升高”或“降低”)(2)产生消毒液过程的有关反应化学方程式:
2NaCl+2H2O
2NaOH+H2↑+Cl2↑,2NaOH+Cl2=NaCl+NaClO+H2O
| ||
2NaCl+2H2O
2NaOH+H2↑+Cl2↑,2NaOH+Cl2=NaCl+NaClO+H2O
.
| ||
(3)若要保存消毒液必须密封,原因是(用化学方程式表示)
NaClO+H2O+CO2=NaHCO3+HClO
NaClO+H2O+CO2=NaHCO3+HClO
.(4)有人认为该消毒液和“洁厕液”(含盐酸)混合使用能增强清洁效果,你认为可行吗?
为什么?
不行,因为二者混合后2HCl+NaClO=Cl2↑+NaCl+H2O
不行,因为二者混合后2HCl+NaClO=Cl2↑+NaCl+H2O
(5)对该消毒液对碳钢制品是否有腐蚀作用进行探究.
仅限选择的仪器和试剂:烧杯、试管、玻璃棒、量筒、容量瓶、滴管、药匙;光亮的铁钉、
消毒液、酚酞试液、2mol/L盐酸、lmol/L硫酸、2mol/L硝酸、20%KSCN溶液.
| 假设 | 实验操作 | 预期现象 | 结论 |
| ①有明显现象 | 用烧杯取少量消毒液,将一颗光亮的铁钉放入烧杯,浸泡一段时间 用烧杯取少量消毒液,将一颗光亮的铁钉放入烧杯,浸泡一段时间 |
铁定表面出现铁锈 铁定表面出现铁锈 |
铁定被锈蚀 铁定被锈蚀 |
| ②无明显现象,要进一步探究 | 用试管取少量(实验①)浸泡后的溶液,滴加足量的1mol/L的硫酸酸化,再用滴管滴加几滴20%的KSCN溶液 用试管取少量(实验①)浸泡后的溶液,滴加足量的1mol/L的硫酸酸化,再用滴管滴加几滴20%的KSCN溶液 |
溶液不变色或溶液显血红色 溶液不变色或溶液显血红色 |
铁钉可能未被腐蚀也可能被腐蚀 铁钉可能未被腐蚀也可能被腐蚀 |
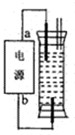
某研究性学习小组设计了一个环保型消毒液发生器,如图所示装置,用一石墨作电极电解饱和NaCl溶液,请你完成以下实验探究过程:
已知25℃H2CO3K1=4.4×10-7、K2=4.7×10-11、HClO K=2.9×10-8
(1)推断电源电极名称:a为______极,电解过程中,与电源正极相连的电极反应式为______.与电源负极相连的电极附近溶液pH______.(填“不变,“升高”或“降低”)
(2)产生消毒液过程的有关反应化学方程式:______.
(3)若要保存消毒液必须密封,原因是(用化学方程式表示)______.
(4)有人认为该消毒液和“洁厕液”(含盐酸)混合使用能增强清洁效果,你认为可行吗?
为什么?______
(5)对该消毒液对碳钢制品是否有腐蚀作用进行探究.
仅限选择的仪器和试剂:烧杯、试管、玻璃棒、量筒、容量瓶、滴管、药匙;光亮的铁钉、
消毒液、酚酞试液、2mol/L盐酸、lmol/L硫酸、2mol/L硝酸、20%KSCN溶液.
查看习题详情和答案>>
已知25℃H2CO3K1=4.4×10-7、K2=4.7×10-11、HClO K=2.9×10-8
(1)推断电源电极名称:a为______极,电解过程中,与电源正极相连的电极反应式为______.与电源负极相连的电极附近溶液pH______.(填“不变,“升高”或“降低”)
(2)产生消毒液过程的有关反应化学方程式:______.
(3)若要保存消毒液必须密封,原因是(用化学方程式表示)______.
(4)有人认为该消毒液和“洁厕液”(含盐酸)混合使用能增强清洁效果,你认为可行吗?
为什么?______
(5)对该消毒液对碳钢制品是否有腐蚀作用进行探究.
仅限选择的仪器和试剂:烧杯、试管、玻璃棒、量筒、容量瓶、滴管、药匙;光亮的铁钉、
消毒液、酚酞试液、2mol/L盐酸、lmol/L硫酸、2mol/L硝酸、20%KSCN溶液.
| 假设 | 实验操作 | 预期现象 | 结论 |
| ①有明显现象 | ______ | ______ | ______ |
| ②无明显现象,要进一步探究 | ______ | ______ | ______ |

 ,pH大的是 。
,pH大的是 。