网址:http://m.1010jiajiao.com/timu3_id_434586[举报]
| ||
| <95.4°C |
若NA为阿伏加德罗常数,则下列说法中,不正确的是?( )
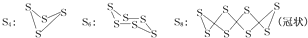
(1)在一定温度下,测得硫蒸气的平均摩尔质量为72g/mol,则该蒸气中S2分子的体积分数不小于
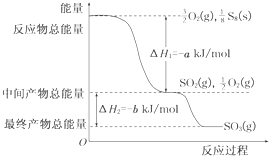
(2)在一定条件下,S8(s)和O2(g)发生反应依次转化为SO2(g)和SO3(g).反应过程和能量关系可用如图简单表示(图中的△H表示生成1mol产物的数据).
①写出表示S8燃烧热
| 1 |
| 2 |
| 1 |
| 2 |
③若已知硫氧键(S=O)的键能为d kJ/mol,氧氧键(O=O)的键能为e kJ/mol,则S8分子中硫硫键(S-S)的键能为
已知单质硫在通常条件下以S8(斜方硫)的形式存在,而在蒸气状态时,含有S2、S4、S6及S8等多种同素异形体,其中S4、S6和S8具有相似的结构特点,其结构如下图所示:

在一定条件下,S8(s)和O2(g)发生反应依次转化为SO2(g)和SO3(g)。反应过程和能量关系可用下图简单表示(图中的ΔH表示生成1 mol含硫产物的数据)。

(1)写出表示S8燃烧热的热化学方程式_____________________。
(2)写出SO3分解生成SO2和O2的热化学方程式_________________________。
(3)若已知SO2中硫氧键的键能为d kJ·mol-1,O2中氧氧键的键能为e kJ·mol-1,则S8分子中硫硫键的键能为___________。
查看习题详情和答案>>
S8分子形成的单斜硫和斜方硫是同素异形体,转化关系如下:
S(斜方,固) S(单斜,固)△H=+0.398kJ·mol-1若NA为阿伏加德罗常数,则下列说法中,错误的是(
)
S(单斜,固)△H=+0.398kJ·mol-1若NA为阿伏加德罗常数,则下列说法中,错误的是(
)
A.常温下斜方硫比单斜硫稳定
B.单斜硫和斜方硫之间的转化属于物理变化
C.单斜硫和斜方硫在充足的氧气中燃烧均生成SO2 ?
D.64 g 单斜硫和斜方硫的混合物含硫原子数目为2NA
查看习题详情和答案>>
已知单质硫在通常条件下以S8(斜方硫)的形式存在,而在蒸气状态时,含有S2、S4、S6及S8等多种同素异形体,其中S4、S6和S8具有相似的结构特点,其结构如下图所示:
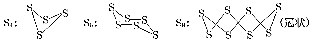
在一定条件下,S8(s)和O2(g)发生反应依次转化为SO2(g)和SO3(g)。反应过程和能量关系可用下图简单表示(图中的ΔH表示生成1 mol产物的数据)。
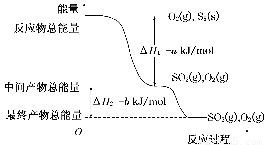
(1)写出表示S8燃烧热的热化学方程式___________________________________。
(2)写出SO3分解生成SO2和O2的热化学方程式_______________________________________________________________。
(3)化学上规定,拆开或形成1 mol化学键吸收或放出的能量称为该化学键的键能,单位kJ·mol。若已知硫氧键的键能为d kJ·mol-1,氧氧键的键能为e kJ·mol-1,则S8分子中硫硫键的键能为____________________________________。
查看习题详情和答案>>