网址:http://m.1010jiajiao.com/timu3_id_434076[举报]
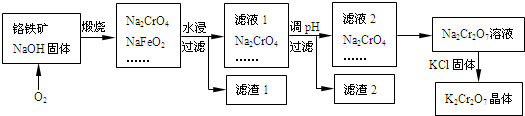
已知:①NaFeO2遇水强烈水解.②Cr2O72-+H2O
 2CrO42-+2H+
2CrO42-+2H+请回答:
(1)K2Cr2O7中Cr元素的化合价是
(2)生成滤渣1中红褐色物质的反应的化学方程式是
(3)利用滤渣2,可制得两种氧化物,其中一种氧化物经电解冶炼可获得金属,该电解反应的化学方程式是
| ||
| ||
(4)由滤液2转化为Na2Cr2O7溶液应采取的措施是
(5)向Na2Cr2O7溶液中加入KCl固体,获得K2Cr2O7晶体的操作依次是:加热浓缩、
(6)煅烧铬铁矿生成Na2CrO4和NaFeO2反应的化学方程式是
| ||
| ||
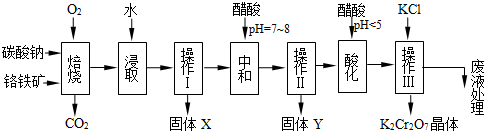
已知:
①4FeO?Cr2O3+8Na2CO3+7O2
| 750℃ |
②Na2CO3+Al2O3
| 750℃ |
③Cr2O72-+H2O?2CrO42-+2H+
根据题意回答下列问题:
(1)固体X中主要含有
(2)酸化步骤用醋酸调节溶液pH<5,其目的是
物质溶解度/(g/100g水)0°C40°C80°CKCl2840.151.3NaCl35.736.438K2Cr2O74.726.373Na2Cr2O7163215376
(3)操作Ⅲ有多步组成,获得K2Cr2O7晶体的操作依次是:加入KCl固体、蒸发浓缩、
(4)表格是相关物质的溶解度数据,操作Ⅲ发生反应的化学方程式是:Na2Cr2O7+2KCl→K2Cr2O7↓+2NaCl.
该反应在溶液中能发生的理由是
| 物质 | 溶解度/(g/100g水) | ||
| 0°C | 40°C | 80°C | |
| KCl | 28 | 40.1 | 51.3 |
| NaCl | 35.7 | 36.4 | 38 |
| K2Cr2O7 | 4.7 | 26.3 | 73 |
| Na2Cr2O7 | 163 | 215 | 376 |
| 26m |
| 17n |
| 26m |
| 17n |
(6)六价铬有毒,而Cr3+相对安全.工业含铬(CrO3)废渣无害化处理的方法之一是干法解毒,用煤不完全燃烧生成的CO还原CrO3.在实验室中模拟这一过程的装置如下:
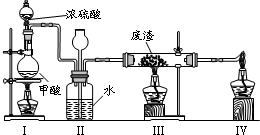
CO由甲酸脱水制得;实验结束时熄灭酒精灯的顺序是
铬铁矿的主要成分可表示为FeO·Cr2O3,还含有MgO、Al2O3、Fe2O3等杂质,以下是以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的流程图:
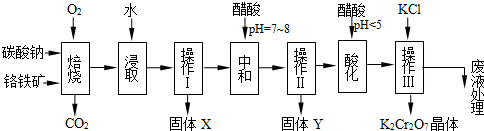
已知:①4FeO·Cr2O3+ 8Na2CO3+
7O2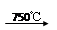 8Na2CrO4
+ 2 Fe2O3 + 8CO2↑;
8Na2CrO4
+ 2 Fe2O3 + 8CO2↑;
②Na2CO3
+ Al2O3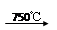 2NaAlO2
+ CO2↑;③ Cr2O72-+ H2O
2NaAlO2
+ CO2↑;③ Cr2O72-+ H2O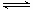 2CrO42- +
2H+
2CrO42- +
2H+
(1)固体X中主要含有_________(填写化学式);要检测酸化操作中溶液的pH是否等于4.5,应该使用__________(填写仪器或试剂名称)。
(2)酸化步骤用醋酸调节溶液pH<5,其目的是_________________________________。
|
物质 |
溶解度/(g/100g水) |
||
|
0°C |
40°C |
80°C |
|
|
KCl |
28 |
40.1 |
51.3 |
|
NaCl |
35.7 |
36.4 |
38 |
|
K2Cr2O7 |
4.7 |
26.3 |
73 |
|
Na2Cr2O7 |
163 |
215 |
376 |
(3)操作Ⅲ有多步组成,获得K2Cr2O7晶体的操作依次是:加入KCl固体、蒸发浓缩、 、
过滤、_______、干燥。
(4)右表是相关物质的溶解度数据,操作Ⅲ发生反应的化学方程式是:Na2Cr2O7+2KCl→K2Cr2O7↓+2NaCl。该反应在溶液中能发生的理由是_______________。
(5)酸性溶液中过氧化氢能使Cr2O72-生成蓝色的过氧化铬(CrO5分子结构为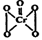 ),
该反应可用来检验Cr2O72-的存在。写出反应的离子方程式:
。
),
该反应可用来检验Cr2O72-的存在。写出反应的离子方程式:
。
该反应 (填“属于”或“不属于”)氧化还原反应。
(6)称取重铬酸钾试样2.500g配成250mL溶液,取出25mL与碘量瓶中,加入10mL2mol/ L H2SO4和足量碘化钾(铬的还原产物为Cr3+),放于暗处5min。然后加入100mL水,加入3mL淀粉指示剂,用0.1200mol/LNa2S2O3标准溶液滴定(I2+2S2O32—=2I-+S4O62—)。
①判断达到滴定终点的依据是 ;
②若实验中共用去Na2S2O3标准溶液40.00mL,则所得产品中重铬酸钾的纯度为 。(保留3位有效数字, K2Cr2O7的摩尔质量为294g/mol)。
查看习题详情和答案>>
铬铁矿的主要成分可表示为FeO·Cr2O3,还含有MgO、Al2O3、Fe2O3等杂质,以下是以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的流程图:

已知:①4FeO·Cr2O3+ 8Na2CO3+
7O2 8Na2CrO4
+ 2 Fe2O3 + 8CO2↑;
8Na2CrO4
+ 2 Fe2O3 + 8CO2↑;
②Na2CO3
+ Al2O3 2NaAlO2
+ CO2↑;③ Cr2O72-+ H2O
2NaAlO2
+ CO2↑;③ Cr2O72-+ H2O
 2CrO42- +
2H+
2CrO42- +
2H+
根据题意回答下列问题:
(1)固体X中主要含有_________(填写化学式);要检测酸化操作中溶液的pH是否等于4.5,应该使用__________(填写仪器或试剂名称)。
(2)酸化步骤用醋酸调节溶液pH<5,其目的是_________________________________。
(3)操作Ⅲ有多步组成,获得K2Cr2O7晶体的操作依次是:加入KCl固体、蒸发浓缩、 、过滤、_______、干燥。
(4)下表是相关物质的溶解度数据,操作Ⅲ发生反应的化学方程式是:Na2Cr2O7+2KCl → K2Cr2O7↓+2NaCl。
|
物质 |
溶解度/(g/100g水) |
||
|
0°C |
40°C |
80°C |
|
|
KCl |
28 |
40.1 |
51.3 |
|
NaCl |
35.7 |
36.4 |
38 |
|
K2Cr2O7 |
4.7 |
26.3 |
73 |
|
Na2Cr2O7 |
163 |
215 |
376 |
该反应在溶液中能发生的理由是_______________。
(5)副产品Y主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,精确分析Y中氢氧化铝含量的方法是称取n g样品,加入过量______(填写试剂)、溶解、过滤、再______(填写试剂)、灼烧、冷却、称量,得干燥固体m g 。计算样品中氢氧化铝的质量分数为_________(用含m、n的代数式表示)。
查看习题详情和答案>>
铬铁矿的主要成分可表示为FeO·Cr2O3,还含有SiO2、Al2O3等杂质,以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的过程如下图所示。
已知:① NaFeO2遇水强烈水解。 ② Cr2O72-+ H2O 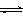 2CrO42- + 2H+
2CrO42- + 2H+ K2Cr2O7中Cr元素的化合价是 。
K2Cr2O7中Cr元素的化合价是 。
生成滤渣1中红褐色物质反应的化学方程式是 。
滤液1的成分除Na2CrO4、Na2SiO3外,还含有(填化学式) 。
利用滤渣2,可制得两种氧化物,其中一种氧化物经电解冶炼可获得金属,该电解反应的化学方程式是 。
由滤液2转化为Na2Cr2O7溶液应采取的措施是 。
向Na2Cr2O7溶液中加入KCl固体,获得K2Cr2O7晶体的操作依次是:加热浓缩、 、过滤、洗涤、干燥。
煅烧铬铁矿生成Na2CrO4和NaFeO2反应的化学方程式是 。