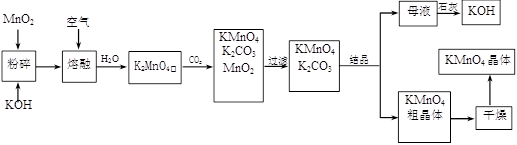网址:http://m.1010jiajiao.com/timu3_id_433222[举报]

(1)KMnO4稀溶液是一种常用的消毒剂,其消毒原理与下列物质相同的是
a.84消毒液(NaClO溶液) b.双氧水 c.福尔马林(35%甲醛溶液) d.75%酒精
(2)高锰酸钾保存在棕色试剂瓶中,下列试剂保存不需要棕色试剂瓶的是
a.浓硝酸 b.硝酸银 c.氯水 d.烧碱
(3)上述流程中可以循环使用的物质有
(4)若不考虑物质循环与制备过程中的损失,则1mol MnO2可制得
| 2 |
| 3 |
| 2 |
| 3 |
(5)写出实验室用KMnO4制备气体的一个化学方程式
| ||
| ||
(6)操作Ⅰ的名称是
高锰酸钾是锰的重要化合物和常用的氧化剂。以下是工业上用软锰矿制备高锰酸钾的一种工艺流程。
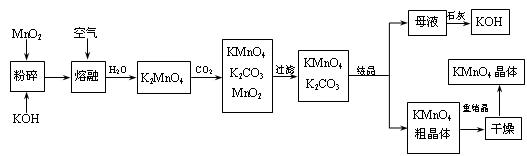
(1)KMnO4稀溶液是一种常用的消毒剂。其消毒机理与下列 (填序号)物质相似。
A.75%酒精 B.双氧水 C.苯酚 D.84消毒液(NaClO溶液)
(2)写出MnO2、KOH的熔融混合物中通入空气时发生的主要反应的化学方程式:
。
(3)向K2MnO4溶液中通入CO2以制备KMnO4,该反应中的还原剂是: 。
(4)上述流程中可以循环使用的物质有石灰、二氧化碳、 和 (写化学式)。
(5)若不考虑物质循环与制备过程中的损失,则1 mol MnO2可制得 mol KMnO4。
查看习题详情和答案>>(18分)高锰酸钾是锰的重要化合物和常用的氧化剂。以下是工业上用软锰矿(主要成份MnO2)制备高锰酸钾的流程图。
(1)软锰矿粉碎的目的 。
软锰矿、KOH混合物在空气加热熔融反应生成K2MnO4的化学方程式为:
。操作Ⅲ的名称为 。
(2)反应②的化学方程式为 。
以上生产流程中可循环利用的物质是Ca(OH)2、CO2、 、 。
工业上用上述原理生产KMnO4方法产率较低,较好的制备方法是电解法。用Pt作阳极,Fe作阴极,电解K2MnO4溶液,阳极的电极反应式为 。
(3)KMnO4是一种较稳定的化合物,但日光对KMnO4溶液的分解有催化作用,生成MnO2、KOH和O2。而 MnO2也是该分解反应的一种催化剂,请你设计一个实验方案,验证MnO2对该分解反应具有催化性。简述实验操作、现象及相关结论:
。
查看习题详情和答案>>