摘要:25.H+.Al3+.NH4+ K+ ClO- .AlO2- (2)①Cl2+2I-=I2+2Cl-
网址:http://m.1010jiajiao.com/timu3_id_432851[举报]
(2012?长春一模)1L某混合溶液,可能含有的离子如表:
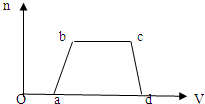
(1)往该溶液中逐滴加入NaOH溶液,产生沉淀的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示.则该溶液中
确定含有的离子是
(2)经检测,该溶液中还含有大量的Cl-、Br-、I-,若向1L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通入Cl2的体积(标准状况)的关系如表所示,分析后回答下列问题:
①当通入Cl2的体积为2.8L时,溶液中发生反应的离子方程式为
②原溶液中Cl-、Br-、I-的物质的量浓度之比为
查看习题详情和答案>>
| 可能大量含有的阳离子 | H+、K+、Mg2+、Al3+、NH4+、Fe2+、Fe3+ |
| 可能大量含有的阴离子 | Cl-、Br-、I-、CO32-、AlO2- |
确定含有的离子是
H+、Al3+、NH4+
H+、Al3+、NH4+
,一定不含有的阳离子是Mg2+、Fe2+、Fe3+
Mg2+、Fe2+、Fe3+
,一定不存在的阴离子是CO32-、AlO2-
CO32-、AlO2-
,b→c 的离子方程式为NH4++OH-=NH3?H2O
NH4++OH-=NH3?H2O
.
(2)经检测,该溶液中还含有大量的Cl-、Br-、I-,若向1L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通入Cl2的体积(标准状况)的关系如表所示,分析后回答下列问题:
| Cl2的体积(标准状况) | 2.8L | 5.6L | 11.2L |
| n(Cl-) | 1.25mol | 1.5mol | 2mol |
| n(Br-) | 1.5mol | 1.4mol | 0.9mol |
| n(I-) | a mol | 0 | 0 |
Cl2+2I-=2Cl-+I2
Cl2+2I-=2Cl-+I2
.②原溶液中Cl-、Br-、I-的物质的量浓度之比为
10:15:4
10:15:4
.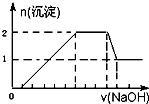 某无色溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-等离子中的几种,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示.下列说法一定正确的是( )
某无色溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-等离子中的几种,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示.下列说法一定正确的是( )| A、一定存在H+、Mg2+、Al3+、NH4+,一定不存在Na+、SO42-、Fe3+ | B、一定存在H+、Al3+、NH4+、SO42-,可能存在Na+、Mg2+ | C、溶液中c(H+):c(Al3+):c(Mg2+)为1:1:1 | D、溶液中c(H+):c(SO42-)为2:9 |