摘要:9.二氧化氮(NO2)是重要的空气污染物.科学家正寻求合适的化合物G与适当的条件以进行如下反应.从而将二氧化氮转化为无毒的N2: NO2+G--N2+H2O+nY 上式中的n为系数.但也可以为0.而Y必须为任何无害的物质.从反应机理分析.上述反应式中的G肯定不可以是 ( ) A.NH3 B.CO C.CH3CH2OH D.H2O2
网址:http://m.1010jiajiao.com/timu3_id_432399[举报]
二氧化氮(NO2)是重要的空气污染物,科学家正寻求合适的 化合物G与适当的条件以进行如下反应,从而将二氧化氮转化为无毒的N2:NO2 + G→N2 +H2O +nY(反应未配平)。上式中的n为系数,但也可以为O,而Y必须为任何无害的物质。从反应机理分析,上述反应式中的G肯定不可以是
[ ]
A.NH3
B.CO
C.CH3CH2OH
D.H2O2
查看习题详情和答案>>
B.CO
C.CH3CH2OH
D.H2O2
 二氧化硫和氮氧化物是常用的化工原料,也会给大气带来严重污染,综合治理其污染是环境化学当前的重要研究内容之一.
二氧化硫和氮氧化物是常用的化工原料,也会给大气带来严重污染,综合治理其污染是环境化学当前的重要研究内容之一.(1)汽车尾气中主要含有CO、NO2、SO2、CO2气体,其中
NO2、SO2
NO2、SO2
能导致酸雨的形成;目前采用的是在汽车排气装置中安装一个净化器,可以有效的将尾气中的有害气体转化.如:CO(g)+NO2(g)═NO(g)+CO2(g)△H=-akJ?mol-1(a>0)
2CO(g)+2NO(g)═N2(g)+2CO2(g)△H=-bkJ?mol-1(b>0)
据此回答:若用标准状况下3.36升CO还原NO2至N2(CO完全反应)的整个过程中转移电子的物质的量为
0.3
0.3
mol,放出的热量为| 3(2a+b) |
| 80 |
| 3(2a+b) |
| 80 |
(2)在火力发电厂产生的废气中含有SO2、N2、CO等气体,为除去SO2,常用Ca(OH)2悬浊液洗涤废气,为了废物利用,再通入空气使反应产物转化为石膏(CaSO4?2H2O).写出有关的化学反应方程式
SO2+Ca(OH)2=CaSO3↓+H2O、2CaSO3+O2+4H2O=2CaSO4?2H2O
SO2+Ca(OH)2=CaSO3↓+H2O、2CaSO3+O2+4H2O=2CaSO4?2H2O
.(3)硫酸工业生产中,SO2催化氧化生成SO3:
2SO2(g)+O2(g)
| 催化剂 |
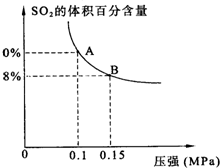
某温度下达到平衡时,SO2的体积百分含量与体系的总压强的关系如图所示:
据此图回答下列问题:
①平衡状态由A变到B时,反应体系
释放
释放
(填“吸收”或“释放”)能量.②将5molSO2和7molO2通入10L密闭容器中,平衡时体系的总压强为0.1MPa.该反应在该温度下的平衡常数等于
32
32
.
二氧化硫和氮氧化物是常用的化工原料,也会给大气带来严重污染,综合治理其污染是环境化学当前的重要研究内容之一。
(1)汽车尾气中主要含有CO、NO2、SO2、CO2气体,其中________________能导致酸雨的形成;目前采用的是在汽车排气装置中安装一个净化器,可以有效的将尾气中的有害气体转化。
如:CO(g)+NO2(g)![]() NO(g)+CO2(g) ΔH=-a kJ·mol-1(a>0)
NO(g)+CO2(g) ΔH=-a kJ·mol-1(a>0)
2CO(g)+2NO(g)![]() N2(g)+2CO2(g) ΔH=-b kJ·mol-1(b>0)
N2(g)+2CO2(g) ΔH=-b kJ·mol-1(b>0)
据此回答:若用标准状况下
(2)在火力发电厂产生的废气中含有SO2、N2、CO等气体,为除去SO2,常用Ca(OH)2悬浊液洗涤废气,为了废物利用,再通入空气使反应产物转化为石膏(CaSO4·2H2O)。写出有关的化学反应方程式______________。
(3)硫酸工业生产中,SO2催化氧化生成SO3:
2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-196 kJ·mol-1
2SO3(g) ΔH=-196 kJ·mol-1

某温度下达到平衡时,SO2的体积百分含量与体系的总压强的关系如上图所示:
据此图回答下列问题:
①平衡状态由A变到B时,反应体系____________(填“吸收”或“释放”)能量。
②将5 mol SO2和7 mol O2通入