摘要:21.下列说法正确的是 A.25℃时.pH=3的盐酸溶液比pH=3的醋酸溶由水电离出的氢离子浓度前者更大 B.利用右图装置.可以用Cu和稀硝酸反应来制取干燥的NO C.往0.1mol/L氢氟酸溶加水稀释时.平衡向右移动.溶液中所 有离子浓度均减小 D.以8% KOH溶液为电解液时.甲烷燃料电池中OH-往负极移动 负极的电极反应式为:CH4+10OH-→CO32-+7H2O+8e-
网址:http://m.1010jiajiao.com/timu3_id_431927[举报]
下列说法正确的是
A.25℃时,NH4Cl溶液的KW大于100℃时NH4Cl溶液的KW
B.25℃时,向10mL pH=3的醋酸溶液中加入水稀释后,溶液中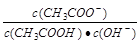 不变
不变
C.25℃时,pH=12的氨水和pH=2的盐酸溶液等体积混合,c(Cl-)>c(NH4+)>c(H+)>c(OH-)
D.100℃时,将pH=2的盐酸与pH=12的NaOH溶液等体积混合,溶液显中性
查看习题详情和答案>>
下列说法正确的是
| A.25℃时,NH4Cl溶液的KW大于100℃时NH4Cl溶液的KW |
B.25℃时,向10mL pH=3的醋酸溶液中加入水稀释后,溶液中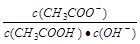 不变 不变 |
| C.25℃时,pH=12的氨水和pH=2的盐酸溶液等体积混合,c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| D.100℃时,将pH=2的盐酸与pH=12的NaOH溶液等体积混合,溶液显中性 |
下列说法正确的是
A.25℃时,NH4Cl溶液的KW大于100℃时NH4Cl溶液的KW
B.25℃时,向10mL pH=3的醋酸溶液中加入水稀释后,溶液中![]() 不变
不变
C.25℃时,pH=12的氨水和pH=2的盐酸溶液等体积混合,c(Cl-)>c(NH4+)>c(H+)>c(OH-)
D.100℃时,将pH=2的盐酸与pH=12的NaOH溶液等体积混合,溶液显中性
查看习题详情和答案>>
下列说法正确的是
| A.25℃时,NH4Cl溶液的KW大于100℃时NH4Cl溶液的KW |
B.25℃时,向10mL pH=3的醋酸溶液中加入水稀释后,溶液中 不变 不变 |
| C.25℃时,pH=12的氨水和pH=2的盐酸溶液等体积混合,c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| D.100℃时,将pH=2的盐酸与pH=12的NaOH溶液等体积混合,溶液显中性 |
下列说法正确的是
| A.KClO3和SO3溶于水后均能导电,故KClO3和SO3都是电解质 |
| B.常温下将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低 |
| C.常温下,等浓度的Na2S与NaHS溶液相比,Na2S溶液的pH大 |
| D.25℃时,用pH=3的盐酸滴定等浓度的氨水至溶液的pH=7,V(氨水)<V(盐酸) |