摘要: 3 .CaSO4 , Na+(填有Ca2+.或SO42- 不给分). 布氏漏斗 抽滤瓶或吸滤瓶 (2)3NaClO + CO(NH2)2 =3NaCl + CO2 ↑+ N2↑+ 2H2O 或 NaOH +3NaClO + CO(NH2)2 =3NaCl + NaHCO3+ N2↑+ 2H2O △ 将Fe2+ 氧化为Fe3+ .并形成Fe(OH)3 被除去. Cl = MgO + HCl↑ ②P(HCl)小.加热时Mg2+ 会发生水解 , 通入HCl .增大P(HCl).抑制Mg2+ 水解.
网址:http://m.1010jiajiao.com/timu3_id_431746[举报]
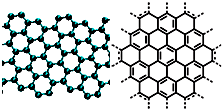 A.美国《科学》杂志评出的2009年十大科学突破之一是石墨烯的研究和应用方面的突破.石墨烯具有原子级的厚度、优异的电学性能、出色的化学稳定性和热力学稳定性.制备石墨烯方法有石墨剥离法、化学气相沉积法等.石墨烯的球棍模型及分子结构示意图如右:
A.美国《科学》杂志评出的2009年十大科学突破之一是石墨烯的研究和应用方面的突破.石墨烯具有原子级的厚度、优异的电学性能、出色的化学稳定性和热力学稳定性.制备石墨烯方法有石墨剥离法、化学气相沉积法等.石墨烯的球棍模型及分子结构示意图如右:(1)下列有关石墨烯说法正确的是
BD
BD
.A.石墨烯的结构与金刚石相似
B.石墨烯分子中所有原子可以处于同一平面
C.12g石墨烯含σ键数为NA
D.从石墨剥离得石墨烯需克服石墨层与层之间的分子间作用
(2)化学气相沉积法是获得大量石墨烯的有效方法之一,催化剂为金、铜、钴等金属或合金,含碳源可以是甲烷、乙炔、苯、乙醇或酞菁等中的一种或任意组合.
①钴原子在基态时,核外电子排布式为:
[Ar]3d74s2
[Ar]3d74s2
.
②乙醇沸点比氯乙烷高,主要原因是
乙醇分子间可形成氢键,而氯乙烷分子间无氢键
乙醇分子间可形成氢键,而氯乙烷分子间无氢键
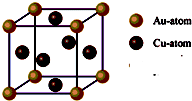
.③右图是金与铜形成的金属互化物合金,它的化学式可表示为:
Cu3Au或AuCu3
Cu3Au或AuCu3
.④含碳源中属于非极性分子的是
a、b、c
a、b、c
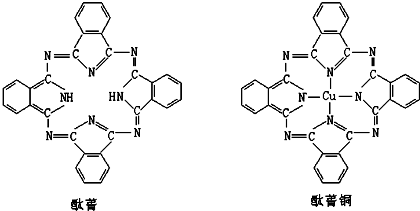
(a.甲烷 b.乙炔 c.苯 d.乙醇)⑤酞菁与酞菁铜染料分子结构如下图,酞菁分子中氮原子采用的杂化方式有:
sp3和sp2
sp3和sp2
;酞菁铜分子中心离子的配位数为:2
2
.
B.硫酸钾是重要的化工产品,生产方法很多,如曼海姆法、石膏两步转化法等.
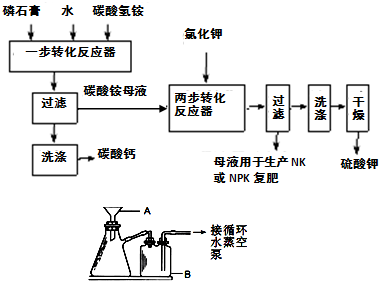
(1)本实验中,采用抽滤方法,图中A、B两仪器名称分别为:
布氏漏斗
布氏漏斗
、安全瓶
安全瓶
.(2)在一部转化反应器中发生的反应为:CaSO4?2H2O+2NH4HCO3=(NH4)2SO4+CaCO3+CO2↑+3H2O,该步反应温度必须低于35℃,其主要目的是
防止NH4HCO3分解
防止NH4HCO3分解
无此空
无此空
.(3)在两步转化反应器中发生反应的化学方程式为
(NH4)2SO4+2KCl=K2SO4+2NH4Cl
(NH4)2SO4+2KCl=K2SO4+2NH4Cl
无此空
无此空
.(4)两步转化反应器中用乙二醇代替水作溶剂,其目的是
降低K2SO4溶解度
降低K2SO4溶解度
有利于K2SO4析出,提高产率
有利于K2SO4析出,提高产率
.(5)磷石膏主要成分为二水硫酸钙(CaSO4?2H2O),还含有未分解的磷矿,未洗涤干净的磷酸、氟化钙、铁铝氧化物等,欲检验母液中含Fe3+,可用亚铁氰化钾溶液检验,该检验反应的离子方程式为:
Fe3++K++[Fe(CN)6]4-=KFe[Fe(CN)6]↓
Fe3++K++[Fe(CN)6]4-=KFe[Fe(CN)6]↓
.(6)该法优点除K2SO4产率高外,再列举一个优点
原料得到充分利用
原料得到充分利用
同时得到副产品化肥等
同时得到副产品化肥等
.某待测液中可能含有Fe2+、Fe3+、Ag+、Al3+、Ba2+、Ca2+、NH 4+

等离子,进行如下实验(所加酸、碱、氨水、溴水都是过量的).
根据实验结果:
(1)判定待测液中有无Ba2+、Ca2+离子,并写出理由.答:
(2)写出沉淀D的分子式:
(3)写出从溶液D生成沉淀E的反应的离子方程式:
查看习题详情和答案>>

等离子,进行如下实验(所加酸、碱、氨水、溴水都是过量的).
根据实验结果:
(1)判定待测液中有无Ba2+、Ca2+离子,并写出理由.答:
含有Ba2+、Ca2+离子中的一种或两种,因为BaSO4不溶于水,CaSO4微溶于水
含有Ba2+、Ca2+离子中的一种或两种,因为BaSO4不溶于水,CaSO4微溶于水
.(2)写出沉淀D的分子式:
Fe(OH)3
Fe(OH)3
.(3)写出从溶液D生成沉淀E的反应的离子方程式:
CO2+3H2O+2AlO2-═2Al(OH)3↓+2CO32-或CO2+2H2O+AlO2-═Al(OH)3↓+2HCO3-,
CO2+3H2O+2AlO2-═2Al(OH)3↓+2CO32-或CO2+2H2O+AlO2-═Al(OH)3↓+2HCO3-,
.硼镁泥是一种工业废料,主要成份是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业.从硼镁泥中提取MgSO4?7H2O的流程如下:

根据题意回答问题:
(1)实验中需用1mol/L的硫酸800mL,若用98%的浓硫酸(ρ=1.84g/mL)来配制,量取浓硫酸时,需使用的量筒的规格为
A.10mL B.20mL C.50mL D.100mL
(2)加入的NaClO可与Mn2+反应:Mn2++ClO-+H2O→MnO2↓+2H++Cl-,还有一种离子也会被NaClO氧化,该反应的离子方程式为 .
(3)滤渣的主要成份除含有Fe(OH)3、Al(OH)3外,还有 .
(4)在“除钙”前,需检验滤液中Fe3+是否被除尽,简述检验方法 .
(5)已知MgSO4、CaSO4的溶解度如下表:
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明操作步骤 .“操作I”是将滤液继续蒸发浓缩,冷却结晶, ,便得到了MgSO4?7H2O.
(6)实验中提供的硼镁泥共100g,得到的MgSO4?7H2O为172.2g,则MgSO4?7H2O的产率为 .
查看习题详情和答案>>

根据题意回答问题:
(1)实验中需用1mol/L的硫酸800mL,若用98%的浓硫酸(ρ=1.84g/mL)来配制,量取浓硫酸时,需使用的量筒的规格为
A.10mL B.20mL C.50mL D.100mL
(2)加入的NaClO可与Mn2+反应:Mn2++ClO-+H2O→MnO2↓+2H++Cl-,还有一种离子也会被NaClO氧化,该反应的离子方程式为
(3)滤渣的主要成份除含有Fe(OH)3、Al(OH)3外,还有
(4)在“除钙”前,需检验滤液中Fe3+是否被除尽,简述检验方法
(5)已知MgSO4、CaSO4的溶解度如下表:
| 温度(℃) | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
(6)实验中提供的硼镁泥共100g,得到的MgSO4?7H2O为172.2g,则MgSO4?7H2O的产率为
(2010?江苏二模)随着工业的迅速发展,产生的废水对水体的污染也日趋严重.通过控制溶液的pH对工业废水中的金属离子进行分离是实际工作中经常使用的方法.下表是常温下金属氢氧化物的Ksp(沉淀溶解平衡常数)和金属离子在某浓度下开始沉淀所需的pH(表中浓度为相应pH时溶液中有关金属离子产生沉淀的最小浓度;当溶液中金属离子浓度小于10-5 mol?L-1时通常认为该离子沉淀完全).
(1)某厂排出的废水中含有Cu2+和Fe3+,测得其浓度均小于0.1mol?L-1.为除去其中的Fe3+,回收铜,需控制的pH范围是
(2)为了处理含有Cr2O72-酸性溶液的工业废水,采用如下方法:向废水中加入适量NaCl,以Fe为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成排出,从而使废水中铬含量低于排放标准.
①Cr2O72-转变为Cr3+的离子方程式为
②pH对废水中Cr2O72-去除率的影响如右图.你认为电解过程中溶液的pH取值在
[注:去除率(%)=[(c0-c)/co]×100%,式中:co-理前废水中Cr2O72-的浓度,c-处理后废水中Cr2O72-的浓度]
(3)沉淀转化在生产中也有重要应用.例如,用Na2CO3溶液可以将锅炉水垢中的CaSO4转化为较疏松而易清除的CaCO3,该沉淀转化达到平衡时,其平衡常数K=
查看习题详情和答案>>
| 金属离子 | Ksp | pH(10-1 mol?L-1) | pH(10-5 mol?L-1) |
| Fe3+ | 4.0×10-38 | 2.7 | 3.7 |
| Cr3+ | 6.0×10-31 | 4.3 | 5.6 |
| Cu2+ | 2.2×10-20 | 4.7 | 6.7 |
| Ca2+ | 4.0×10-5 | 12.3 | 14.3 |
3.7≤pH<4.7
3.7≤pH<4.7
.(2)为了处理含有Cr2O72-酸性溶液的工业废水,采用如下方法:向废水中加入适量NaCl,以Fe为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成排出,从而使废水中铬含量低于排放标准.
①Cr2O72-转变为Cr3+的离子方程式为
Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
.
②pH对废水中Cr2O72-去除率的影响如右图.你认为电解过程中溶液的pH取值在
5~6
5~6
范围内对降低废水中的铬含量最有利,请说明理由:pH越小,Cr2O72-的去除率越大,但难形成Cr(OH)3沉淀从废水中分离;pH越大,Cr2O72-的去除率越小
pH越小,Cr2O72-的去除率越大,但难形成Cr(OH)3沉淀从废水中分离;pH越大,Cr2O72-的去除率越小
.[注:去除率(%)=[(c0-c)/co]×100%,式中:co-理前废水中Cr2O72-的浓度,c-处理后废水中Cr2O72-的浓度]
(3)沉淀转化在生产中也有重要应用.例如,用Na2CO3溶液可以将锅炉水垢中的CaSO4转化为较疏松而易清除的CaCO3,该沉淀转化达到平衡时,其平衡常数K=
3.25×103
3.25×103
(写数值).[已知Ksp(CaSO4)=9.1x10-6,Ksp(CaCO3)=2.8×10-9].