摘要:8.下列说法或表示方法正确的是 ( ) A.等物质的量的硫蒸气和硫固体分别完全燃烧.后者放出热量多 B.由H+(aq)+OH-(aq)===H2O(l);△H=-57.3kJ·mol-1可知.若将含1 mol CH3COOH的稀溶液与含1 mol NaOH的稀溶液混合.放出的热量小于57.3 kJ C.由C===C;△H= +1.90 kJ·mol-1可知.金刚石比石墨稳定 D.500℃.30MPa下.将0.5molN2(g)和1.5mol H2(g)置于密闭容器中充分反应生成NH3(g).放热19.3kJ.其热化学方程式为:N2(g)+3H2(g)2NH3(g);△H=-38.6kJ·mol-1
网址:http://m.1010jiajiao.com/timu3_id_429274[举报]
下列说法或表示方法正确的是 ( )
| A.等物质的量的硫蒸气和固体硫分别完全燃烧,后者放出热量多 |
| B.由C(石墨)= C(金刚石);△H=+1.90 kJ/mol可知,金刚石比石墨稳定 |
| C.在101kPa时,2g氢气完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)= 2H2O(l)△H=-285.8kJ/mol |
| D.在稀溶液中,H+(aq)+ OH-(aq) = H2O(l) △H=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热大于57.3kJ |
下列说法或表示方法正确的是
| A.等物质的量的硫蒸气和硫固体分别完全燃烧,前者放出热量多 |
| B.依据焓判据即可判定(NH4)2CO3受热分解可自发进行 |
| C.热化学方程式未注明温度和压强,△H表示标准状况下的数据 |
| D.能自发进行的反应一定是放热反应,不能自发进行的反应一定是吸热反应 |
下列说法或表示方法正确的是
| A.等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
B.由C(石墨)=C(金刚石)△H="+1.90" kJ·mol 可知,金刚石比石墨稳定 可知,金刚石比石墨稳定 |
C.在稀溶液中,H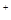 (aq))+OH (aq))+OH (aq))=H (aq))=H O(l)△H=-57.3 kJ·mol O(l)△H=-57.3 kJ·mol ,若将含0.5 mol H ,若将含0.5 mol H SO SO 的浓硫酸与含1 mol NaOH的溶液混合,放出的热大于57.3 kJ 的浓硫酸与含1 mol NaOH的溶液混合,放出的热大于57.3 kJ |
D.在101 kPa时,2 gH 完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H 完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H (g)+O (g)+O (g)=2H (g)=2H O(1)△H=-285.8 kJ·mol O(1)△H=-285.8 kJ·mol |