网址:http://m.1010jiajiao.com/timu3_id_429169[举报]
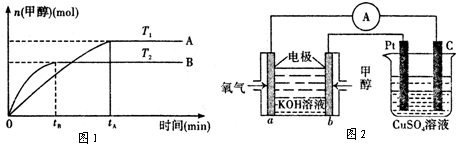
(1)合成甲醇的反应为:CO(g)+2H2(g)CH3OH(g);图1表示某次合成实验过程中甲醇的体积分数φ(CH3OH)与反应温度的关系曲线,则该反应的△H
(2)若在230℃时,平衡常数K=1.若其它条件不变,将温度升高到500℃时,达到平衡时,K
(3)在某温度下,向一个容积不变的密闭容器中通入2.5mol CO和7.5mol H2,达到平衡时CO的转化率为90%,此时容器内的压强为开始时的
(4)利用甲醇燃料电池设计如图2所示的装置:
①则该装置中b为
②当铜片的质量变化为12.8g时,a极上消耗的O2在标准状况下的体积为
(5)低碳经济是以低能耗、低污染、低排放为基础的经济模式,其中一种技术是将CO2转化成有机物实现碳循环.如:
2CO2(g)+2H2O(l)═C2H4(g)+3O2(g)△H=+1411.0kJ/mol
2CO2(g)+3H2O(l)═C2H5OH(1)+3O2(g)△H=+1366.8kJ/mol
则由乙烯水化制乙醇反应的热化学方程式

(l)已知:在 25℃、101kPa 下,1g 甲醇燃烧生成 CO2和液态水时放热 22.70kJ.请写出甲醇燃烧的热化学方程式
(2)由CO2和H2合成甲醇的化学方程式为:CO2(g)+3H2(g)
| 催化剂 | 加热 |
①合成甲醇反应的△H
②平衡常数的表达式为:
③在T1温度下,将1mol CO2和 1molH2充入一密闭恒容容器中,充分反应达到平衡后,若CO2转化率为α,则容器内的压强与起始压强的比值为
(3)利用甲醇燃料电池设计如图2所示的装置.该装置中 Pt 极为
A.工业生产应在较低的温度下进行
B.反应中吸收热量为2.55A kJ
C.平衡时混合气体中碳、氢元素的质量比1:6
D.平衡时容器内的压强为开始时的0.55倍
查看习题详情和答案>>能源问题是人类社会面临的重大课题,甲醇是未来重要的能源物质之一。
(1)合成甲醇的反应为:
CO(g)+2H2(g)![]() CH3OH(g);△H
CH3OH(g);△H
下图表示某次合成实验过程中甲醇的体积分数 φ(CH3OH)与反应温度的关系曲线,若在230℃时,平衡常数K=1。若其它条件不变,将温度升高到500℃时,达到平衡时,K 1 (填“>、< 或 = ”)
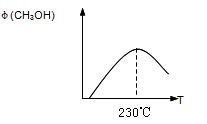
(2)利用甲醇燃料电池设计如下图所示的装置:则该装置中Cu极为 极;写出b极的电极反应式 ,当铜片的质量变化为12.8 g时:a极上消耗的O2在标准状况下的体积为 L。 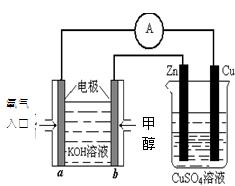
| 难(微)溶物 | 溶度积常数(Ksp) |
| BaSO4 | 1×10-10 |
| BaCO3 | 2.6×10-9 |
| CaSO4 | 7×10-5 |
| CaCO3 | 5×10-9 |
(3)工业中常将BaSO4转化为BaCO3后,再将其制成各种可溶性的钡盐(如:BaCl2)。
具体做法是用饱和纯碱溶液浸泡BaSO4粉末,并不断补充纯碱,最后BaSO4转化为BaCO3。现有足量BaSO4悬浊液,在该悬浊液中加纯碱粉末并不断搅拌,为使SO42-物质的量浓度达到0.0lmol·L-1以上,则溶液中CO32-物质的量浓度应≥ mol·L-1
查看习题详情和答案>>(10分)能源问题是人类社会面临的重大课题,甲醇是未来重要的能源物质之一。
(1)合成甲醇的反应为:CO(g)+2H2(g)CH3OH(g);下图表示某次合成实验过程中甲醇的体积分数φ(CH3OH)与反应温度的关系曲线,则该反应的△H 0。(填“>、<或=”下同)
(2)在某温度下,向一个容积不变的密闭容器中通入2.5mol CO和7.5mol H2,达到平衡时CO的转化率为90%,此时容器内的压强为开始时的 倍。
(3)利用甲醇燃料电池设计如图所示的装置:
①则该装置中b为 极,写出装置中电解池内发生反应的离子方程式 ,
②当锌片的质量变化为12.8 g时,a极上消耗的O2 在标准状况下的体积为 L。
(4)低碳经济是以低能耗、低污染、低排放为基础的经济模式,其中一种技术是将CO2转化成有机物实现碳循环。如:
2CO2(g)+2H2O(l)== C2H4(g)+3O2(g) ΔH=+1411.0 kJ/mol
2CO2(g)+3H2O(l)== C2H5OH(1)+3O2(g) ΔH=+1366.8 kJ/mol
则由乙烯水化制乙醇反应的热化学方程式 。
查看习题详情和答案>>