摘要:14.过氧化氢俗称双氧水.它是一种液体.在催化剂的作用下.易分解为水和氧气.常作氧化剂.漂白剂和消毒剂.为贮存.运输.使用的方便.工业常将H2O2转化为固态的过碳酸钠晶体(其化学式为2Na2CO3 ·3H2O2).该晶体具有Na2CO3和H2O2的双重性质.下列物质不会使过碳酸钠晶体失效的是 A.NaHCO3 B.SO2 C.稀盐酸 D.MnO2
网址:http://m.1010jiajiao.com/timu3_id_428139[举报]
过氧化氢俗称双氧水,它是一种液体,在催化剂的作用下,易分解为水和氧气,常作氧化剂、漂白剂和消毒剂。为贮存、运输、使用的方便,工业常将H2O2转化为固态的过碳酸钠晶体(其化学式为2Na2CO3 ·3H2O2),该晶体具有Na2CO3和H2O2的双重性质。下列物质不会使过碳酸钠晶体失效的是
A.NaHCO3 B.SO2 C.稀盐酸 D.MnO2
查看习题详情和答案>>|
过氧化氢俗称双氧水,它是一种液体,在催化剂的作用下,易分解为水和氧气,常作氧化剂、漂白剂和消毒剂.为贮存、运输、使用的方便,工业常将H2O2转化为固态的过碳酸钠晶体(其化学式为2Na2CO3·3H2O2),该晶体具有Na2CO3和H2O2的双重性质.下列物质不会使过碳酸钠晶体失效的是 | |
| [ ] | |
A. |
NaHCO3 |
B. |
SO2 |
C. |
稀盐酸 |
D. |
MnO2 |
(I)多项选择题
下列有关化工生产的说法中不正确的是
A.工业上用电解熔融的氯化物的方法制备金属镁和铝
B.适当提高合成氨原料气中N2的含量,可提高H2的转化率
C.从安全运输上看,硫酸厂靠近硫酸消费中心比靠近原料产地更为有利
D.利用反应NaCl(饱和)+CO2+NH3+H2O=NH4Cl+NaHCO3↓制取NaHCO3时,应在NaCl饱和溶液中先通入过量CO2再通入过量的NH3
E.硫酸厂生产时常采有高压条件提高SO2的转化率
(II)
过碳酸钠(2Na2CO3?3H2O2)俗称固体双氧水,被大量用于洗涤、印染、纺织、造纸、医药卫生等领域中.它的制备原理和路线如下:
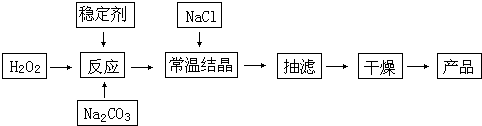
试回答下列问题:
(1)与过碳酸钠的用途相关的化学性质是
A.MnO2 B. H2S C.稀硫酸 D. NaHCO3
(2)加入NaCl的作用是
(3)工业纯碱中含有Fe3+等杂质,加入稳定剂的作用是与生成稳定的配合物.Fe3+的不良影响是
(4)反应的最佳温度控制在15~25℃,温度偏高时造成产率偏低的可能原因是
(5)有人想用过碳酸钠测定氢溴酸的浓度.若一定量的过碳酸钠与100mL氢溴酸溶液恰好完全反应,在标准状况下产生448mL气体,则所用氢溴酸的浓度为
查看习题详情和答案>>
下列有关化工生产的说法中不正确的是
ADE
ADE
A.工业上用电解熔融的氯化物的方法制备金属镁和铝
B.适当提高合成氨原料气中N2的含量,可提高H2的转化率
C.从安全运输上看,硫酸厂靠近硫酸消费中心比靠近原料产地更为有利
D.利用反应NaCl(饱和)+CO2+NH3+H2O=NH4Cl+NaHCO3↓制取NaHCO3时,应在NaCl饱和溶液中先通入过量CO2再通入过量的NH3
E.硫酸厂生产时常采有高压条件提高SO2的转化率
(II)
过碳酸钠(2Na2CO3?3H2O2)俗称固体双氧水,被大量用于洗涤、印染、纺织、造纸、医药卫生等领域中.它的制备原理和路线如下:

试回答下列问题:
(1)与过碳酸钠的用途相关的化学性质是
强氧化性
强氧化性
,下列四种物质可使过碳酸钠较快失效的是ABC
ABC
A.MnO2 B. H2S C.稀硫酸 D. NaHCO3
(2)加入NaCl的作用是
降低2Na2CO3?3H2O2溶解度,析出更多晶体
降低2Na2CO3?3H2O2溶解度,析出更多晶体
(3)工业纯碱中含有Fe3+等杂质,加入稳定剂的作用是与生成稳定的配合物.Fe3+的不良影响是
催化双氧水的分解
催化双氧水的分解
,反应方程式为2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
.
| ||
(4)反应的最佳温度控制在15~25℃,温度偏高时造成产率偏低的可能原因是
温度高时双氧水易分解
温度高时双氧水易分解
,温度偏低时造成产率偏低的可能原因是温度低时反应慢
温度低时反应慢
,而该流程中还是遗漏了一步操作,造成产品产率偏低,这步操作名称是洗涤
洗涤
.(5)有人想用过碳酸钠测定氢溴酸的浓度.若一定量的过碳酸钠与100mL氢溴酸溶液恰好完全反应,在标准状况下产生448mL气体,则所用氢溴酸的浓度为
1
1
mol/L.(已知:H2O2+2HBr=Br2+2H2O)过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口.关于双氧水,回答下列问题:
A.Na2O2+2HCl=2NaCl+H2O2
B.Ag2O+H2O2=2Ag+O2↑+H2O
C.2H2O2=2H2O+O2↑
D.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
(1)上述反应中,H2O2仅体现氧化性的反应是(填代号,下同) ,H2O2既体现氧化性又体现还原性的反应是 ,H2O2体现酸性的反应是 .
(2)上述反应说明H2O2、Ag2O、K2CrO4氧化性顺序是 .
(3)保存过氧化氢试剂瓶上的最适合贴上的一个标签是 (填序号);
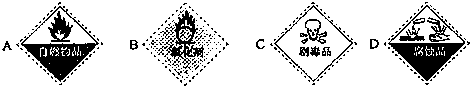
(4)某强酸反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:O2、MnO-4、H2O、Mn2+、H2O2、H+.已知该反应中H2O2只发生了如下过程:H2O2→O2.
①反应体系选择的酸是: (填序号).
A.盐酸 B.浓硫酸 C.稀硫酸 D.醋酸
②如果上述反应中有6.72L(标准状况)气体生成,转移的电子为 mol.
(5)H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称;如消除采矿业胶液中的氰化物(如KCN),经以下反应实验:KCN+H2O2+H2O=A+NH3↑,试指出生成物A的化学式为 ,并阐明H2O2被称为绿色氧化剂的理由是 .
(6)图是实验室制取氢气的常用装置,但却不能用于过氧化氢在二氧化锰催化作用下分解制氧气.某同学经过认真研究,
借助生活中的某种建筑材料和二氧化锰创造性地解决了上述问题.你认为他的做法是 .
查看习题详情和答案>>
A.Na2O2+2HCl=2NaCl+H2O2
B.Ag2O+H2O2=2Ag+O2↑+H2O
C.2H2O2=2H2O+O2↑
D.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
(1)上述反应中,H2O2仅体现氧化性的反应是(填代号,下同) ,H2O2既体现氧化性又体现还原性的反应是 ,H2O2体现酸性的反应是 .
(2)上述反应说明H2O2、Ag2O、K2CrO4氧化性顺序是 .
(3)保存过氧化氢试剂瓶上的最适合贴上的一个标签是 (填序号);
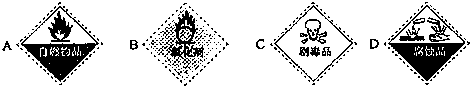
(4)某强酸反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:O2、MnO-4、H2O、Mn2+、H2O2、H+.已知该反应中H2O2只发生了如下过程:H2O2→O2.
①反应体系选择的酸是: (填序号).
A.盐酸 B.浓硫酸 C.稀硫酸 D.醋酸
②如果上述反应中有6.72L(标准状况)气体生成,转移的电子为 mol.
(5)H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称;如消除采矿业胶液中的氰化物(如KCN),经以下反应实验:KCN+H2O2+H2O=A+NH3↑,试指出生成物A的化学式为 ,并阐明H2O2被称为绿色氧化剂的理由是 .
(6)图是实验室制取氢气的常用装置,但却不能用于过氧化氢在二氧化锰催化作用下分解制氧气.某同学经过认真研究,
借助生活中的某种建筑材料和二氧化锰创造性地解决了上述问题.你认为他的做法是 .

过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口.关于双氧水,回答下列问题:
A.Na2O2+2HCl=2NaCl+H2O2
B.Ag2O+H2O2=2Ag+O2↑+H2O
C.2H2O2=2H2O+O2↑
D.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
(1)上述反应中,H2O2仅体现氧化性的反应是(填代号,下同)______,H2O2既体现氧化性又体现还原性的反应是______,H2O2体现酸性的反应是______.
(2)上述反应说明H2O2、Ag2O、K2CrO4氧化性顺序是______.
(3)保存过氧化氢试剂瓶上的最适合贴上的一个标签是______(填序号);
(4)某强酸反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:O2、MnO-4、H2O、Mn2+、H2O2、H+.已知该反应中H2O2只发生了如下过程:H2O2→O2.
①反应体系选择的酸是:______(填序号).
A.盐酸 B.浓硫酸 C.稀硫酸 D.醋酸
②如果上述反应中有6.72L(标准状况)气体生成,转移的电子为______mol.
(5)H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称;如消除采矿业胶液中的氰化物(如KCN),经以下反应实验:KCN+H2O2+H2O=A+NH3↑,试指出生成物A的化学式为______,并阐明H2O2被称为绿色氧化剂的理由是______.
(6)图是实验室制取氢气的常用装置,但却不能用于过氧化氢在二氧化锰催化作用下分解制氧气.某同学经过认真研究,
借助生活中的某种建筑材料和二氧化锰创造性地解决了上述问题.你认为他的做法是______.
 查看习题详情和答案>>
查看习题详情和答案>>
A.Na2O2+2HCl=2NaCl+H2O2
B.Ag2O+H2O2=2Ag+O2↑+H2O
C.2H2O2=2H2O+O2↑
D.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
(1)上述反应中,H2O2仅体现氧化性的反应是(填代号,下同)______,H2O2既体现氧化性又体现还原性的反应是______,H2O2体现酸性的反应是______.
(2)上述反应说明H2O2、Ag2O、K2CrO4氧化性顺序是______.
(3)保存过氧化氢试剂瓶上的最适合贴上的一个标签是______(填序号);

(4)某强酸反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:O2、MnO-4、H2O、Mn2+、H2O2、H+.已知该反应中H2O2只发生了如下过程:H2O2→O2.
①反应体系选择的酸是:______(填序号).
A.盐酸 B.浓硫酸 C.稀硫酸 D.醋酸
②如果上述反应中有6.72L(标准状况)气体生成,转移的电子为______mol.
(5)H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称;如消除采矿业胶液中的氰化物(如KCN),经以下反应实验:KCN+H2O2+H2O=A+NH3↑,试指出生成物A的化学式为______,并阐明H2O2被称为绿色氧化剂的理由是______.
(6)图是实验室制取氢气的常用装置,但却不能用于过氧化氢在二氧化锰催化作用下分解制氧气.某同学经过认真研究,
借助生活中的某种建筑材料和二氧化锰创造性地解决了上述问题.你认为他的做法是______.
 查看习题详情和答案>>
查看习题详情和答案>>