网址:http://m.1010jiajiao.com/timu3_id_42373[举报]
将下列物质分类,并用序号填空:
①氢气 ②硫磺 ③二氧化硫 ④液氧 ⑤氧化镁 ⑥矿泉水 ⑦空气 ⑧四氧化三铁 ⑨石灰水 ⑩铜丝
混合物有________;纯净物有________;化合物有________;氧化物有________;金属单质有________;非金属单质有________.
将下列物质分类,并用序号填空:
①氢气 ②硫磺 ③二氧化硫 ④液氧 ⑤氧化镁 ⑥矿泉水 ⑦空气 ⑧四氧化三铁 ⑨石灰水 ⑩铜丝
混合物有________;纯净物有________;
化合物有________;氧化物有________;
金属单质有________;
非金属单质有________;
查看习题详情和答案>>将下列物质分类,并用序号填空:
①氢气 ②硫磺 ③二氧化硫 ④液氧 ⑤氧化镁 ⑥矿泉水 ⑦空气 ⑧四氧化三铁 ⑨石灰水 ⑩铜丝
混合物有________;纯净物有________;
化合物有________;氧化物有________;
金属单质有________;
非金属单质有________;
查看习题详情和答案>>动手实验:下面是某同学研究氯气性质过程中的一个片断.请你帮助他完成部分实验并补全活动记录.
[观察]氯气的颜色、状态:__________色_________态;闻氯气的气味:__________气味.
[预测]氯气是一种非金属单质,它可能具备的性质有___________.
[实验探究]
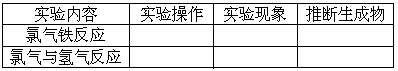
[实验结论]
(1)氯气与铁反应生成__________,氯气与氢气反应生成__________.
(2)通过比较氯气和曾经学习过的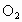 等非金属单质的性质,可推知氯气的化学性质_________,能跟__________等物质反应.
等非金属单质的性质,可推知氯气的化学性质_________,能跟__________等物质反应.
(3)这位同学是按照怎样的程序来研究物质的?
(4)在上述过程中,他都用到了哪些研究物质的方法.
(5)氧气也是一种非金属单质,说出闻其气味的方法.
查看习题详情和答案>>| X |
| X |
(1)若A是一种金属固体,C是淡黄色固体,则C的化学式为
(2)若A、B、C的焰色反应均为黄色,A是一种工业原料,B俗称小苏打,电解C的水溶液可以得到两种气态产物,这两种气态产物在工业上可以合成X,则电解C的水溶液的离子方程式为
| ||
| ||
检验B中是否含有A的试剂可以是
①HCl ②BaCl2③Ca(OH)2 ④CaCl2
(3)若A为黑色非金属单质,C是造成地球温室效应的罪魁祸首,C可与金属镁发生反应,其化学方程式为
| ||
| ||