摘要:请根据下列实验数据确定某水合含Fe(II)的盐的化学式.①将0.784g该含亚铁的盐强烈加热至质量恒定.得到0.160gFe2O3;②将0.784g该盐溶于水.加入过量的BaCl2溶液.得到0.932gBaSO4,③0.392该盐溶于水.加入过量的NaOH溶液后煮沸.释放出的氨气用50.0mL 0.10 mol/L盐酸吸收后.吸收液需要30.0mL 0.10mol/LNaOH溶液恰好中和.
网址:http://m.1010jiajiao.com/timu3_id_423365[举报]
请根据下列实验数据确定某水合物含Fe2+的盐的化学式。
(1)将0.784 g该含亚铁的盐强烈加热至质量恒定,得到0.160 g Fe2O3;
(2)将0.784 g该盐溶于水,加入过量的BaCl2溶液,得到0.932 g BaSO4;
(3)0.392 g该盐溶于水,加入过量的NaOH溶液后煮沸,释放出的氨气用50.0 mL 0.10 mol·L-1盐酸吸收后,吸收液需要30.0 mL 0.10 mol·L-1NaOH溶液恰好中和。
查看习题详情和答案>>
我国劳动人民早在4000多年前就已用一种朱红色的颜料W,请根据下列实验事实确定组成W的两种元素,并填空:
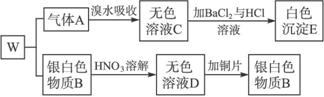
(1)W的组成元素是_______________、_______________。
(2)A![]() C的化学方程式___________________________。
C的化学方程式___________________________。
(3)使用朱红颜料W不慎会使人中毒的原因是____________________________________。
查看习题详情和答案>>
某样品质量23.24 g,可能由NaCl、CuSO4、Na2O2、K2CO3、(NH4)2SO4、Na2SO4、K2SO4中的几种组成。请根据下列实验步骤、现象和数据,分析该样品的组成。
(1)将粉末全部投入足量蒸馏水中,得无色溶液和气体,加热使反应完全,收集到的气体干燥后体积为3.36 L(标准状况)。
(2)将所得溶液分成两等份。一份中滴入酚酞试液,显红色,用4 mol·L-1盐酸12.5 mL恰好中和;向另一份中加稀HNO3酸化,无气体产生,加入过量Ba(NO3)2溶液,得到白色沉淀,经过滤、干燥,质量为12.815 g,滤液中加入AgNO3溶液无现象。
(3)所得的3.36 L气体通过浓H2SO4,体积明显减少,再通过碱石灰,体积不变。
请根据以上实验现象和数据,确定物质的组成,并计算各组分的质量。
查看习题详情和答案>> 某同学设计了如图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请根据下列实验回答问题:
某同学设计了如图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请根据下列实验回答问题:(1)若A为水,B为过氧化钠,C中盛有盐酸酸化过的FeCl2溶液,旋开活塞E后,B中发生反应的化学方程式为
2Na2O2+2H2O=4NaOH+O2
2Na2O2+2H2O=4NaOH+O2
;C中现象为变黄或加深
变黄或加深
.(2)若A为硫酸,B为亚硫酸钠固体,C中盛有氢硫酸溶液,旋开活塞E后,B中发生反应的化学方程式的为
H2SO4+Na2SO3=Na2SO4+H2O+SO2
H2SO4+Na2SO3=Na2SO4+H2O+SO2
,C中发生反应的化学方程式的为2H2S+SO2=3S+2H2O
2H2S+SO2=3S+2H2O
.(3)利用上述装置还可以验证物质的性质,如设计证明氧化性:KClO3>Cl2>Br2,则A中加浓盐酸,B中加
KClO3
KClO3
,C中发生反应的离子方程式为2Br-+Cl2=2Cl-+Br2
2Br-+Cl2=2Cl-+Br2
.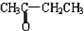 B.
B.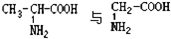
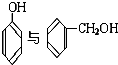 D.
D.