摘要:17.下表是元素周期表的一部分. 族 周期 ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 1 ① 2 ② ③ ④ ⑤ ⑥ 3 ⑦ ⑧ ⑨ ⑩ (1)表中元素⑩的氢化物的化学式为 .此氢化物的还原性比元素⑨的氢化物的还原性 (2)某元素原子的核外电子层中L层电子数比K层电子数多3.则该元素的元素符号是 .其单质的电子式为 . (3)已知某些不同族元素的性质也有一定的相似性.如元素③与元素⑧的氢氧化物有相似的性质.写出元素③的氢氧化物与NaOH溶液反应的化学方程式: , 又如表中与元素⑦的性质相似的不同族元素是 (4)元素⑤的氢化物是最重要的氮肥.是产量最大的化工产品之一.课本里介绍的合成氨技术叫哈伯法.是德国人哈伯在1905年发明的.其合成原理为:N2(g)+3H2(g)2NH3(g) △H= -92.4kJ/mol.他因此获得了1918年诺贝尔化学奖.试回答下列问题: ①合成氨工业中采取的下列措施可用勒夏特列原理解释的是 A.采用较高压强 B.采用500℃的高温 C.用铁触媒作催化剂 D.将生成的氨液化并及时从体系中分离出来.N2和H2循环到合成塔中并补充N2和H2 ②右图是实验室模拟工业法合成氨的简易装置. 简述检验有氨气生成的方法 . ③在298K时.将10 mol N2和30 mol H2放入合成塔中.为何放出的热量小于924kJ? . ④1998年希腊亚里斯多德大学的Marmellos和Stoukides发明一种合成氨的新方法.在常压下.将H2与用He稀释的N2分别通入一加热到570℃的.以锶-铈-钇-钙钛矿多孔陶瓷(SCY)为固体电解质的电解池中转化为氨气(SCY陶瓷能传递H+).H2转化率达到78%.其实验装置如图所示. 阴极的电极反应式 . 已知白色固体N中阴.阳离子具有相同的核外电子层结构. (1)写出M中存在的离子: (2) 请写出M与N反应的离子方程式: . (3)写出A在空气中锻烧的化学方程式: . (4)某同学取H的溶液.通入气体B.所得溶液中仍只有一种阴离子.请写出上 述变化过程中的离子方程式 .
网址:http://m.1010jiajiao.com/timu3_id_420197[举报]
下表是元素周期表的一部分.
(1)表中元素⑩的氢化物的化学式为
(2)某元素是空气中含量最多的元素,则该元素的元素符号是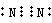
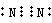 .
.
(3 已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑧的氢氧化物有相似的性质.写出元素③的氢氧化物与NaOH溶液反应的化学方程式
又如表中与元素⑦的性质相似的不同族、不同周期元素X是
查看习题详情和答案>>
| 族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 1 | ① | ||||||
| 2 | ② | ③ | ④ | ⑤ | ⑥ | ||
| 3 | ⑦ | ⑧ | ⑨ | ⑩ | |||
HCl
HCl
,此氢化物的还原性比元素⑨的氢化物的还原性弱
弱
(填强或弱)(2)某元素是空气中含量最多的元素,则该元素的元素符号是
N
N
,其单质的电子式为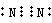
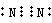
(3 已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑧的氢氧化物有相似的性质.写出元素③的氢氧化物与NaOH溶液反应的化学方程式
Be(OH)2+2NaOH═Na2BeO2+2H2O
Be(OH)2+2NaOH═Na2BeO2+2H2O
,又如表中与元素⑦的性质相似的不同族、不同周期元素X是
Li
Li
(填元素符号),预测X单质与冷水反应的化学方程式2Li+2H2O═2LiOH+H2↑
2Li+2H2O═2LiOH+H2↑
.
下表是元素周期表的一部分.
(1)表中元素⑩的氢化物的化学式为 ,此氢化物的还原性比元素⑨的氢化物的还原性 (填强或弱)
(2)某元素是空气中含量最多的元素,则该元素的元素符号是 ,其单质的电子式为 .
(3 已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑧的氢氧化物有相似的性质.写出元素③的氢氧化物与NaOH溶液反应的化学方程式 ,
又如表中与元素⑦的性质相似的不同族、不同周期元素X是 (填元素符号),预测X单质与冷水反应的化学方程式 . 查看习题详情和答案>>
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 1 | ① | ||||||
| 2 | ② | ③ | ④ | ⑤ | ⑥ | ||
| 3 | ⑦ | ⑧ | ⑨ | ⑩ | |||
(2)某元素是空气中含量最多的元素,则该元素的元素符号是 ,其单质的电子式为 .
(3 已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑧的氢氧化物有相似的性质.写出元素③的氢氧化物与NaOH溶液反应的化学方程式 ,
又如表中与元素⑦的性质相似的不同族、不同周期元素X是 (填元素符号),预测X单质与冷水反应的化学方程式 . 查看习题详情和答案>>
下表是元素周期表的一部分.
(1)表中元素⑩的氢化物的化学式为______,此氢化物的还原性比元素⑨的氢化物的还原性______(填强或弱)
(2)某元素原子的核外p电子数比s电子数少1,则该元素的元素符号是______,其单质的电子式为______.
(3)俗称为“矾”的一类化合物通常含有共同的元素是______
(4)已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑧的氢氧化物有相似的性质.写出元素③的氢氧化物与NaOH溶液反应的化学方程式______又如表中与元素⑦的性质相似的不同族元素是______(填元素符号)
查看习题详情和答案>>
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 1 | ① | ||||||
| 2 | ② | ③ | ④ | ⑤ | ⑥ | ||
| 3 | ⑦ | ⑧ | ⑨ | ⑩ | |||
(2)某元素原子的核外p电子数比s电子数少1,则该元素的元素符号是______,其单质的电子式为______.
(3)俗称为“矾”的一类化合物通常含有共同的元素是______
(4)已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑧的氢氧化物有相似的性质.写出元素③的氢氧化物与NaOH溶液反应的化学方程式______又如表中与元素⑦的性质相似的不同族元素是______(填元素符号)
查看习题详情和答案>>
下表是元素周期表的一部分.
用表中的①~⑨九种元素及其化合物,填写下列空白:
(1)②号元素的元素符号为______.
(2)非金属性最强的元素是______(填元素符号).
(3)常用来做半导体材料的元素是______(填元素符号).
(4)最高价氧化物的水化物中,碱性最强的是______(填化学式).
(5)最高价氧化物是两性氧化物的是______(填化学式).
(6)⑤、⑧两元素形成的化合物的电子式为______.
查看习题详情和答案>>
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ |
(1)②号元素的元素符号为______.
(2)非金属性最强的元素是______(填元素符号).
(3)常用来做半导体材料的元素是______(填元素符号).
(4)最高价氧化物的水化物中,碱性最强的是______(填化学式).
(5)最高价氧化物是两性氧化物的是______(填化学式).
(6)⑤、⑧两元素形成的化合物的电子式为______.
下表是元素周期表的一部分.
(1)表中元素⑩的氢化物的化学式为______,此氢化物的还原性比元素⑨的氢化物的还原性______(填强或弱)
(2)某元素原子的核外p电子数比s电子数少1,则该元素的元素符号是______,其单质的电子式为______.
(3)俗称为“矾”的一类化合物通常含有共同的元素是______
(4)已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑧的氢氧化物有相似的性质.写出元素③的氢氧化物与NaOH溶液反应的化学方程式______又如表中与元素⑦的性质相似的不同族元素是______(填元素符号)
查看习题详情和答案>>
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 1 | ① | ||||||
| 2 | ② | ③ | ④ | ⑤ | ⑥ | ||
| 3 | ⑦ | ⑧ | ⑨ | ⑩ | |||
(2)某元素原子的核外p电子数比s电子数少1,则该元素的元素符号是______,其单质的电子式为______.
(3)俗称为“矾”的一类化合物通常含有共同的元素是______
(4)已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑧的氢氧化物有相似的性质.写出元素③的氢氧化物与NaOH溶液反应的化学方程式______又如表中与元素⑦的性质相似的不同族元素是______(填元素符号)