摘要:30.[化学-物质结构与性质] K^S*5U.C W.X.Y.Z4种元素原子序数依次减小.W的原子序数为24,X原子p轨道共有11个电子,Y是第三周期主族元素.其部分电离能()如下表,Z原子价电子排布式为.请回答下列问题: 电离能/KJ·mol·L-1 Y 584 1823 2751 11584 14837 (1)W基态原子的电子排步式为 . (2)点负性:X Y. (3)R是与X同主族的短周期元素.R的氢化物沸点比X的氢化物更高.原因是: . (4)氨为常见化工原料.氨分子中N原子采用 杂化.该分子的空间构型为 .分子中N.H原子之间形成 (填“ 或“ )键,已知能与氨分子形成配离子.该配离子中存在的化学键有 . A.金属键 B.离子键 C.共价键 D.配位键
网址:http://m.1010jiajiao.com/timu3_id_419656[举报]
 (2013?临沂一模)【化学--物质结构与性质】
(2013?临沂一模)【化学--物质结构与性质】碳是形成化合物种类最多的元素.
(1)CH2=CH-C≡N是制备晴纶的原料,其分子中σ键和π键的个数之比为
2:1
2:1
(填最简整数比),写出该分子中所有碳原子的杂化方式sp2、sp
sp2、sp
.(2)乙醇(CH3CH2OH)与二甲醚(OH3OCH3)的分子式均为C2H6O,但CH3CH2OH的沸点高于CH3OCH3的沸点,其原因是
乙醇分子之间形成氢键
乙醇分子之间形成氢键
.(3)某元素位于第四周期VIII族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的价层电子排布式为
3d84s2
3d84s2
.(4)碳化硅的结构与金刚石类似,其硬度仅次于金刚石,具有较强的耐磨性能.如图所示为碳化硅的晶胞(其中●为碳原子,○为硅原子).每个碳原子周围与其距离最近的硅原子有
4
4
个.设晶胞边长为a cm,密度为b g/cm3,则阿伏加德罗常数可表示为| 160 |
| a3b |
| 160 |
| a3b |
【化学-物质结构与性质】
钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”.试回答下列问题:
(1)钛有2248和2250Ti两种原子,它们互称为
 (2)偏钛酸钡在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构如右图所示,它的化学式是
(2)偏钛酸钡在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构如右图所示,它的化学式是
(3)现有含Ti3+的配合物,化学式为[TiCl(H2O)5]Cl2?H2O.配离子[TiCl(H2O)5]2+中含有的化学键类型是
查看习题详情和答案>>
钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”.试回答下列问题:
(1)钛有2248和2250Ti两种原子,它们互称为
同位素
同位素
.Ti元素在元素周期表中的位置是第四
四
周期,第IVB
IVB
族;基态原子的电子排布式为Is22s22p63S23p63d24s2(或[Ar]3d24s2)
Is22s22p63S23p63d24s2(或[Ar]3d24s2)
按电子排布Ti元素的元素周期表分区中属于d
d
区元素. (2)偏钛酸钡在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构如右图所示,它的化学式是
(2)偏钛酸钡在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构如右图所示,它的化学式是BaTiO3
BaTiO3
.(3)现有含Ti3+的配合物,化学式为[TiCl(H2O)5]Cl2?H2O.配离子[TiCl(H2O)5]2+中含有的化学键类型是
极性共价键(或共价键)、配位键
极性共价键(或共价键)、配位键
,该配合物的配体是H2O、Cl-
H2O、Cl-
.(2011?烟台模拟)【化学--物质结构与性质】
微粒A、B、C为分子,D和F为阳离子,E为阴离子,它们都含有10个电子;B溶于A后所得的物质可电离出D和E;C是重要的化石能源.将A、B和含F离子的物质混合后可得D和一种白色沉淀.G3+离子与Ar原子的电子层结构相同.请回答:
(1)基态G原子的外围电子排布式是
(2)根据等电子体原理,D离子的空间构型是
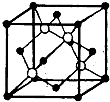
(3)构成C的中心原子可以形成多种单质,其中有一种为空间网状结构,右图立方体中心的“ ”表示该晶体中的一个原子,请在该立方体的顶点上用“
”表示该晶体中的一个原子,请在该立方体的顶点上用“ ”表示出与之紧邻的原子.
”表示出与之紧邻的原子.
(4)光谱证实F与烧碱溶液反应有Na[F(OH)4]生成,则Na[F(OH)4]中不存在
a.金属键 b.离子键 c.非极性键 d.极性键 f.配位键 g.σ键 h.π键.
查看习题详情和答案>>
微粒A、B、C为分子,D和F为阳离子,E为阴离子,它们都含有10个电子;B溶于A后所得的物质可电离出D和E;C是重要的化石能源.将A、B和含F离子的物质混合后可得D和一种白色沉淀.G3+离子与Ar原子的电子层结构相同.请回答:
(1)基态G原子的外围电子排布式是
3d14s2
3d14s2
.在A、B、C三种分子中,属于非极性分子的有CH4
CH4
(写化学式).(2)根据等电子体原理,D离子的空间构型是
正四面体
正四面体
,其中心原子轨道的杂化类型是sp3
sp3
.(3)构成C的中心原子可以形成多种单质,其中有一种为空间网状结构,右图立方体中心的“
 ”表示该晶体中的一个原子,请在该立方体的顶点上用“
”表示该晶体中的一个原子,请在该立方体的顶点上用“ ”表示出与之紧邻的原子.
”表示出与之紧邻的原子.
(4)光谱证实F与烧碱溶液反应有Na[F(OH)4]生成,则Na[F(OH)4]中不存在
ach
ach
(填字母).a.金属键 b.离子键 c.非极性键 d.极性键 f.配位键 g.σ键 h.π键.
(2010?青岛二模)【化学-物质结构与性质】
第四周期的Cr、Fe、Co、Ni、Cu、Zn等许多金属能形成配合物.
(1)Cr的核外电子排布式为
(2)科学家通过X射线测得胆矾结构示意图可简单表示如下:

图中虚线表示的作用力为
(3)胆矾溶液与氨水在一定条件下可以生成Cu(NH3)4SO4?H2O晶体.在Cu(NH3)4SO4?H2O晶体中,[Cu(NH3)4]2+ 为平面正方形结构,则呈正四面体结构的原子团是
(4)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,呈正四面体构型.试推测四羰基镍的晶体类型是
A.水 B.四氯化碳 C.苯 D.硫酸镍溶液.
查看习题详情和答案>>
第四周期的Cr、Fe、Co、Ni、Cu、Zn等许多金属能形成配合物.
(1)Cr的核外电子排布式为
1s22s22p63s23p63d54s1
1s22s22p63s23p63d54s1
;(2)科学家通过X射线测得胆矾结构示意图可简单表示如下:

图中虚线表示的作用力为
氢键、配位键
氢键、配位键
;(3)胆矾溶液与氨水在一定条件下可以生成Cu(NH3)4SO4?H2O晶体.在Cu(NH3)4SO4?H2O晶体中,[Cu(NH3)4]2+ 为平面正方形结构,则呈正四面体结构的原子团是
SO42一
SO42一
,其中心原子的杂化轨道类型是sp3
sp3
;(4)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,呈正四面体构型.试推测四羰基镍的晶体类型是
分子晶体
分子晶体
,Ni(CO)4 易溶于下列BC
BC
.A.水 B.四氯化碳 C.苯 D.硫酸镍溶液.
[化学--物质结构与性质]
(1)第ⅢA、ⅤA元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似.Ga原子的电子排布式为
(2)NH3分子的空间构型是:
(3)NH3与PH3相比,热稳定性更强的是:
(4)一定压强,将NH3和PH3混合气体降温时,首先液化的物质是
(5)铜、铁元素能形成多种配合物.微粒间形成配位键的条件是:一方是能够提供孤电子对的原子或离子,另一方是具有
查看习题详情和答案>>
(1)第ⅢA、ⅤA元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似.Ga原子的电子排布式为
1s22s22p63s23p63d104s24p1
1s22s22p63s23p63d104s24p1
.在GaN晶体中,与同一个Ga原子相连的N原子构成的空间构型为正四面体
正四面体
.在四大晶体类型中,GaN属于原子
原子
晶体.(2)NH3分子的空间构型是:
三角锥型
三角锥型
,中心原子N的杂化轨道类型是:sp3
sp3
.(3)NH3与PH3相比,热稳定性更强的是:
NH3
NH3
,理由是:氮的原子半径比磷的原子半径小,N-H键长比P-H键长短,键能更大,分子更稳定
氮的原子半径比磷的原子半径小,N-H键长比P-H键长短,键能更大,分子更稳定
.(4)一定压强,将NH3和PH3混合气体降温时,首先液化的物质是
NH3
NH3
,理由是:因为氨分子之间存在氢键,使分子间作用力更大,沸点更高
因为氨分子之间存在氢键,使分子间作用力更大,沸点更高
.(5)铜、铁元素能形成多种配合物.微粒间形成配位键的条件是:一方是能够提供孤电子对的原子或离子,另一方是具有
能够接受孤电子对的空轨道
能够接受孤电子对的空轨道
的原子或离子.