网址:http://m.1010jiajiao.com/timu3_id_419507[举报]
(1)汽车尾气中含有氮氧化物,严重污染大气.NO和NO2是常见的氮氧化物,这两种氮氧化物中,呈红棕色的是
(2)一氧化氮在常温下很容易与空气中的氧气化合,生成二氧化氮.该反应的化学方程式为
(3)实验室常用NH3做“喷泉实验”,该实验说明NH3的溶解性是
(4)干燥的氯气可以使红色的鲜花变成无色,但却不能使干燥的有色布条褪色,由此说明Cl2本身
(5)蘸有浓盐酸的玻璃棒靠近蘸有浓氨水的玻璃棒,可以看到的实验现象是
某一化学反应的实验装置如下图所示:
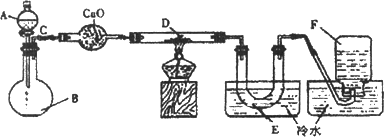
A~F属于F列物质中某一种:
浓硫酸、浓盐酸、浓氨水、锌粒、铜片、食盐、氧化钙、氧化铜、氮气、氧气、一氧化碳和水.
实验现象:
①D物质由黑色变为红色
②无水硫酸铜粉末放入无色透明的E中得到蓝色溶液
③燃着的镁带伸入无色无味的F中.镁带继续燃烧,生成一种灰黄色物质.将该物质放入水中,有气体放出,该气体能使润湿的红色石蕊试纸变蓝.通避分析回答:
(1)写出A~F中某些物质的名称:A________,F________;
(2)写出有关的化学方程式:C与D________;
F与Mg的反应产物与水的反应________.
(3)用上图中的气体发生器还可以制取氢气、二氧化碳、硫化氢等,问实验室条件下,能制取氧气和氯化氢吗?若能,请写出相应的反应方程式和文字表述;若不能,此空不填.
________;________.
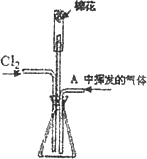
(4)见下图装置中试管口放置的棉花中应该浸有一种液体,这种液体是________,其作用是:________.
方法一:将氨气通入灼热的氧化铜粉末,得到纯净的氮气和铜;
方法二:将空气通过灼热的铜,得到较纯净的氮气和氧化铜粉末;
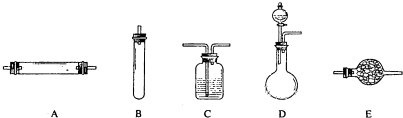
方法三:将亚硝酸钠(NaNO2)和氯化铵的混合溶液加热,氮元素全部转化为氮气.进行实验时可选择的实验仪器如下图所示(省略夹持装置与加热装置):
(1)方法一:制氮气所需的氨气可以用浓氨水滴加到生石灰中得到,此反应的发生装置最好选用
(2)方法二:为保证所得氮气尽可能纯净,除了使用铜外,还可以向装置
(选填装置编号)中加入
(3)方法三:制氮气的化学方程式为:
(4)绿色化学是指在制造和应用化学产品时应有效利用(最好可再生)原料,消除废物和避免使用有毒的和危险的试剂与溶剂.在制取氮气的3种方法中,联合使用方法-和方法二与单独使用方法三相比,具有很多优越性,请从绿色化学的角度进行评价:
(5)1892年,英国科学家瑞利(Rayleigh)发现,采用方法二得到的氮气在相同条件下比方法三得到的氮气密度总是偏大5‰左右.若上述实验设计与操作均无错误,且氮气已完全干燥,请解释产生这一现象的原因:
实验室获取氮气有很多种途径,常见的3种方法是:
方法一:将氨气通入灼热的氧化铜粉末,得到纯净的氮气和铜;
方法二:将空气通过灼热的铜,得到较纯净的氮气和氧化铜粉末;
方法三:将亚硝酸钠(NaNO2)和氯化铵的混合溶液加热,氮元素全部转化为氮气。
进行实验时可选择的实验仪器如下图所示(省略夹持装置与加热装置):
(1)方法一:制氮气所需的氨气可以用浓氨水滴加到生石灰中得到,此反应的发生装置最好选用_____________________(选填装置编号)。请写出生石灰在此反应中的两个作用:__________________________________,___________________________________________.
(2)方法二:为保证所得氮气尽可能纯净,除了使用铜外,还可以向装置_________________
(选填装置编号)中加入_________________________以除去其它杂质气体。
(3)方法三:制氮气的化学方程式为:_____________________________________________。
(4)绿色化学是指在制造和应用化学产品时应有效利用(最好可再生)原料,消除废物和避免使用有毒的和危险的试剂与溶剂。在制取氮气的3种方法中,联合使用方法—和方法二与单独使用方法三相比,具有很多优越性,请从绿色化学的角度进行评价:_____________
______________________________________________________________________________.
(5) 1892年,英国科学家瑞利(Rayleigh)发现,采用方法二得到的氮气在相同条件下比方法三得到的氮气密度总是偏大5‰左右。若上述实验设计与操作均无错误,且氮气已完全干燥,
请解释产生这一现象的原因:_______________________________________________.
三氯化氮是液氯等生产过程中能引起爆炸的一种化合物。由原盐、生产用水中含有的氮氢化合物―――氨随盐水进入电解槽它在电解过程中,与电解产物氯气反应或者是用水洗涤氯气而生成。由于它易分解并释放出大量气体而易发生爆炸事故。在液氯生产过程中,当NCl3质量分数(指NCl3的质量占氯气和NCl3的总质量的百分比)超过5%时即有爆炸的危险。
⑴在氯化铵遇到Cl2时,当PH值<5时,生成三氯化氮的化学方程式: 。
⑵NCl3爆炸时生成N2和C12。已知24.1g NCl3发生上述反应时放出的热量为91.2KJ,则标准状况下2.24LCl2生成时能放出热量 KJ。
⑶某氯碱厂为测氯气中三氯化氮的含量,将样品先用内盛15.0 mL盐酸试剂的吸收管吸收NCl3(NCl3+HCl→NH4Cl+C12,未配平),然后用内盛400 mL 30.0%(ρ=1.22g/cm3)工业氢氧化钠吸收瓶吸收氯气,碱吸收瓶吸收后质量增加77.1g。三氯化氮吸收管内的氯化铵经仪器测定:其中NH4+质量为0.405g。试求该样品中NCl3的质量分数,该样品是否安全?(请写出计算过程)
查看习题详情和答案>>