摘要:现有某一铵盐.为测定其氮的质量分数.称取铵盐样品2.55g.溶于水后.再加入足量HCHO溶液配成100mL溶液.充分反应后.从中取出5.00mL溶液.用0.100mol·L-1的NaOH溶液进行中和滴定.恰好用去19.5mL.试求该铵盐中氮元素的质量分数为 .20.硝酸工业尾气中NO.NO2被NaOH溶液吸收的主要反应为:2NO2+2NaOH=NaNO2+NaNO3+H2O,NO2+NO+2NaOH=2NaNO2+H2O.若用纯碱溶液处理尾气.反应类似.生成NaNO2.NaNO3.同时放出CO2. (1)现有标准状况下aLNO2(其中N2O4的体积分数为20%)和bLNO的混合气体恰好被200mLNa2CO3溶液完全吸收.则a.b应满足的关系是 .Na2CO3溶液的物质的量浓度是 mol·L-1. (2)若有标准状况下氮氧化物的混合气体2.016L恰好与1mol·L-1的Na2CO3溶液50mL完全反应.且生成的NaNO2与NaNO3的物质的量之比为4∶1.则混合气体中N2O4与NO2的体积比为 .
网址:http://m.1010jiajiao.com/timu3_id_41944[举报]
已知NH4+与HCHO在水溶液中发生如下反应:4NH4++6HCHO→(CH2)6N4+4H++6H2O。现有某一铵盐,为测定其氮的质量分数,称取铵盐样品m g,溶于水后,再加入足量HCHO溶液配成100 mL溶液。充分反应后,从中取出V1 mL溶液,用c mol·L-1的NaOH溶液进行中和滴定,恰好用去V2 mL。试求该铵盐中氮元素的质量分数为:
A.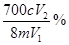 B.
B.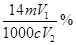 C.
C.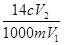 D.
D.
查看习题详情和答案>>
已知NH4+与HCHO在水溶液中发生如下反应:4NH4++6HCHO→(CH2)6N4+4H++6H2O。现有某一铵盐,为测定其氮的质量分数,称取铵盐样品m g,溶于水后,再加入足量HCHO溶液配成100 mL溶液。充分反应后,从中取出V1 mL溶液,用c mol·L-1的NaOH溶液进行中和滴定,恰好用去V2 mL。试求该铵盐中氮元素的质量分数为:
A. | B. | C.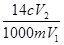 | D. |
已知NH4+与HCHO在水溶液中发生如下反应:4NH4++6HCHO→(CH2)6N4+4H++6H2O。现有某一铵盐,为测定其氮的质量分数,称取铵盐样品m g,溶于水后,再加入足量HCHO溶液配成100 mL溶液。充分反应后,从中取出V1 mL溶液,用c mol·L-1的NaOH溶液进行中和滴定,恰好用去V2 mL。试求该铵盐中氮元素的质量分数为:
A.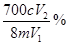 | B.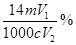 | C.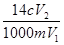 | D.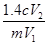 |
| |||||||||||||||||||||||||||||||||
三农问题是政府和社会关注的问题,化肥是土地的营养品.某农资商店出售一种化肥,其有效成分为氯化铵,现欲测定该种化肥中氮元素的质量分数,设计实验步骤如下(杂质中不含氮元素,且杂质均不与盐酸或氢氧化钠溶液反应):
①配制1.00mol/L的HCl溶液和1.00mol/L的NaOH溶液;
②每次取1.00g此化肥样品,溶于20mL蒸馏水中;
③加入30.00mL1.00mol/L的NaOH溶液,将反应后的溶液加热煮沸约1分钟,冷却至常温;
④…;
⑤重复②③④步操作1-2次;
⑥记录整理实验所得数据,计算该化肥中氮元素的质量分数.
请回答下列问题:
(1)写出步骤④中的实验内容
(2)下列仪器中,配制盐酸和氢氧化钠溶液都能用到的是
A.玻璃棒 B.托盘天平 C.烧杯 D.漏斗
(3)步骤⑤的实验目的是
(4)配制本实验所需的1.00mol/L的盐酸和1.00mol/L的NaOH溶液从节约化学药品的角度出发,最好应选用的容量瓶规格分别为
A.50mL,50mL B.150mL,100mL C.100mL,150mL D.250mL,500mL
(5)若以Vx(mL)表示实验所测定消耗盐酸数据的平均值,该化肥样品中氮元素的质量分数计算表达式为
×100%
×100%.(不需要化简)
查看习题详情和答案>>
①配制1.00mol/L的HCl溶液和1.00mol/L的NaOH溶液;
②每次取1.00g此化肥样品,溶于20mL蒸馏水中;
③加入30.00mL1.00mol/L的NaOH溶液,将反应后的溶液加热煮沸约1分钟,冷却至常温;
④…;
⑤重复②③④步操作1-2次;
⑥记录整理实验所得数据,计算该化肥中氮元素的质量分数.
请回答下列问题:
(1)写出步骤④中的实验内容
以酚酞为指示剂,用1.00mol/L的HCl溶液滴定,达到滴定终点用去V(mL)
以酚酞为指示剂,用1.00mol/L的HCl溶液滴定,达到滴定终点用去V(mL)
,写出实验步骤④中的离子方程式:OH-+H+═H2O
OH-+H+═H2O
.(2)下列仪器中,配制盐酸和氢氧化钠溶液都能用到的是
AC
AC
A.玻璃棒 B.托盘天平 C.烧杯 D.漏斗
(3)步骤⑤的实验目的是
减小误差,提高实验结果的准确度
减小误差,提高实验结果的准确度
.(4)配制本实验所需的1.00mol/L的盐酸和1.00mol/L的NaOH溶液从节约化学药品的角度出发,最好应选用的容量瓶规格分别为
C
C
(填字母选项).A.50mL,50mL B.150mL,100mL C.100mL,150mL D.250mL,500mL
(5)若以Vx(mL)表示实验所测定消耗盐酸数据的平均值,该化肥样品中氮元素的质量分数计算表达式为
| (30×10-3L×1mol/L-Vx×10-3L×1mol/L)×14g/mol |
| 1g |
| (30×10-3L×1mol/L-Vx×10-3L×1mol/L)×14g/mol |
| 1g |