摘要:5.将电解质分为强.弱电解质的依据是 A.在一定条件下的电离程度 B.属于离子化合物还是共价化合物 C.熔融状态下是否完全电离 D.溶于水后的导电能力是强还是弱
网址:http://m.1010jiajiao.com/timu3_id_411537[举报]
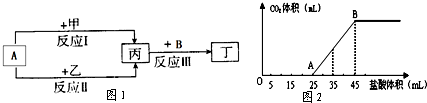
在图1物质转化关系中,反应的条件和部分产物已略去.其中A为常用的溶剂,B为常见的有色气体单质.
回答下列问题:若甲、乙是两种常见金属,反应Ⅲ是工业制盐酸的反应.
(1)反应I中,甲在通常条件下和A剧烈反应,除丙外,还生成一种焰色反应为黄色的物质,则工业上生产甲的一般方法是 .
A.热分解法 B.热还原法 C.电解法
(2)反应Ⅱ中,乙与A在高温下反应,除丙外,还生成一种有磁性的物质,则反应Ⅱ的化学方程式是 .
(3)通过比较反应I、Ⅱ的反应条件,可得出甲的金属性比乙的金属性强弱关系,比较二者金属性强弱的依据还可以是 (写出一种即可).
(4)将3.5g甲的碳酸盐、碳酸氢盐和氢氧化物的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol?L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如图2所示.
①写出OA段所发生反应的离子方程式 .
②当加入35mL盐酸时,产生CO2的体积为 mL(标准状况).
(5)若甲、乙是化合物,反应Ⅲ是工业制漂白液的反应.其中乙为含有非极性键的离子化合物,若向氯化亚铁溶液中加入固体乙,产生红褐色沉淀,但无气体生成,该反应的离子方程式为 .
查看习题详情和答案>>
回答下列问题:若甲、乙是两种常见金属,反应Ⅲ是工业制盐酸的反应.

(1)反应I中,甲在通常条件下和A剧烈反应,除丙外,还生成一种焰色反应为黄色的物质,则工业上生产甲的一般方法是
A.热分解法 B.热还原法 C.电解法
(2)反应Ⅱ中,乙与A在高温下反应,除丙外,还生成一种有磁性的物质,则反应Ⅱ的化学方程式是
(3)通过比较反应I、Ⅱ的反应条件,可得出甲的金属性比乙的金属性强弱关系,比较二者金属性强弱的依据还可以是
(4)将3.5g甲的碳酸盐、碳酸氢盐和氢氧化物的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol?L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如图2所示.
①写出OA段所发生反应的离子方程式
②当加入35mL盐酸时,产生CO2的体积为
(5)若甲、乙是化合物,反应Ⅲ是工业制漂白液的反应.其中乙为含有非极性键的离子化合物,若向氯化亚铁溶液中加入固体乙,产生红褐色沉淀,但无气体生成,该反应的离子方程式为
