摘要:2.[江苏省启东中学2009届高三最后一考]A决定物质性质的重要因素是物质结构.请回答下列问题. (1)已知A和B为第三周期元素.其原子的第一至第四电离能如下表所示: 电离能/kJ·mol-1 I1 I2 I3 I4 A 578 1817 2745 11578 B 738 1451 7733 10540 A通常显 价.A的电负性 B的电负性. (2)已知:波长为300nm的紫外光的光子所具有的能量约为399 kJ/mol.根据下表有关蛋白质分子中重要化学键的信息.说明人体长时间照射紫外光后皮肤易受伤害的原因: 共价键 C-C C-N C-S 键能/ kJ·mol-1 347 305 259 (3)科学家通过X射线探明.KCl.MgO.CaO.TiN的晶体结构与NaCl的晶体结构相似.其中3种离子晶体的晶格能数据如下表: 离子晶体 NaCl KCl CaO 晶格能/kJ·mol-1 786 715 3401 离子键的强弱可以用离子晶体的晶格能来衡量.KCl.MgO.CaO.TiN 4种离子晶体熔点从高到低的顺序是 .MgO晶体中一个Mg2+周围和它最邻近且等距离的Mg2+有 个. (4)研究物质磁性表明:金属阳离子含未成对电子越多.则磁性越大.磁记录性能越好.离子型氧化物V2O5和CrO2中.适合作录音带磁粉原料的是 . (5)某配合物的分子结构如下图所示.其分子内不含有 . A. 离子键 B. 共价键 C. 金属键 D. 配位键 E.氢键 答案. (2)紫外光具有的能量比蛋白质分子中重要的化学键C-C.C-N和C-S的键能都大.紫外光的能量足以使这些化学键断裂.从而破坏蛋白质分子 (3)TiN>MgO>CaO>KClCrO2 3( 江苏省淮阴中学2009届高三化学仿真模拟试题 )四种常见元素的性质或结构信息如下表.试根据信息回答有关问题. 元素 A B C D 性质 结构 信息 原子核外有两个电子层.最外层有3个未成对的电子 原子的M层有1对成对的p电子 原子核外电子排布为[Ar]3d104sx. 有+1.+2两种常见化合价 有两种常见氧化物.其中有一种是冶金工业常用的还原剂 ⑴写出B原子的电子排布式 . ⑵A元素的氢化物的沸点比同主族相邻元素氢化物沸点 .其原因是 . ⑶D元素最高价氧化物的熔点比同主族相邻元素最高价氧化物的熔点 .其原因是 . ⑷往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液.可生成的配合物的化学式为 .简要描述该配合物中化学键的成键情况 . ⑸下列分子结构图中的“ 表示上述相关元素的原子中除去最外层电子的剩余部分. “ 表示氢原子.小黑点“ 表示没有形成共价键的最外层电子.短线表示共价键. 则在以上分子中.中心原子采用sp3杂化形成化学键的是 , 在②的分子中有 个σ键和 个π键. 答案.⑴ 1s22s22p63s23p4 ⑵高.因为A的氢化物分子间存在氢键 ⑶低.晶体类型不同 ⑷[Cu(NH3)4]SO4, 中心原子与配位体之间以配位键相结合.内界与外界之间以离子键相结合 ⑸①③④
网址:http://m.1010jiajiao.com/timu3_id_410197[举报]
[江苏省启东中学2009届高三第一学期第二次月考 ] “人文奥运、科技奥运、绿色奥运”是2008年北京奥运会的重要特征。其中禁止运动员使用兴奋剂是重要举措之一。以下两种兴奋剂的结构分别为:
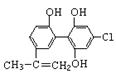
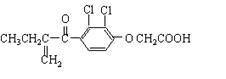
①利尿酸 ②兴奋剂X
则关于它们的说法中正确的是
 A.利尿酸分子中有三种含氧官能团,在核磁共振氢谱上共有六个峰
A.利尿酸分子中有三种含氧官能团,在核磁共振氢谱上共有六个峰
B.1 mol兴奋剂X与足量浓溴水反应,最多消耗4 mol Br2
C.两种兴奋剂均属于芳香烃化合物
D.两种分子中的所有碳原子均不可能共平面
查看习题详情和答案>>