摘要:(1)A中含有的化学键为 (2)用化学方程式表示E在冶金工业上的一种重要用途 , (3)写出反应①的化学方程式 .
网址:http://m.1010jiajiao.com/timu3_id_409347[举报]
化学是一门以实验为基础的自然科学,掌握实验方法以及完成化学实验所必顺的技能是学好化学的关键.试回答下列实验问题:

(1)某同学认为MnO2与浓HCl反应制得的Cl2中含有HCl气体,该同学设计如图1所示装量时行验证.
已知B中试剂为CCl4,则:
①判定含有HCl气体的实验现象为:
②装置A中两仪器名称分别为:
③有人认为可将D装置溶液换成另一溶液,你认为可能为:
(2)某课外研究小组设计如图所示的实验过程,用石油化学工业的废气催化剂(主要成份为Ag/α-Al2O3)来回收金属银和α-Al2O3,部分操作过程省略.α-Al2O3作为催化剂的载体,且不溶于硝酸:
Ag/α-Al2O3
①Ag/α-Al2O3加HNO3溶解可选用图2所示装置中的
②实验操作II中,所需要的主要玻璃仪器有
③实验操作II中能否用自来水代替蒸馏水?
④操作I中所发生的离子反应方程式:
查看习题详情和答案>>

(1)某同学认为MnO2与浓HCl反应制得的Cl2中含有HCl气体,该同学设计如图1所示装量时行验证.
已知B中试剂为CCl4,则:
①判定含有HCl气体的实验现象为:
C装置中淀粉碘化钾试纸不变色,D装置中有白色沉淀生成.
C装置中淀粉碘化钾试纸不变色,D装置中有白色沉淀生成.
.②装置A中两仪器名称分别为:
分液漏斗
分液漏斗
、烧瓶
烧瓶
.③有人认为可将D装置溶液换成另一溶液,你认为可能为:
氢氧化钠溶液
氢氧化钠溶液
.(2)某课外研究小组设计如图所示的实验过程,用石油化学工业的废气催化剂(主要成份为Ag/α-Al2O3)来回收金属银和α-Al2O3,部分操作过程省略.α-Al2O3作为催化剂的载体,且不溶于硝酸:
Ag/α-Al2O3

①Ag/α-Al2O3加HNO3溶解可选用图2所示装置中的
a
a
(选填a、b、c)②实验操作II中,所需要的主要玻璃仪器有
漏斗、玻璃棒、烧杯
漏斗、玻璃棒、烧杯
.③实验操作II中能否用自来水代替蒸馏水?
否
否
(填“能”或“否”)原因是一般用自来水用氯气消毒,氯气和水反应生成盐酸和次氯酸Cl2+H2O=H++Cl-+HClO,盐酸和氧化铝反应生成氯化铝6 H++Al2O3=2Al3++3H2O,导致回收的氧化铝的质量减少,所以不能用自来水代替蒸馏水.
一般用自来水用氯气消毒,氯气和水反应生成盐酸和次氯酸Cl2+H2O=H++Cl-+HClO,盐酸和氧化铝反应生成氯化铝6 H++Al2O3=2Al3++3H2O,导致回收的氧化铝的质量减少,所以不能用自来水代替蒸馏水.
(结合有关离子方程式给以必要的文字说明)④操作I中所发生的离子反应方程式:
Ag+NO3-+2H+=3Ag++NO↑+H2O
Ag+NO3-+2H+=3Ag++NO↑+H2O
.化学是一门以实验为基础的自然科学,掌握实验方法以及完成化学实验所必需的技能,是学好化学的关键.试回答下列与实验有关的问题:
(1)某同学认为MnO2与浓HCl反应制得的Cl2中含有HCl气体,该同学设计如图所示装置进行验证.最终该同学判定含有HCl气体的依据是:装置C中的试纸颜色无变化,装置D中产生白色沉淀.(部分夹持装置和加热装置省略)
①装置B中的试剂是
②装置C的作用是
(2)某课外研究小组设计如图所示的实验过程,用石油化学工业的废弃催化剂(主要成分:Ag/a-Al2O3)来回收金属银和a-Al2O3,a-Al2O3作为催化剂的载体,且不溶于硝酸.(部分操作过程省略)

①进行操作Ⅰ可选用如图所示装置中的装置

②实验操作Ⅱ中,所需的主要玻璃仪器有
③实验操作Ⅱ中能否用自来水代替蒸馏水,
查看习题详情和答案>>
(1)某同学认为MnO2与浓HCl反应制得的Cl2中含有HCl气体,该同学设计如图所示装置进行验证.最终该同学判定含有HCl气体的依据是:装置C中的试纸颜色无变化,装置D中产生白色沉淀.(部分夹持装置和加热装置省略)

①装置B中的试剂是
四氯化碳
四氯化碳
(填写名称);②装置C的作用是
检验Cl2是否除净,防止干扰实验效果
检验Cl2是否除净,防止干扰实验效果
.(2)某课外研究小组设计如图所示的实验过程,用石油化学工业的废弃催化剂(主要成分:Ag/a-Al2O3)来回收金属银和a-Al2O3,a-Al2O3作为催化剂的载体,且不溶于硝酸.(部分操作过程省略)

①进行操作Ⅰ可选用如图所示装置中的装置
a
a
(选填a、b、c);
②实验操作Ⅱ中,所需的主要玻璃仪器有
漏斗、烧杯、玻璃棒
漏斗、烧杯、玻璃棒
;③实验操作Ⅱ中能否用自来水代替蒸馏水,
否
否
(填“能”或“否”);为什么?因为自来水中含有Cl-,会发生反应Ag++Cl-=AgCl↓,导致回收的a-Al2O3中掺杂AgCl杂质
因为自来水中含有Cl-,会发生反应Ag++Cl-=AgCl↓,导致回收的a-Al2O3中掺杂AgCl杂质
(请结合有关离子方程式回答).[化学--有机化学基础]
肉桂酸甲酯( )常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精.
)常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精.
(1)肉桂酸甲酯的分子式是
(2)有关肉桂酸甲酯的叙述中,正确的是
A.能与溴的四氯化碳溶液发生加成反应 B.无法使酸性高锰酸钾溶液褪色
C.在碱性条件下能发生水解反应 D.不可能发生加聚反应
(3)G为肉桂酸甲酯的一种同分异构体,其分子结构模型如图1所示(图中球与球之间连线表示单键或双键).G的结构简式为
 ;
;
(4)用芳香烃A为原料合成G的路线如图2:?

①化合物E中的官能团有
②F→G的反应类型是 +CH3OH
+CH3OH
 +H2O
+H2O +CH3OH
+CH3OH
 +H2O.
+H2O.
③写出符合下列条件的F的同分异构体的结构简式
 .
.
ⅰ.分子内含苯环,且苯环上只有一个支链;
ⅱ.一定条件下,1mol该物质与足量银氨溶液充分反应,生成4mol银单质.
查看习题详情和答案>>
肉桂酸甲酯(
 )常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精.
)常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精.(1)肉桂酸甲酯的分子式是
C10H10O2
C10H10O2
;(2)有关肉桂酸甲酯的叙述中,正确的是
AC
AC
(填标号);A.能与溴的四氯化碳溶液发生加成反应 B.无法使酸性高锰酸钾溶液褪色
C.在碱性条件下能发生水解反应 D.不可能发生加聚反应
(3)G为肉桂酸甲酯的一种同分异构体,其分子结构模型如图1所示(图中球与球之间连线表示单键或双键).G的结构简式为


(4)用芳香烃A为原料合成G的路线如图2:?

①化合物E中的官能团有
羟基、羧基
羟基、羧基
(填名称).②F→G的反应类型是
酯化反应
酯化反应
,该反应的化学方程式为: +CH3OH
+CH3OH| 浓硫酸 |
| △ |
 +H2O
+H2O +CH3OH
+CH3OH| 浓硫酸 |
| △ |
 +H2O
+H2O③写出符合下列条件的F的同分异构体的结构简式


ⅰ.分子内含苯环,且苯环上只有一个支链;
ⅱ.一定条件下,1mol该物质与足量银氨溶液充分反应,生成4mol银单质.
[化学--有机化学基础]
有机物A(C6H8O4)为食品包装纸的常用防腐剂.A可以使溴水褪色.A难溶于水,但在酸性条件下可发生水解反应,得到B(C4H4O4)和甲醇.通常状况下B为无色晶体,能与氢氧化钠溶液发生反应.
(1)A可以发生的反应有
①加成反应 ②酯化反应 ③加聚反应 ④氧化反应
(2)B分子所含官能团的名称是
(3)B分子中没有支链,其结构简式是
(4)由B制取A的化学方程式是
(5)天门冬氨酸(C4H7NO4)是组成人体蛋白质的氨基酸之一,可由B通过以下反应制取:
天门冬氨酸的结构简式是
查看习题详情和答案>>
有机物A(C6H8O4)为食品包装纸的常用防腐剂.A可以使溴水褪色.A难溶于水,但在酸性条件下可发生水解反应,得到B(C4H4O4)和甲醇.通常状况下B为无色晶体,能与氢氧化钠溶液发生反应.
(1)A可以发生的反应有
①③④
①③④
(选填序号).①加成反应 ②酯化反应 ③加聚反应 ④氧化反应
(2)B分子所含官能团的名称是
碳碳双键
碳碳双键
、羧基
羧基
.(3)B分子中没有支链,其结构简式是
HOOCCH=CHCOOH
HOOCCH=CHCOOH
,B的具有相同官能团的同分异构体的结构简式是CH2=C(COOH)2
CH2=C(COOH)2
.(4)由B制取A的化学方程式是
HOOCCH=CHCOOH+2CH3OH
CH3OOCCH=CHCOOCH3+2H2O
| 浓硫酸 |
| △ |
HOOCCH=CHCOOH+2CH3OH
CH3OOCCH=CHCOOCH3+2H2O
.| 浓硫酸 |
| △ |
(5)天门冬氨酸(C4H7NO4)是组成人体蛋白质的氨基酸之一,可由B通过以下反应制取:
| B |
|
C |
|
天门冬氨酸 |
HOOCCH2CH(NH2)COOH
HOOCCH2CH(NH2)COOH
.[化学-选修/物质结构与性质]
(1)①对硝基苯酚水合物(2C6H5NO3?3H2O)晶体属于分子晶体,实验表明,加热至94℃时该晶体失去结晶水,该晶体失去结晶水的过程,破坏的微粒间的主要作用力属于 .
②一种铜与金形成的合金,其晶体具有面心立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子的数目之比为 .
(2)下表为元素周期表的一部分,根据此表回答下列问题:
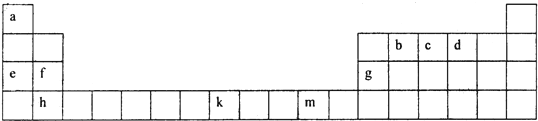
①f、g、h三种元素的第一电离能由小到大的顺序是 (用元素符号表示),b、c、d三种元素的电负性由大到小的顺序是 (用元素符号表示),b、c、d分别与a形成的简单化合物分子中,属于含有极性键的非极性分子是 .(填写化学式)
②有一种元素x和上表中所列元素k位于同周期、同一族且不相邻的位置,请写出元素x原子的基态价电子排布式 .
目前,利用金属或合金作为储氢材料的研究取得很大进展,如图是一种La-x合金储氢后的晶胞结构图.该合金储氢后,含有lmol La(镧)的合金中吸附的H2的数目为 .
③科学家把由c、d、e组成的离子化合物ecd 3和e2d在一定条件下反应得到一种白色晶体,该晶体中的阴离子为cd
,其中各原子的最外层电子均满足8电子稳定结构.该阴离子的中心原子的杂化轨道方式为 杂化,阴离子的电子式为 .
查看习题详情和答案>>
(1)①对硝基苯酚水合物(2C6H5NO3?3H2O)晶体属于分子晶体,实验表明,加热至94℃时该晶体失去结晶水,该晶体失去结晶水的过程,破坏的微粒间的主要作用力属于
②一种铜与金形成的合金,其晶体具有面心立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子的数目之比为
(2)下表为元素周期表的一部分,根据此表回答下列问题:

①f、g、h三种元素的第一电离能由小到大的顺序是
②有一种元素x和上表中所列元素k位于同周期、同一族且不相邻的位置,请写出元素x原子的基态价电子排布式

目前,利用金属或合金作为储氢材料的研究取得很大进展,如图是一种La-x合金储氢后的晶胞结构图.该合金储氢后,含有lmol La(镧)的合金中吸附的H2的数目为
③科学家把由c、d、e组成的离子化合物ecd 3和e2d在一定条件下反应得到一种白色晶体,该晶体中的阴离子为cd
3- 4 |