摘要: (3)72×103 (4)反应SO2+I2+2H2O=H2SO4+2HI n(SO2)=n(I2)=20×10-3 L×0.025 mol/L=0.0005 mol V(SO2)=0.0005 mol×22.4 L/mol=0.0112 L V(SO2)%=×100%=0.1%>0.05%.故不能直接排放
网址:http://m.1010jiajiao.com/timu3_id_409311[举报]
设NA为阿伏伽德罗常数的值,下列叙述正确的是
A.1molCH3+含电子数为10NA
B.质量均为7.8 g Na2S、Na2O2的固体中含有的阴离子数均为0.1NA
C.标准状况下,2.24L Cl2通入足量H2O或NaOH溶液中反应,转移的电子数均为0.1 NA
D.在反应S+2KNO3+3C K2S+N2↑+3CO2↑中,每生成1molN2转移的电子数为10NA
K2S+N2↑+3CO2↑中,每生成1molN2转移的电子数为10NA
查看习题详情和答案>>
设NA为阿伏伽德罗常数的值,下列叙述正确的是 ( )
A.1molCH![]() 含电子数为10NA
含电子数为10NA
B.质量均为7.8 g Na2S、Na2 O2的固体中含有的阴离子数均为0.1NA
C.2. 24LCl2通入足量H2O或NaOH溶液中反应,转移的电子数均为0.1 NA
D.在反应S+2KNO3+3C K2S+N2↑+3CO2↑中,每生成1molN2转移的电子数为10NA
设NA为阿伏伽德罗常数的值,下列叙述正确的是
A.1molCH3+含电子数为10NA
B.质量均为7.8 g Na2S、Na2O2的固体中含有的阴离子数均为0.1NA
C.标准状况下,2.24L Cl2通入足量H2O或NaOH溶液中反应,转移的电子数均为0.1 NA
D.在反应S+2KNO3+3C![]() K2S+N2↑+3CO2↑中,每生成1molN2转移的电子数为10NA
K2S+N2↑+3CO2↑中,每生成1molN2转移的电子数为10NA
氢能以其洁净、高效、高热值、环境友好等特点成为最有前途的新能源,制氢和储氢方法很多.
(1)直接热分解法制氢
①属于吸热反应的是: (选填:A、B、C、D)
②某温度下,H2O(g)?H2(g)+
O2(g),平衡常数K= (用含K1、K2、K3、K4表达)
(2)热化学循环制氢
已知:Br2(g)+CaO(s)→CaBr2(s)+
O2(g)△H=-73kJ/mol
3FeBr2(s)+4H2O(g)→Fe3O4(s)+6HBr(g)+H2(g)△H=384kJ/mol
CaBr2(s)+H2O(g)→CaO(s)+2HBr(g)△H=212kJ/mol
Fe3O4(s)+8HBr(g)→Br2(g)+3FeBr2(s)+4H2O(g)△H=-274kJ/mol
则H2O(g)?H2(g)+
O2(g),△H= KJ/mol
(3)光电化学分解制氢,其原理如图1.
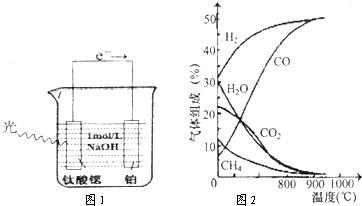
钛酸锶光电极的电极反应为4OH一+4hv-O2+2H2O,则铂电极的电极反应为 .
(4)生物质制氢,若将生物质气化炉中出来的气体[主要有CH4、CO2、H2O(g)、CO及H2]在1.0 1×105Pa下,进入转换炉,改变温度条件,各成分的体积组成关系如图2所示.下列有关图象的解读正确的是 .
A.利用CH4与H2O(g)及CO2转化为合成气CO和H2理论上是可行的
B.CH4(g)+CO2(g)→2CO(g)+2H2(g)和CH4(g)+H2O(g)→CO(g)+3H2(g),都是放热反应
C.CH4与CO2及H2O(g)转化为合成气CO和H2适宜温度约900℃
D.图象中曲线的交点处表示反应达到平衡
(5)LiBH4由于具有非常高的储氢能力,分解时生成氢化锂和两种单质,试写出反应的化学方程式 .
查看习题详情和答案>>
(1)直接热分解法制氢
| 序号 | 分解水的过程 | 平衡常数 | T=2500K | T=3000K |
| A | H2O(g)?HO(g)+H(g) | K1 | 1.34×10-4 | 8.56×10-3 |
| B | HO(g)?H(g)+O(g) | K2 | 4.22×10-4 | 1.57×10-2 |
| C | 2H(g)?H2(g) | K3 | 1.52×103 | 3.79×10 |
| D | 2O(g)?O2(g) | K4 | 4.72×103 | 7.68×10 |
②某温度下,H2O(g)?H2(g)+
| 1 |
| 2 |
(2)热化学循环制氢
已知:Br2(g)+CaO(s)→CaBr2(s)+
| 1 |
| 2 |
3FeBr2(s)+4H2O(g)→Fe3O4(s)+6HBr(g)+H2(g)△H=384kJ/mol
CaBr2(s)+H2O(g)→CaO(s)+2HBr(g)△H=212kJ/mol
Fe3O4(s)+8HBr(g)→Br2(g)+3FeBr2(s)+4H2O(g)△H=-274kJ/mol
则H2O(g)?H2(g)+
| 1 |
| 2 |
(3)光电化学分解制氢,其原理如图1.

钛酸锶光电极的电极反应为4OH一+4hv-O2+2H2O,则铂电极的电极反应为
(4)生物质制氢,若将生物质气化炉中出来的气体[主要有CH4、CO2、H2O(g)、CO及H2]在1.0 1×105Pa下,进入转换炉,改变温度条件,各成分的体积组成关系如图2所示.下列有关图象的解读正确的是
A.利用CH4与H2O(g)及CO2转化为合成气CO和H2理论上是可行的
B.CH4(g)+CO2(g)→2CO(g)+2H2(g)和CH4(g)+H2O(g)→CO(g)+3H2(g),都是放热反应
C.CH4与CO2及H2O(g)转化为合成气CO和H2适宜温度约900℃
D.图象中曲线的交点处表示反应达到平衡
(5)LiBH4由于具有非常高的储氢能力,分解时生成氢化锂和两种单质,试写出反应的化学方程式
黄铁矿(主要成分为FeS2)是工业制取硫酸的重要原料,其燃烧产物为SO2和Fe2O3.
(1)已知1g FeS2完全燃烧放出7.1kJ热量,则表示FeS2完全燃烧反应的热化学方程式为:
(2)将0.050molSO2(g)和0.030molO2(g)放入容积为1L的密闭容器中,反应:2SO2(g)+O2(g)?2SO3(g) 在一定条件下达到平衡,测得c(SO3)=0.040mol/L.则该条件下反应的平衡常数K的数值为
(3)当该反应处于平衡状态时,欲使平衡向正反应方向移动且反应速率加快,下列措施可行的是
A.向平衡混合物中充入Ar B.向平衡混合物中充入O2
C.改变反应的催化剂 D.降低反应的温度
(4)反应:2SO2(g)+O2(g)?2SO3(g)△H<0,SO2的转化率在起始温度T1=673K下随反应时间(t)的变化如下图,其他条件不变,仅改变起始温度为T2=723K,请在图中画出温度T2下SO2的转化率随反应时间变化的预期结果示意图.
查看习题详情和答案>>
(1)已知1g FeS2完全燃烧放出7.1kJ热量,则表示FeS2完全燃烧反应的热化学方程式为:
4FeS2(s)+11O2(g)
2Fe2O3(s)+8SO2(g)△H=-3408kJ/mol
| ||
4FeS2(s)+11O2(g)
2Fe2O3(s)+8SO2(g)△H=-3408kJ/mol
.
| ||
(2)将0.050molSO2(g)和0.030molO2(g)放入容积为1L的密闭容器中,反应:2SO2(g)+O2(g)?2SO3(g) 在一定条件下达到平衡,测得c(SO3)=0.040mol/L.则该条件下反应的平衡常数K的数值为
1.6×103
1.6×103
,SO2的平衡转化率为80%
80%
.(3)当该反应处于平衡状态时,欲使平衡向正反应方向移动且反应速率加快,下列措施可行的是
B
B
.(填字母)A.向平衡混合物中充入Ar B.向平衡混合物中充入O2
C.改变反应的催化剂 D.降低反应的温度
(4)反应:2SO2(g)+O2(g)?2SO3(g)△H<0,SO2的转化率在起始温度T1=673K下随反应时间(t)的变化如下图,其他条件不变,仅改变起始温度为T2=723K,请在图中画出温度T2下SO2的转化率随反应时间变化的预期结果示意图.
