网址:http://m.1010jiajiao.com/timu3_id_406948[举报]
(1)列叙述正确的是______(填写序号)
A.不慎把苯酚溶液沾到了皮肤上,应立即用大量水冲洗.
B.乙醛和新制氢氧化铜的反应实验要有明显现象,必须在强碱性条件下加热煮沸.
C.只有碳、氢两种元素组成的有机化合物称为烃.
D.甲、乙两种有机物具有相同的相对分子质量和不同结构,则甲和乙一定是同分异构体.
E.乙烯、乙醇和乙醛均能发生加成反应.
F.浓溴水滴入苯酚溶液中能产生2,4,6-三溴苯酚的白色沉淀.
G.溴的苯溶液中加少量铁粉后会剧烈反应,并放出大量的热,该现象能说明苯和溴的取代反应是放热反应.
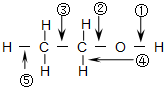
(2)乙醇分子中各化学键如图所示,对乙醇在各种反应中应断裂的键说明正确的是:(填写序号)
①和金属钠作用时,断裂______;
②和浓硫酸共热至170℃时,断裂______;
③在铜催化下和氧气反应时,断裂______;
④与氢卤酸反应时,断裂______.
 填空题
填空题(1)列叙述正确的是
A.不慎把苯酚溶液沾到了皮肤上,应立即用大量水冲洗.
B.乙醛和新制氢氧化铜的反应实验要有明显现象,必须在强碱性条件下加热煮沸.
C.只有碳、氢两种元素组成的有机化合物称为烃.
D.甲、乙两种有机物具有相同的相对分子质量和不同结构,则甲和乙一定是同分异构体.
E.乙烯、乙醇和乙醛均能发生加成反应.
F.浓溴水滴入苯酚溶液中能产生2,4,6-三溴苯酚的白色沉淀.
G.溴的苯溶液中加少量铁粉后会剧烈反应,并放出大量的热,该现象能说明苯和溴的取代反应是放热反应.
(2)乙醇分子中各化学键如图所示,对乙醇在各种反应中应断裂的键说明正确的是:(填写序号)
①和金属钠作用时,断裂
②和浓硫酸共热至170℃时,断裂
③在铜催化下和氧气反应时,断裂
④与氢卤酸反应时,断裂

(1)根据上图,计算从反应开始到平衡时,平均反应速率v (NH3)为
(2)该反应的化学平衡常数表达式K
| C2(NH3) |
| C (N2)C3(H2) |
| C2(NH3) |
| C (N2)C3(H2) |
(3)反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为
a.0.20mol/L b.0.12mol/L c.0.10mol/L d.0.08mol/L
(4)在一定条件下,合成氨反应已达化学平衡状态的是
A.3v(H2)(正)=2v(NH3)(逆) B.混合气体的密度保持不变
C.容器内压强保持不变 D.条件一定,混合气体的平均相对分子质量不再变化
E.单位时间内1mol N≡N键断裂的同时,有3mol H-H键生成
F.单位时间内生成了n mol N2的同时,减少了n mol NH3
(5)反应达到平衡后,第5分钟末,保持其它条件不变,若只把容器的体积缩小一半,平衡
(6)在第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3的浓度约为0.25mol/L),请在图1中画出第5分钟末到此平衡时NH3浓度的变化曲线.
(7)已知化学反应N2+3H2=2NH3 的能量变化如图2所示,
①1mol N 和3mol H 生成1mol NH3(g)是
②
| 1 |
| 2 |
| 3 |
| 2 |
③N2(g)和H2生成NH3(l)的热化学方程式为
目前,在研究新能源的前沿技术上,科学家致力于二氧化碳的“组合转化”技术的研究,把过多的二氧化碳转化为有益于人类的物质。
(1)乙烯的产量是衡量一个国家石油化工发展水平的标志之一,下列石油化工生产能提高乙烯的产量的是________。
A.蒸馏、分馏 B.催化裂化
C.催化裂解 D.催化重整
(2)下列说法不正确的是__________。
A.石油是混合物,分馏后得到的馏分是纯净物
B.煤隔绝空气加强热可以得到黑褐色油状的煤焦油
C.煤的气化和液化是使煤变成清洁能源的有效途径
D.从绿色化学角度考虑,以植物为主的生物质资源,是未来的理想资源
(3)如果将CO2和H2以1∶4的比例混合,通入反应器,在适当的条件下反应,可获得一种重要的能源。请完成以下化学方程式:
CO2+4H2―→(__________)+2H2O
(4)若将CO2和H2以1∶3的比例混合,使之发生反应生成某种重要的化工原料和水,该原料可能是________。
A.烷烃 B.烯烃 C.炔烃 D.芳香烃
(5)甲、乙、丙三个化肥厂生产尿素所用的原料不同,但生产流程相同:
原料— →CO(NH2)2
→CO(NH2)2
①甲厂以焦炭和水为原料;②乙厂以天然气和水为原料;③丙厂以石脑油(主要成分为C5H12)和水为原料。按工业有关规定,利用原料所制得的原料气H2和CO2的物质的量之比,若最接近合成尿素的原料气NH3(换算成H2的物质的量)和CO2的物质的量之比,则对原料的利用率最高。据此判断甲、乙、丙三个工厂哪个工厂对原料的利用率最高?________。
(6)请根据以上信息,设计工业合成尿素的条件_________________________。
目前,在研究新能源的前沿技术上,科学家致力于二氧化碳的“组合转化”技术的研究,把过多的二氧化碳转化为有益于人类的物质。
(1)乙烯的产量是衡量一个国家石油化工发展水平的标志之一,下列石油化工生产能提高乙烯的产量的是________。
A.蒸馏、分馏 B.催化裂化
C.催化裂解 D.催化重整
(2)下列说法不正确的是__________。
A.石油是混合物,分馏后得到的馏分是纯净物
B.煤隔绝空气加强热可以得到黑褐色油状的煤焦油
C.煤的气化和液化是使煤变成清洁能源的有效途径
D.从绿色化学角度考虑,以植物为主的生物质资源,是未来的理想资源
(3)如果将CO2和H2以1∶4的比例混合,通入反应器,在适当的条件下反应,可获得一种重要的能源。请完成以下化学方程式:
CO2+4H2―→(__________)+2H2O
(4)若将CO2和H2以1∶3的比例混合,使之发生反应生成某种重要的化工原料和水,该原料可能是________。
A.烷烃 B.烯烃 C.炔烃 D.芳香烃
(5)甲、乙、丙三个化肥厂生产尿素所用的原料不同,但生产流程相同:
原料—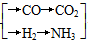 →CO(NH2)2
→CO(NH2)2
①甲厂以焦炭和水为原料;②乙厂以天然气和水为原料;③丙厂以石脑油(主要成分为C5H12)和水为原料。按工业有关规定,利用原料所制得的原料气H2和CO2的物质的量之比,若最接近合成尿素的原料气NH3(换算成H2的物质的量)和CO2的物质的量之比,则对原料的利用率最高。据此判断甲、乙、丙三个工厂哪个工厂对原料的利用率最高?________。
(6)请根据以上信息,设计工业合成尿素的条件_________________________。
查看习题详情和答案>>