摘要:10.B铅蓄电池的充放电反应为:Pb+PbO2+2H2SO4PbSO4+2H2O.放电时Pb作负极:Pb-2e-+SO42- ===PbSO4.在正极上:PbO2+2e-+4H++SO42- ===PbSO4+2H2O,充电时.H2SO4的浓度不断增大.阳极上发生的是氧化反应.是失去电子而不是得到电子.
网址:http://m.1010jiajiao.com/timu3_id_404318[举报]
铅蓄电池的示意图如图所示。下列说法正确的是
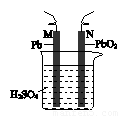
A.放电时,N为负极,其电极反应式为:PbO2+SO42-+4H++2e-=PbSO4+2H2O
B.放电时,c(H2SO4)不变,两极的质量增加
C.充电时,阳极反应式为:PbSO4+2e-= Pb+SO42-
D.充电时,若N连电源正极,则该极生成PbO2
查看习题详情和答案>>
铅蓄电池的电池反应为:Pb(s) + PbO2(s) + 2H2SO4(aq)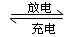 2PbSO4(s) + 2H2O(l);下列说法正确的是 ( )
2PbSO4(s) + 2H2O(l);下列说法正确的是 ( )
A.放电时覆盖Pb的电极为正极,发生还原反应
B.放电时电解质溶液中的H+向正极移动
C.充电时阳极的电极反应为:PbSO4(s) + 2e- == Pb(s) + SO42-(aq)
D.充电是阳极附近电解质溶液的pH逐渐增大
查看习题详情和答案>>
铅蓄电池的电池反应为:Pb(s) + PbO2(s) + 2H2SO4(aq)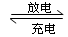 2PbSO4(s) + 2H2O(l);下列说法正确的是 ( )
2PbSO4(s) + 2H2O(l);下列说法正确的是 ( )
 2PbSO4(s) + 2H2O(l);下列说法正确的是 ( )
2PbSO4(s) + 2H2O(l);下列说法正确的是 ( )| A.放电时覆盖Pb的电极为正极,发生还原反应 |
| B.放电时电解质溶液中的H+向正极移动 |
| C.充电时阳极的电极反应为:PbSO4(s) + 2e-==Pb(s) + SO42-(aq) |
| D.充电是阳极附近电解质溶液的pH逐渐增大 |