摘要:13.标准状况下.某同学向100mL H2S饱和溶液中通入SO2. 所得溶液pH变化如下图所示.下列分析中.不正确的是 A.段反应是: B.亚硫酸是比氢硫酸更强的酸 C.原H2S溶液的物质的量浓度为0.05 mol·L-1 D.SO2在反应中作氧化剂
网址:http://m.1010jiajiao.com/timu3_id_404035[举报]
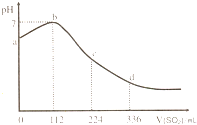 标准状况下,某同学向 100mL H2S 饱和溶液中通入SO2,所得溶液pH变化如图所示.下列分析中,正确的是( )
标准状况下,某同学向 100mL H2S 饱和溶液中通入SO2,所得溶液pH变化如图所示.下列分析中,正确的是( )| A、ab 段的反应是:SO2+2H2S=3S↓+2 H2O | B、b 点对应的溶液导电性最强 | C、原H2S溶液的物质的量浓度为0.1mol?L-1 | D、bd段对应的溶液呈酸性的原因是:H2SO3=2H++SO32- |
标准状况下,某同学向100mL H2S饱和溶液中通入SO2, 所得溶液pH变化如图所示。下列分析中,正确的是

[ ]
A.ab段反应是:SO2 + 2H2S=3S↓+2H2O
B.亚硫酸是比氢硫酸更弱的酸
C.原H2S溶液的物质的量浓度为0.05mol·L-1
D.b 点对应的溶液导电性最强
查看习题详情和答案>>
B.亚硫酸是比氢硫酸更弱的酸
C.原H2S溶液的物质的量浓度为0.05mol·L-1
D.b 点对应的溶液导电性最强