网址:http://m.1010jiajiao.com/timu3_id_40388[举报]
在实验过程中,若一种气体极易溶于一种液体,则容易发生倒吸现象,给实验造成危险.现有五位同学分别设计了一个实验,希望通过观察到的明显现象,说明CO2极易溶于NaOH溶液,设计的装置如图所示.

其中一位同学向充满CO2气体的塑料瓶E中加入NaOH溶液,盖紧瓶塞后振荡,如果看到瓶子变瘪了,说明CO2与NaOH溶液发生了反应.对A~D装置,将能达到实验目的的装置以及操作方法和实验现象填入下表中(可不填满):

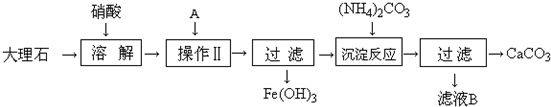
(1)溶解大理石时,用硝酸而不用硫酸的原因是
(2)操作Ⅱ的目的是
(3)写出加入碳酸铵所发生反应的离子方程式:
(4)所得滤液B是NH4NO3溶液,检验滤液中含有CO32-的方法是:
(5)写出滤液B的一种用途:
方法一:将氨气通入灼热的氧化铜粉末,得到纯净的氮气和铜;
方法二:将空气通过灼热的铜,得到较纯净的氮气和氧化铜粉末;
方法三:将亚硝酸钠(NaNO2)和氯化铵的混合溶液加热,氮元素全部转化为氮气.进行实验时可选择的实验仪器如下图所示(省略夹持装置与加热装置):
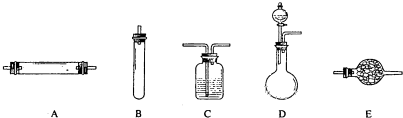
(1)方法一:制氮气所需的氨气可以用浓氨水滴加到生石灰中得到,此反应的发生装置最好选用
(2)方法二:为保证所得氮气尽可能纯净,除了使用铜外,还可以向装置
(选填装置编号)中加入
(3)方法三:制氮气的化学方程式为:
(4)绿色化学是指在制造和应用化学产品时应有效利用(最好可再生)原料,消除废物和避免使用有毒的和危险的试剂与溶剂.在制取氮气的3种方法中,联合使用方法-和方法二与单独使用方法三相比,具有很多优越性,请从绿色化学的角度进行评价:
(5)1892年,英国科学家瑞利(Rayleigh)发现,采用方法二得到的氮气在相同条件下比方法三得到的氮气密度总是偏大5‰左右.若上述实验设计与操作均无错误,且氮气已完全干燥,请解释产生这一现象的原因:

图4-3
(1)圆底烧瓶中发生反应的离子方程式:_______________________________________。
(2)如果将过量二氧化锰与20 mL 12 mol·L-1的盐酸混合加热,充分反应后生成的氯气明显少于0.06 mol。其主要原因有:
①_________________________________________________________________,
②_________________________________________________________________。
(3)为了提高浓盐酸的利用率,你对实验的建议是_____________________________________。
(4)实验结束清洗仪器时,为了减少烧瓶中残留氯气对环境的污染,可以向烧瓶中加入的溶液是_____________,有关的离子方程式是_____________________________。
查看习题详情和答案>>方法一:将氨气通过灼热的氧化铜粉末,得到氮气和铜等。
方法二:将空气通过灼热的铜,得到较纯净的氮气和氧化铜粉末。
方法三:将亚硝酸钠(NaNO2)和氯化铵的混合溶液加热,逸出氮气。
方法一有关装置如下图所示(其中有些仪器如:铁架台、铁夹、铁圈、石棉网、酒精灯等未画出):
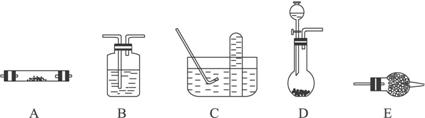
请回答下列问题:
(1)方法一制氮气:氨气是用浓氨水跟生石灰反应得到,应选用__________(填编号)作发生装置,该反应的化学方程式为______________________________。要制取并收集较纯净的氮气(可含有少量的水),还应使用上述装置中的(填装置的编号,并按气流方向从左向右列出)_____________________________________________________________________。
(2)制取氮气的三种方法中,方法一和方法二越来越受到人们的关注,经常被联合使用。这两种方法与方法三相比,其优越性在于______________________________。
查看习题详情和答案>>