摘要:2.某同学通过下列装置进行实验.推断SO2与Na2O2反应的产物.已知SO2可由浓H2SO4与Na2SO3反应制取.Na2O2完全反应. (1)怎样确定反应中是否有O2生成? , (2)装置B的作用是 , 装置D的作用是 , (3)该同学为了确定另一产物是Na2SO3还是Na2SO4.设计实验如下: 你认为该同学的实验是否合理 .理由 . 若你认为不合理.请你设计一个合理实验来确定产物(括号内填加入物质.方框内填现象),若你认为合理.可不回答此问. 检测提高
网址:http://m.1010jiajiao.com/timu3_id_40379[举报]
某同学通过下列装置进行实验,推断SO2与Na2O2反应的产物,已知SO2可由浓H2SO4与Na2SO3反应制取,与Na2O2完全反应。
(1)怎样确定反应中是否有O2生成?
(2)装置B的作用是__________________,装置D的作用是__________________。

(3)该同学为了确定另一产物是Na2SO3还是Na2SO4,设计实验如下:
![]()
![]()
你认为该同学的实验是否合理__________,理由是______________________________。
若你认为不合理,请你设计一个合理实验来确定产物(括号内填加入物质,方框内填现象);若你认为合理,可不回答此问。
![]()
某同学通过下列装置进行实验,推断SO2与Na2O2反应的产物,已知SO2可由浓H2SO4与Na2SO3反应制取,与Na2O2完全反应。
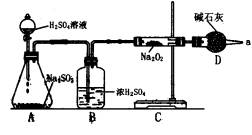
(1)怎样确定反应中是否有O2生成?
(2)装置B的作用是________,装置D的作用是________。
(3)该同学为了确定另一产物是Na2SO3还是Na2SO4,设计实验如下:
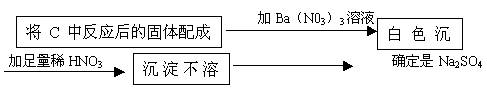
确定是Na2SO4 你认为该同学的实验是否合理________,理由是________。
若你认为不合理,请你设计一个合理实验来确定产物(括号内填加人物质,方框内填现象):若你认为合理,可不回答此问。
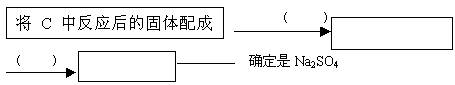
查看习题详情和答案>>
某同学想通过利用下图所示装置(夹持装置已略去)实验,探究SO2与Na2O2反应的产物.
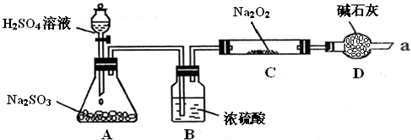
实验后测得反应前C管的质量为m1 g,反应后C管的质量为m 2 g,反应后装置D质量增加了n g.请分析:
Ⅰ.装置B的作用
Ⅱ.如何检验反应中是否有O2生成
Ⅲ.对C中固体产物提出如下假设:
假设1:只有Na2SO3
假设2:只有Na2SO4
假设3:
(1)若按假设2进行,反应方程式为
(2)若Na2O2反应完全,为确定C中固体产物的成分,甲同学设计如下实验:

得出结论:产物是Na2SO4.
该方案是否合理
(3)若假设1成立,某同学以反应前后C管的质量差( m 2-m 1 )g为依据推断生成Na2SO3的质量为( m 2-m 1 )×126/64g.老师提示推算不合理,请你分析其中的缘由:
(4)若假设2成立,则参加反应的Na2O2物质的量为
(列计算式)摩尔.
查看习题详情和答案>>

实验后测得反应前C管的质量为m1 g,反应后C管的质量为m 2 g,反应后装置D质量增加了n g.请分析:
Ⅰ.装置B的作用
干燥SO2气体,防止水蒸气与Na2O2反应
干燥SO2气体,防止水蒸气与Na2O2反应
.装置D的作用防止空气中的水蒸气和二氧化碳进入C装置与Na2O2反应,同时吸收过量的SO2,以免污染空气
防止空气中的水蒸气和二氧化碳进入C装置与Na2O2反应,同时吸收过量的SO2,以免污染空气
.Ⅱ.如何检验反应中是否有O2生成
用带火星的木条靠近干燥管口a,观察其是否燃烧
用带火星的木条靠近干燥管口a,观察其是否燃烧
.Ⅲ.对C中固体产物提出如下假设:
假设1:只有Na2SO3
假设2:只有Na2SO4
假设3:
有Na2SO3和Na2SO4
有Na2SO3和Na2SO4
.(1)若按假设2进行,反应方程式为
Na2O2+SO2=Na2SO4
Na2O2+SO2=Na2SO4
.(2)若Na2O2反应完全,为确定C中固体产物的成分,甲同学设计如下实验:

得出结论:产物是Na2SO4.
该方案是否合理
否
否
(填“是”或“否”),理由是HNO3有氧化性,据此不能确定产物是Na2SO3还是Na2SO4或二者兼有
HNO3有氧化性,据此不能确定产物是Na2SO3还是Na2SO4或二者兼有
.(3)若假设1成立,某同学以反应前后C管的质量差( m 2-m 1 )g为依据推断生成Na2SO3的质量为( m 2-m 1 )×126/64g.老师提示推算不合理,请你分析其中的缘由:
因为该反应中吸收SO2同时有O2产生,所以(m2-m1)不等于参加反应的SO2质量,故该推算不合理
因为该反应中吸收SO2同时有O2产生,所以(m2-m1)不等于参加反应的SO2质量,故该推算不合理
.(4)若假设2成立,则参加反应的Na2O2物质的量为
| m2-m1 |
| 64 |
| m2-m1 |
| 64 |
某同学想通过利用下图所示装置(夹持装置已略去)实验,探究SO2与Na2O2反应的产物.
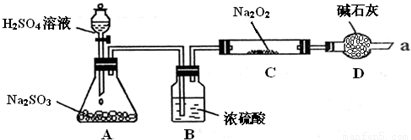
实验后测得反应前C管的质量为m1 g,反应后C管的质量为m 2 g,反应后装置D质量增加了n g.请分析:
Ⅰ.装置B的作用______.装置D的作用______.
Ⅱ.如何检验反应中是否有O2生成______.
Ⅲ.对C中固体产物提出如下假设:
假设1:只有Na2SO3
假设2:只有Na2SO4
假设3:______.
(1)若按假设2进行,反应方程式为______.
(2)若Na2O2反应完全,为确定C中固体产物的成分,甲同学设计如下实验:

得出结论:产物是Na2SO4.
该方案是否合理______(填“是”或“否”),理由是______.
(3)若假设1成立,某同学以反应前后C管的质量差( m 2-m 1 )g为依据推断生成Na2SO3的质量为( m 2-m 1 )×126/64g.老师提示推算不合理,请你分析其中的缘由:______.
(4)若假设2成立,则参加反应的Na2O2物质的量为______ (列计算式)摩尔.
查看习题详情和答案>>

实验后测得反应前C管的质量为m1 g,反应后C管的质量为m 2 g,反应后装置D质量增加了n g.请分析:
Ⅰ.装置B的作用______.装置D的作用______.
Ⅱ.如何检验反应中是否有O2生成______.
Ⅲ.对C中固体产物提出如下假设:
假设1:只有Na2SO3
假设2:只有Na2SO4
假设3:______.
(1)若按假设2进行,反应方程式为______.
(2)若Na2O2反应完全,为确定C中固体产物的成分,甲同学设计如下实验:

得出结论:产物是Na2SO4.
该方案是否合理______(填“是”或“否”),理由是______.
(3)若假设1成立,某同学以反应前后C管的质量差( m 2-m 1 )g为依据推断生成Na2SO3的质量为( m 2-m 1 )×126/64g.老师提示推算不合理,请你分析其中的缘由:______.
(4)若假设2成立,则参加反应的Na2O2物质的量为______ (列计算式)摩尔.
查看习题详情和答案>>
某研究学习小组的同学为了探究过氧化钠与二氧化硫的反应,用如图所示的装置进行实验。通入过量的
SO2气体后,用带余烬的木条检验从C导出的气体,木条复燃。实验前称得Na2O2固体的质量为m1 g,充分反应后称得生成物固体质量为m2 g。回答下列问题
SO2气体后,用带余烬的木条检验从C导出的气体,木条复燃。实验前称得Na2O2固体的质量为m1 g,充分反应后称得生成物固体质量为m2 g。回答下列问题

(1)依据题中所描述的现象,推测装置B中发生了怎样的反应,写出反应的化学方程式:____________。
(2)设计一种实验方案,验证你对上述推测的结论是正确的。
____________________________________。
(3)装置C的作用是____________。
(4)根据反应前后固体的质量,通过计算判断m2的取值范围?(用含m1的关系式表示)
____________。
查看习题详情和答案>>
(2)设计一种实验方案,验证你对上述推测的结论是正确的。
____________________________________。
(3)装置C的作用是____________。
(4)根据反应前后固体的质量,通过计算判断m2的取值范围?(用含m1的关系式表示)
____________。