摘要:21.在一个氧化还原反应体系中有反应物和生成物共六种微粒:MnO4-.Mn2+.H+.H2O.H2O2.O2.其中被氧化和被还原的元素都只有一种. (1)该反应的还原剂是 .氧化产物是 . (2)1mol还原剂在反应中失去电子的个数为 . (3)该反应的化学方程式为 .
网址:http://m.1010jiajiao.com/timu3_id_402261[举报]
在一个氧化还原反应体系中反应物、生成物共六种粒子,Fe3+、NO3-、Fe2+、NH4+、H+、H2O,下列叙述正确的是( )
| A、该反应说明Fe(NO3)2溶液不宜加酸酸化 | B、该反应中氧化剂与还原剂物质的量之比为8:1 | C、若有1mol NO3-发生氧化反应,转移电子5mol | D、若将该反应设计成原电池,则负极反应为Fe3++e-═Fe2+ |
在一个氧化还原反应体系中反应物、生成物共六种粒子,Fe3+、NO3—、Fe2+、NH4+、H+、H2O,下列叙述正确的是
| A.该反应说明Fe(NO3)2溶液不宜加酸酸化 |
| B.该反应中氧化剂与还原剂物质的量之比为8:1 |
| C.若有1mol NO3—发生氧化反应,转移电子5mol |
| D.若将该反应设计成原电池,则负极反应为Fe3++e—=Fe2+ |
在一个氧化还原反应体系中反应物、生成物共六种粒子,Fe3+、NO3-、Fe2+、NH4+、H+、H2O,下列叙述正确的是( )
查看习题详情和答案>>
| A.该反应说明Fe(NO3)2溶液不宜加酸酸化 |
| B.该反应中氧化剂与还原剂物质的量之比为8:1 |
| C.若有1molNO3-发生氧化反应,转移电子5mol |
| D.若将该反应设计成原电池,则负极反应为Fe3++e-═Fe2+ |
在一个氧化还原反应体系中反应物、生成物共六种粒子,Fe3+、NO3—、Fe2+、NH4+、H+、H2O,下列叙述正确的是
| A.该反应说明Fe(NO3)2溶液不宜加酸酸化 |
| B.该反应中氧化剂与还原剂物质的量之比为8:1 |
| C.若有1mol NO3—发生氧化反应,转移电子5mol |
| D.若将该反应设计成原电池,则负极反应为Fe3++e—=Fe2+ |
(16分)氧化还原反应在生产、生活中具有广泛的用途,贯穿古今。
(1)下列生产、生活中的事例中没有发生氧化还原反应的是________。
| A.煤的形成 | B.原电池工作 |
| C.简单机械织布 | D.我国古代烧制陶器 |
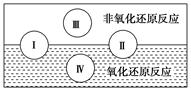
试写出有水参加的符合反应类型Ⅳ的一个化学方程式:_________________________,其中水为________剂。
(3)氯化铵常用于焊接。如:在焊接铜器时用氯化铵除去铜器表面的氧化铜以便焊接,其反应为:
________CuO+________NH4Cl
 ________Cu+______CuCl2+______ N2↑+______H2O。
________Cu+______CuCl2+______ N2↑+______H2O。①配平此氧化还原反应方程式。
②该反应中,被氧化的元素是________(填元素名称),氧化剂是________(填化学式)。
③反应中若产生0.2 mol的气体,则有________ mol的电子转移。 查看习题详情和答案>>