摘要:30.现有含等物质的量的KHSO3.NaHSO3的混合物m g与200 mL盐酸反应.假设生成的气体全部从溶液中逸出.且气体体积均以标准状况计.请以具体数值或带有字母的代数式等填写下列空白: (1)该固体混合物中KHSO3与NaHSO3的质量比为 . (2)如亚硫酸氢盐与盐酸恰好完全反应.则盐酸的物质的量浓度为 mol/L. (3)如果盐酸过量.则生成SO2气体的体积为 L. (4)如果反应后亚硫酸氢盐有剩余.盐酸不足量.要计算生成SO2气体的体积.还需知道数据是 . (5)若KHSO3和NaHSO3以任意物质的量之比混合.则m g固体混合物与足量的盐酸完全反应时生成SO2的体积范围是 .
网址:http://m.1010jiajiao.com/timu3_id_401502[举报]
已知天然气的主要成分 是一种会产生温室效应的气体,等物质够量的
是一种会产生温室效应的气体,等物质够量的 和
和 产生的温室效应,前者大,下面有关天然气的几种叙述中正确的是
产生的温室效应,前者大,下面有关天然气的几种叙述中正确的是
①天然气与煤、柴油相比是较清洁的能源
②等质量的 和
和 产生的温室效应也是前者大
产生的温室效应也是前者大
③燃烧天然气也是酸雨的成因之一
[ ]
A.①②③
B.只有①
C.①和②
D.只有③
已知天然气的主要成分 是一种会产生温室效应的气体,等物质够量的
是一种会产生温室效应的气体,等物质够量的 和
和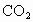 产生的温室效应,前者大,下面有关天然气的几种叙述中正确的是
产生的温室效应,前者大,下面有关天然气的几种叙述中正确的是
①天然气与煤、柴油相比是较清洁的能源
②等质量的 和
和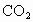 产生的温室效应也是前者大
产生的温室效应也是前者大
③燃烧天然气也是酸雨的成因之一
[ ]
A.①②③
B.只有①
C.①和②
D.只有③
尾气SO2用NaOH溶液吸收后会生成Na2SO3.现有常温下0.1mol/L Na2SO3溶液,实验测定其pH约为8,完成下列问题:
(1)该溶液中c(Na+)与 c(OH-)之比为 .该溶液中c(OH-)=c(H+)+ + (用溶液中所含微粒的浓度表示).
(2)如果用含等物质的量溶质的下列各溶液分别来吸收SO2,则理论吸收量由多到少的顺序是 (用编号排序)
A.Na2SO3 B.Ba(NO3)2 C.Na2S D.酸性KMnO4. 查看习题详情和答案>>
(1)该溶液中c(Na+)与 c(OH-)之比为
(2)如果用含等物质的量溶质的下列各溶液分别来吸收SO2,则理论吸收量由多到少的顺序是
A.Na2SO3 B.Ba(NO3)2 C.Na2S D.酸性KMnO4. 查看习题详情和答案>>
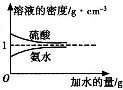 已知硫酸、氨水的密度与所加水的量的关系如图所示,现有硫酸与氨水各一份,请根据表中信息,回答下列问题:
已知硫酸、氨水的密度与所加水的量的关系如图所示,现有硫酸与氨水各一份,请根据表中信息,回答下列问题:| 溶质的物质的量浓度/mol?L-1 | 溶液的密度/g?cm-3 | |
| 硫酸 | c1 | ρ1 |
| 氨水 | c2 | ρ2 |
(2)物质的量浓度为c1mol?L-1的硫酸与水等体积混合(混合后溶液的体积变化忽略不计),所得溶液的物质的量浓度为
(3)将物质的量浓度分别为c2mol?L-1.和
| 1 |
| 5 |
| 3 |
| 5 |