网址:http://m.1010jiajiao.com/timu3_id_40121[举报]
有下列常用药:
A:阿司匹林(乙酰水杨酸)
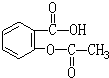
B:阿莫西林(羟氨苄青霉素)
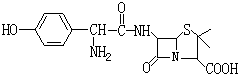
C:磺胺SN(对氨基苯磺酰胺)
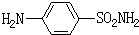
D:胃舒平(复方氢氧化铝)
(1)以上常用药中属于抗酸类药物的是______(填编号字母,下同);属于解热镇痛类药物的是______;属于抗生素类药物的是______.购买时无需医师处方的药物叫非处方药,英文缩写为______.
(2)一些抗酸类药物常会引起便秘副作用,所以常在其中添加能引起轻泻的药物,如三硅酸镁(2MgO?3SiO2?nH2O),三硅酸镁也有一定的抗酸作用,请写出三硅酸镁和胃酸(HCl)反应的化学方程式______.
(3)阿司匹林是由水杨酸(邻羟基苯甲酸)和乙酸酐(CH3CO)2O在浓硫酸存在的条件下,加热而制成的,请写出该反应的化学方程式______.
(4)写出阿司匹林在氢氧化钠溶液中水解的化学方程式______.
有下列常用药:
A:阿司匹林(乙酰水杨酸)
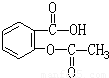
B:阿莫西林(羟氨苄青霉素)
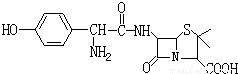
C:磺胺SN(对氨基苯磺酰胺)
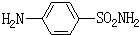
D:胃舒平(复方氢氧化铝)
(1)以上常用药中属于抗酸类药物的是______(填编号字母,下同);属于解热镇痛类药物的是______;属于抗生素类药物的是______.购买时无需医师处方的药物叫非处方药,英文缩写为______.
(2)一些抗酸类药物常会引起便秘副作用,所以常在其中添加能引起轻泻的药物,如三硅酸镁,三硅酸镁也有一定的抗酸作用,请写出三硅酸镁和胃酸(HCl)反应的化学方程式______.
(3)阿司匹林是由水杨酸(邻羟基苯甲酸)和乙酸酐(CH3CO)2O在浓硫酸存在的条件下,加热而制成的,请写出该反应的化学方程式______.
(4)写出阿司匹林在氢氧化钠溶液中水解的化学方程式______.
查看习题详情和答案>>
(15分)【化学——化学与技术】
(1)火山喷发所产生的硫黄可用于生产重要的化工原料硫酸。某企业用如图所示的工艺流程生产硫酸。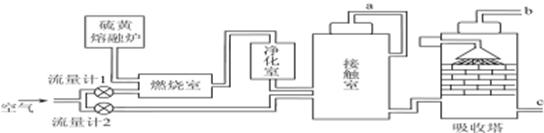
请回答下列问题:
①为充分利用反应放出的热量,接触室中应安装______________(填设备名称)。吸收塔中填充有许多瓷管,其作用是__________________________。
②为使硫黄充分燃烧,经流量计1通入燃烧室的氧气过量50%。为提高SO2转化率,经流量计2的氧气量为接触室中二氧化硫完全氧化时理论需氧量的2.5倍,则生产过程中流经流量计1和流量计2的空气体积比应为________。假设接触室中SO2的转化率为95%,b管排出的尾气中二氧化硫的体积分数为________。(空气中氧气的体积分数按0.2计),该尾气的处理方法是____________________________________________。
③与以硫铁矿为原料的生产工艺相比,该工艺的特点是________。
A.耗氧量减少 B.二氧化硫的转化率提高
C.产生的废气减少 D.不需要使用催化剂
(2)硫酸的用途非常广泛,可应用于下列哪些方面________(可多选)。
A.橡胶的硫化 B.表面活性剂“烷基苯磺酸钠”的合成
C.铅蓄电池的生产 D.过磷酸钙的制备
(3)矿物燃料的燃烧是产生大气中SO2的主要原因之一。在燃煤中加入适量的石灰石,可有效减少煤燃烧时SO2的排放,请写出此脱硫过程中反应的化学方程式__________________________________________、______________________________、___________________________________________。
利用硫酸工业废渣(主要含Fe2O3、SiO2、Al2O3、MgO等杂质)制备氧化铁的工艺流程如下:
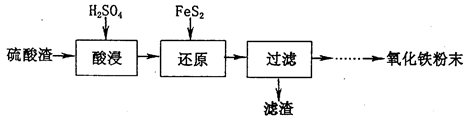
(1)“酸浸”中硫酸要适当过量,目的是:①提高铁的浸出率,②__________________。
(2)“还原”是将Fe3+转化为Fe2+,同时FeS2被氧化为SO
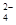 ,该反应的离子方程式为____________.
,该反应的离子方程式为____________.(3)为测定“酸浸”步骤后溶液中Fe3+的量以控制加入FeS2的量。
实验步骤为:准确量取一定体积的酸浸后的溶液于锥形瓶中,加入HCl、稍过量SnCl2,再加HgCl2除去过量的SnCl2,以二苯胺磺酸钠为指示剂,用K2Cr2O7标准溶液滴定,有关反应方程式如下:
2Fe3++Sn2++6Cl-===2Fe2++SnCl
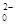
Sn2++4Cl-+2HgCl2="==" SnCl
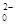 +Hg2Cl2↓
+Hg2Cl2↓6Fe2++ Cr2O
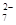 +14H+===6Fe3++2Cr3++7H2O
+14H+===6Fe3++2Cr3++7H2O①若SnCl2不足量,则测定的Fe3+量__________(填“偏高”、“偏低”、“不变”,下同)。
②若不加HgCl2,则测定的Fe3+量偏高,其原因是_____________。
(4)①可选用______________(填试剂)检验滤液中含有Fe3+。产生Fe3+的原因是_________________(用离子反应方程式表示)。
②已知部分阳离子以氢氧化物形式沉淀时溶液的,pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Mg(OH)2 | Mn(OH)2 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 | 9.4 | 8.3 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 | 12.4 | 9.8 |
a.氧化:________________________________;b.沉淀:_____________________________;
c.分离,洗涤;d.烘干,研磨。
(1)火山喷发所产生的硫黄可用于生产重要的化工原料硫酸。某企业用如图所示的工艺流程生产硫酸。
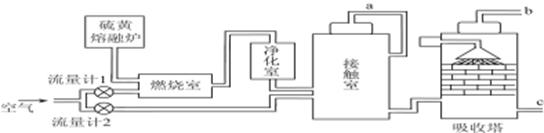
请回答下列问题:
①为充分利用反应放出的热量,接触室中应安装______________(填设备名称)。吸收塔中填充有许多瓷管,其作用是__________________________。
②为使硫黄充分燃烧,经流量计1通入燃烧室的氧气过量50%。为提高SO2转化率,经流量计2的氧气量为接触室中二氧化硫完全氧化时理论需氧量的2.5倍,则生产过程中流经流量计1和流量计2的空气体积比应为________。假设接触室中SO2的转化率为95%,b管排出的尾气中二氧化硫的体积分数为________。(空气中氧气的体积分数按0.2计),该尾气的处理方法是____________________________________________。
③与以硫铁矿为原料的生产工艺相比,该工艺的特点是________。
A.耗氧量减少 B.二氧化硫的转化率提高
C.产生的废气减少 D.不需要使用催化剂
(2)硫酸的用途非常广泛,可应用于下列哪些方面________(可多选)。
A.橡胶的硫化 B.表面活性剂“烷基苯磺酸钠”的合成
C.铅蓄电池的生产 D.过磷酸钙的制备
(3)矿物燃料的燃烧是产生大气中SO2的主要原因之一。在燃煤中加入适量的石灰石,可有效减少煤燃烧时SO2的排放,请写出此脱硫过程中反应的化学方程式__________________________________________、______________________________、___________________________________________。