网址:http://m.1010jiajiao.com/timu3_id_401032[举报]
反应N2+3H2![]() 2NH3 ⊿H= —92.4 kJ/mol 在一定温度和体积不变的密闭容器中进行并达到平衡,如果最初c (N2 )= 2mol/L,c (H2)=5mol/L,反应达到平衡时有一半的N2发生了反应,则:
2NH3 ⊿H= —92.4 kJ/mol 在一定温度和体积不变的密闭容器中进行并达到平衡,如果最初c (N2 )= 2mol/L,c (H2)=5mol/L,反应达到平衡时有一半的N2发生了反应,则:
(1)求达到平衡时, H2和NH3的浓度分别为c (H2 )= mol/L,c (NH3)= mol/L
(2)求平衡时H2的转化率为 ;求平衡时NH3的物质的量与平衡后总物质的量的比值为
(3)求该温度下的平衡常数为 ;达到平衡后,提高温度,则平衡 (填正移,逆移或不移动);K值 ;H2的转化率 (后两个空填增大,减小或不变)
查看习题详情和答案>>反应N2+3H22NH3 ⊿H= —92.4 kJ/mol 在一定温度和体积不变的密闭容器中进行并达到平衡,如果最初c (N2)= 2mol/L,c (H2)=5mol/L,反应达到平衡时有一半的N2发生了反应,则:
(1)求达到平衡时, H2和NH3的浓度分别为c (H2 )= mol/L,c (NH3)= mol/L
(2)求平衡时H2的转化率为 ;求平衡时NH3的物质的量与平衡后总物质的量的比值为
(3)求该温度下的平衡常数为 ;达到平衡后,提高温度,则平衡 (填正移,逆移或不移动);K值 ;H2的转化率 (后两个空填增大,减小或不变)
查看习题详情和答案>>
反应N2+3H2 2NH3 ⊿H= —92.4 kJ/mol 在一定温度和体积不变的密闭容器中进行并达到平衡,如果最初c (N2 )= 2mol/L,c (H2)=5mol/L,反应达到平衡时有一半的N2发生了反应,则:
2NH3 ⊿H= —92.4 kJ/mol 在一定温度和体积不变的密闭容器中进行并达到平衡,如果最初c (N2 )= 2mol/L,c (H2)=5mol/L,反应达到平衡时有一半的N2发生了反应,则:
(1)求达到平衡时, H2和NH3的浓度分别为c (H2 )= mol/L,c (NH3)=" " mol/L
(2)求平衡时H2的转化率为 ;求平衡时NH3的物质的量与平衡后总物质的量的比值为
(3)求该温度下的平衡常数为 ;达到平衡后,提高温度,则平衡 (填正移,逆移或不移动);K值 ;H2的转化率 (后两个空填增大,减小或不变)
反应N2+3H2 2NH3 ⊿H= —92.4 kJ/mol 在一定温度和体积不变的密闭容器中进行并达到平衡,如果最初c (N2
)= 2mol/L,c (H2)=5mol/L,反应达到平衡时有一半的N2发生了反应,则:
2NH3 ⊿H= —92.4 kJ/mol 在一定温度和体积不变的密闭容器中进行并达到平衡,如果最初c (N2
)= 2mol/L,c (H2)=5mol/L,反应达到平衡时有一半的N2发生了反应,则:
(1)求达到平衡时, H2和NH3的浓度分别为c (H2 )= mol/L,c (NH3)= mol/L
(2)求平衡时H2的转化率为 ;求平衡时NH3的物质的量与平衡后总物质的量的比值为
(3)求该温度下的平衡常数为 ;达到平衡后,提高温度,则平衡 (填正移,逆移或不移动);K值 ;H2的转化率 (后两个空填增大,减小或不变)
查看习题详情和答案>>
 反应过程的能量变化如图所示。已知l mol SO2(g)氧化为1 molSO3 (g)的
反应过程的能量变化如图所示。已知l mol SO2(g)氧化为1 molSO3 (g)的 。请回答下问题;
。请回答下问题;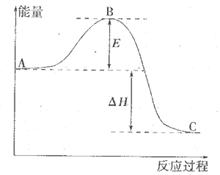
(1)E表示___________________;E的大小对该反应的反应热__________(填“有”或“无”)影响。
(2)该反应通常用V2O5作催化剂,加V2O5会使图中△H___________(填“变大”、“变小”或“不变”),理由是________。
(3)已知单质硫的燃烧热为296 kJ·mol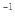 ,计算由S(s)生成2mol SO3(g)的△H =________________。
,计算由S(s)生成2mol SO3(g)的△H =________________。
(4)在一定条件下向容积为2L的容器中通入4molSO2和3molO2,充分反应达平衡后,SO3的体积分数为1/3。若在相同的条件下向容积为2L的容器中通入amolSO2和,bmolSO3,和cmol,反应向逆反应方向进行且达到平衡时SO3的体积分数也为1/3。则c的取值范围为___________。