网址:http://m.1010jiajiao.com/timu3_id_40043[举报]
(1)把一块纯净的锌片插入装有稀硫酸的烧杯里,可观察到锌片上有气泡,再平行插入一块铜片,可观察到铜片上____________(填“有”或“没有”)气泡产生.再用导线把锌片和铜片连接起来(见图A),组成一个原电池,负极为___________,正极的电极反应式为___________.
(2)如果烧杯中最初装入的是2mol/L500mL的稀硫酸溶液,构成铜锌原电池(见图B,假设产生的气体没有损失),当在标准状况下收集到11.2L的氢气时,则此时烧杯内溶液中溶质的物质的量浓度应为(溶液体积变化忽略不计)___________.
(3)金属的腐蚀分为两种:化学腐蚀(与化学物质直接接触而发生化学反应)和电化学腐蚀(由于构成原电池而发生电极反应),电化学腐蚀中又分为吸氧腐蚀和析氢腐蚀.如果电极材料分别是铁片和石墨并进行连接,插入氯化钠溶液中(见图C),放置数天后,主要发生___________电化学腐蚀,写出正极的电极反应式一.

(4)生活中利用原电池原理生产了各种各样的电池,废电池必须进行集中处理的问题已被提到议事日程,其最主要原因是___________.
(A)回收利用电池外壳的金属
(B)防止电池中汞、镉和铅等重金属离子对土壤、水源的污染
(C)防止电池中渗泄的电解液腐蚀其他物品
(D)回收其中的石墨电极
查看习题详情和答案>>(1)把一块纯净的锌片插入装有稀硫酸的烧杯里,可观察到锌片上有气泡,再平行插入一块铜片,可观察到铜片上____________(填“有”或“没有”)气泡产生.再用导线把锌片和铜片连接起来(见图A),组成一个原电池,负极为___________,正极的电极反应式为___________.
(2)如果烧杯中最初装入的是2mol/L500mL的稀硫酸溶液,构成铜锌原电池(见图B,假设产生的气体没有损失),当在标准状况下收集到11.2L的氢气时,则此时烧杯内溶液中溶质的物质的量浓度应为(溶液体积变化忽略不计)___________.
(3)金属的腐蚀分为两种:化学腐蚀(与化学物质直接接触而发生化学反应)和电化学腐蚀(由于构成原电池而发生电极反应),电化学腐蚀中又分为吸氧腐蚀和析氢腐蚀.如果电极材料分别是铁片和石墨并进行连接,插入氯化钠溶液中(见图C),放置数天后,主要发生___________电化学腐蚀,写出正极的电极反应式一.

(4)生活中利用原电池原理生产了各种各样的电池,废电池必须进行集中处理的问题已被提到议事日程,其最主要原因是___________.
(A)回收利用电池外壳的金属
(B)防止电池中汞、镉和铅等重金属离子对土壤、水源的污染
(C)防止电池中渗泄的电解液腐蚀其他物品
(D)回收其中的石墨电极
查看习题详情和答案>>(1)把一块纯净的锌片插入装有稀硫酸的烧杯里,可观察锌片上有气泡,再平行插入一块铜片,可观察到铜片 (填“有”或“没有”)气泡产生。再用导线把锌片和铜片连接起来,组成一个原电池,负极为 ,正极的电极反应式为 ;
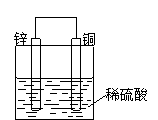
(2)如果烧杯中最初装入的是2mol/L 500mL的稀硫酸溶液,构成铜锌原电池(见下图,假设产生的气体没有损失),当在标准状况下收集到11.2L的氢气时,则此时烧杯内 溶液中硫酸的物质的量浓度为(溶液体积变化忽略不计) ;
(3)生活中利用原电池原理生产了各样的电池,废电池必须进行集中处理的问题已被提到议事日程,其最主要原因是 。
A、回收利用电池外壳的金属
B、防止电池中汞、镉和铅等重金属离子对土壤、水源的污染
C、防止电池中渗泄的电解液腐蚀其他物品
D、回收其中石墨电极
![]()
(10分)用“√”或“×”判断下列说法是否正确。
(1)一个D2O分子所含的中子数为8。
(2)HI、HBr、HCl、HF的稳定性依次增强。
(3)同主族元素从上到下,单质的熔点逐渐降低。
(4)常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快。
(5)从能量角度看,断开化学键要放热,形成化学键要吸热。一个化学反应是释放能量,还是吸收能量,取决于二者的相对大小。
(6)将锌片和铜片用导线连接,并平行插入稀硫酸中,由于锌片是负极,所以溶液中的H+向负极迁移。
(7)在二氧化硫与氧气的反应中,适当提高氧气浓度,可提高二氧化硫的转化率。
(8)二氯甲烷没有同分异构体,证明甲烷分子具有正四面体结构。
(9)用点燃或通入酸性高锰酸钾溶液中的方法均可以鉴别甲烷和乙烯。
(10)苯不与酸性高锰酸钾溶液、溴水发生反应,证明苯不具有类似乙烯中的双键。
【解析】氘原子含有1个中子,所以一个D2O分子中含有10个中子。非金属性是F>Cl>Br>I,所以相应氢化物的稳定性逐渐减弱。同主族元素从上到下,单质的熔点可以逐渐降低,例如第IA,也可以逐渐升高,例如第 ⅦA。在加热是钠和氧气的生成物是过氧化钠。断开化学键要吸热,形成化学键要放热。在原电池中,电子从负极经导线传递到正极上,溶液中的阳离子向正极移动。增大反应物浓度,可以加快反应速率。若甲烷是平面型结构,则二氯甲烷必然存在2种同分异构体。乙烯能使酸性高锰酸钾溶液褪色,甲烷不可以。同时乙烯中含碳量高,燃烧会冒出黑烟。由于苯中不存在碳碳双键,所以不能使溴水褪色,也不能使酸性高锰酸钾溶液褪色。
查看习题详情和答案>>
(10分)用“√”或“×”判断下列说法是否正确。
(1)一个D2O分子所含的中子数为8。
(2)HI、HBr、HCl、HF的稳定性依次增强。
(3)同主族元素从上到下,单质的熔点逐渐降低。
(4)常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快。
(5)从能量角度看,断开化学键要放热,形成化学键要吸热。一个化学反应是释放能量,还是吸收能量,取决于二者的相对大小。
(6)将锌片和铜片用导线连接,并平行插入稀硫酸中,由于锌片是负极,所以溶液中的H+向负极迁移。
(7)在二氧化硫与氧气的反应中,适当提高氧气浓度,可提高二氧化硫的转化率。
(8)二氯甲烷没有同分异构体,证明甲烷分子具有正四面体结构。
(9)用点燃或通入酸性高锰酸钾溶液中的方法均可以鉴别甲烷和乙烯。
(10)苯不与酸性高锰酸钾溶液、溴水发生反应,证明苯不具有类似乙烯中的双键。
【解析】氘原子含有1个中子,所以一个D2O分子中含有10个中子。非金属性是F>Cl>Br>I,所以相应氢化物的稳定性逐渐减弱。同主族元素从上到下,单质的熔点可以逐渐降低,例如第IA,也可以逐渐升高,例如第 ⅦA。在加热是钠和氧气的生成物是过氧化钠。断开化学键要吸热,形成化学键要放热。在原电池中,电子从负极经导线传递到正极上,溶液中的阳离子向正极移动。增大反应物浓度,可以加快反应速率。若甲烷是平面型结构,则二氯甲烷必然存在2种同分异构体。乙烯能使酸性高锰酸钾溶液褪色,甲烷不可以。同时乙烯中含碳量高,燃烧会冒出黑烟。由于苯中不存在碳碳双键,所以不能使溴水褪色,也不能使酸性高锰酸钾溶液褪色。
查看习题详情和答案>>