摘要:22.下列反应中.一定有白色沉淀生成的是 ( ) ①向久置的Na2SO3溶液中加入BaC12溶液.再加入稀盐酸, ②向Na2CO3溶液中加入酸性CaC12溶液, ③向Na2CO3溶液中通入C12.再滴加BaC12和稀盐酸, ④向Na2CO3溶液中加入稀HNO3后再加入BaC12溶液, ⑤H2S通入Cu(NO3)2溶液中 A.①③④ B.①③④⑤ C.①②③④ D.②③④ 第Ⅱ卷
网址:http://m.1010jiajiao.com/timu3_id_400294[举报]
 某校化学研究性学习小组为探究铜及其化合物的性质,进行了如下科学探究:
某校化学研究性学习小组为探究铜及其化合物的性质,进行了如下科学探究:
[实验一]:研究性学习小组甲以铜为电极电解饱和食盐水,探究过程如下:
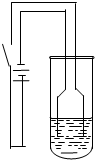
实验过程:按如图装置,接通电源后,阴极产生大量气泡;阳极铜丝由粗变细,不久出现砖红色浑浊,最后在试管底部聚集砖红色沉淀,溶液始终未出现蓝色.
查阅资料:某些铜的化合物有关性质如表所示:
| 物质 | 性质 | 物质 | 性质 |
| 氯化铜 | 浓溶液呈绿色,稀溶液呈蓝色 | 氯化亚铜 | 白色 |
| 氧化亚铜 | 砖红色,在酸性条件下易反应: Cu2O+2H+=Cu+Cu2++H2O. Cu2O在空气中灼烧生成CuO | 氢氧化亚铜 | 橙黄色,不稳定 |
(1)试管底部砖红色沉淀的化学式为______.
(2)写出电解总反应方程式______.
[实验二]研究性学习小组乙为检测[实验一]生成的砖红色沉淀中是否含有Cu,设计了以下两种方案进行探究.
方案1:取少量砖红色沉淀溶于足量的浓硝酸中,观察溶液颜色变化.
方案2:取一定质量砖红色沉淀在空气中充分灼烧,根据灼烧前后质量变化进行判断.
(3)请你评价方案1和方案2是否合理,并简述其原因.
方案1______.
方案2______.
思考与交流:实验结束后,同学们关于[实验二]中“方案一”溶液呈绿色,而不呈蓝色展开了讨论.丙同学认为是该溶液中硝酸铜的质量分数较高所致;丁同学则认为是该溶液中溶解了生成的气体.
(4)同学们分别设计了以下4个实验来判断两种看法是否正确.这些方案中不可行的是(选填序号字母)______.
A、加热该绿色溶液,观察颜色变化.
B、加水稀释绿色溶液,观察颜色变化
C、向该绿色溶液中通入氧气,观察颜色变化
D、向饱和的硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化. 查看习题详情和答案>>
 (2010?祁阳县一模)某校化学研究性学习小组为探究铜及其化合物的性质,进行了如下科学探究:
(2010?祁阳县一模)某校化学研究性学习小组为探究铜及其化合物的性质,进行了如下科学探究:[实验一]:研究性学习小组甲以铜为电极电解饱和食盐水,探究过程如下:
实验过程:按如图装置,接通电源后,阴极产生大量气泡;阳极铜丝由粗变细,不久出现砖红色浑浊,最后在试管底部聚集砖红色沉淀,溶液始终未出现蓝色.
查阅资料:某些铜的化合物有关性质如表所示:
| 物质 | 性质 | 物质 | 性质 |
| 氯化铜 | 浓溶液呈绿色,稀溶液呈蓝色 | 氯化亚铜 | 白色 |
| 氧化亚铜 | 砖红色,在酸性条件下易反应: Cu2O+2H+=Cu+Cu2++H2O. Cu2O在空气中灼烧生成CuO |
氢氧化亚铜 | 橙黄色,不稳定 |
(1)试管底部砖红色沉淀的化学式为
Cu2O
Cu2O
.(2)写出电解总反应方程式
2Cu+H2O
Cu2O+H2↑
| ||
2Cu+H2O
Cu2O+H2↑
.
| ||
[实验二]研究性学习小组乙为检测[实验一]生成的砖红色沉淀中是否含有Cu,设计了以下两种方案进行探究.
方案1:取少量砖红色沉淀溶于足量的浓硝酸中,观察溶液颜色变化.
方案2:取一定质量砖红色沉淀在空气中充分灼烧,根据灼烧前后质量变化进行判断.
(3)请你评价方案1和方案2是否合理,并简述其原因.
方案1
不合理,因为铜和氧化亚铜都能与硝酸生成Cu2+
不合理,因为铜和氧化亚铜都能与硝酸生成Cu2+
.方案2
合理,因为等质量的Cu2O与Cu2O、Cu的混合物在空气中灼烧前后质量变化不同
合理,因为等质量的Cu2O与Cu2O、Cu的混合物在空气中灼烧前后质量变化不同
.思考与交流:实验结束后,同学们关于[实验二]中“方案一”溶液呈绿色,而不呈蓝色展开了讨论.丙同学认为是该溶液中硝酸铜的质量分数较高所致;丁同学则认为是该溶液中溶解了生成的气体.
(4)同学们分别设计了以下4个实验来判断两种看法是否正确.这些方案中不可行的是(选填序号字母)
B
B
.A、加热该绿色溶液,观察颜色变化.
B、加水稀释绿色溶液,观察颜色变化
C、向该绿色溶液中通入氧气,观察颜色变化
D、向饱和的硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化.
| |||||||||||||||||||||||||||
绿矾是一种重要的化工原料.
【问题1】绿矾晶体(FeSO4?7H2O)由于保存不妥或长久放置,容易被空气中的氧气氧化而变质.为探究绿矾样品的变质情况,化学兴趣小组的同学设计了下列实验方案.可供选择的试剂:KSCN溶液、酸性KMnO4溶液、Cl2水、NaOH溶液、BaCl2溶液请参与完成方案设计.
实验准备:取少量绿矾样品,用蒸馏水在烧杯中配成溶液.
方案1:取少量溶液,加入几滴 试剂,如果观察到的现象是 ;实验结论:证明绿矾样品没有被氧化.
方案2:取少量溶液,加入几滴 试剂,如果观察到的现象是 .
实验结论:证明绿矾样品完全被氧化.
使用FeSO4时,如要防止Fe3+的干扰,可以加入适量铁粉进行除杂,写出加入铁粉后发生反应的离子方程式 .
【问题2】以绿矾为原料可以制取聚合硫酸铁(SPFS).聚合硫酸铁是一种重要的无机高分子絮凝剂,极易溶于水,作为工业和生活污水处理等领域具有重要的应用.其组成可表示成Fex(OH)y(SO4)z?nH2O(其中Fe为+3价).工业上常用的一种制备流程为:

取7.507g某固体聚合硫酸铁溶解于水,向其中加入过量的BaCl2溶液到沉淀完全,经过滤、洗涤、干燥得白色沉淀10.485g,向上述滤液中加入NH3?H2O,调节溶液pH=6,经过滤、洗涤、干燥得Fe2O3固体2.800g.通过计算确定该固体聚合硫酸铁样品的化学式为 .(写出计算过程)
查看习题详情和答案>>
【问题1】绿矾晶体(FeSO4?7H2O)由于保存不妥或长久放置,容易被空气中的氧气氧化而变质.为探究绿矾样品的变质情况,化学兴趣小组的同学设计了下列实验方案.可供选择的试剂:KSCN溶液、酸性KMnO4溶液、Cl2水、NaOH溶液、BaCl2溶液请参与完成方案设计.
实验准备:取少量绿矾样品,用蒸馏水在烧杯中配成溶液.
方案1:取少量溶液,加入几滴
方案2:取少量溶液,加入几滴
实验结论:证明绿矾样品完全被氧化.
使用FeSO4时,如要防止Fe3+的干扰,可以加入适量铁粉进行除杂,写出加入铁粉后发生反应的离子方程式
【问题2】以绿矾为原料可以制取聚合硫酸铁(SPFS).聚合硫酸铁是一种重要的无机高分子絮凝剂,极易溶于水,作为工业和生活污水处理等领域具有重要的应用.其组成可表示成Fex(OH)y(SO4)z?nH2O(其中Fe为+3价).工业上常用的一种制备流程为:

取7.507g某固体聚合硫酸铁溶解于水,向其中加入过量的BaCl2溶液到沉淀完全,经过滤、洗涤、干燥得白色沉淀10.485g,向上述滤液中加入NH3?H2O,调节溶液pH=6,经过滤、洗涤、干燥得Fe2O3固体2.800g.通过计算确定该固体聚合硫酸铁样品的化学式为
