摘要:溶液的碱性强弱根与溶液中OH-数量有关.一定体积的溶液中OH-数量越多.则溶液的碱性越强.取10%的NaOH溶液(密度为1.1g/cm3)与10%的KOH(溶液密度也为1.1g/cm3)各30克相比较.碱性更强的是( ) A.NaOH B. KOH C. 一样强 D. 无法比较
网址:http://m.1010jiajiao.com/timu3_id_4000399[举报]
判断含氧酸酸性强弱的一条经验规律是:含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性就越强.含氧酸酸性强弱与非羟基氧原子数的关系如下表所示:
(1)亚磷酸H3PO3和亚砷酸H3AsO3分子式相似,但它们的酸性差别很大,H3PO3是中强酸,H3AsO3既有弱酸性又有弱碱性.由此可推断它们的结构式分别为:① ;② .
(2)H3PO3和H3AsO3与过量的NaOH溶液反应的化学方程式分别是:① ;② .
(3)在H3PO3和H3AsO3中分别加入浓盐酸,化学方程式为: ; .
请按要求回答下列问题:
(4)指出下面物质分子或离子的空间构型:PO43- ;CS2 .
(5)有两种活性反应中间体微粒,它们的微粒中均含有1个碳原子和3个氢原子.根据下面给出的这两种微粒的球棍模型,写出相应的化学式:
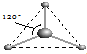 ;
;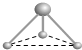 .
.
(6)按要求写出第二周期非金属元素构成的中性分子的化学式:平面形分子 ;三角锥形分子 ;四面体形分子 .
查看习题详情和答案>>
| 名称 | 次氯酸 | 磷酸 | 硫酸 | 高氯酸 |
| 结构式 | Cl-OH | 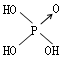 |
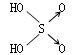 |
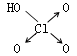 |
| 非羟基氧原子数 | 0 | 1 | 2 | 3 |
| 酸性 | 弱酸 | 中强酸 | 强酸 | 最强酸 |
(2)H3PO3和H3AsO3与过量的NaOH溶液反应的化学方程式分别是:①
(3)在H3PO3和H3AsO3中分别加入浓盐酸,化学方程式为:
请按要求回答下列问题:
(4)指出下面物质分子或离子的空间构型:PO43-
(5)有两种活性反应中间体微粒,它们的微粒中均含有1个碳原子和3个氢原子.根据下面给出的这两种微粒的球棍模型,写出相应的化学式:


(6)按要求写出第二周期非金属元素构成的中性分子的化学式:平面形分子
 (2013?安徽模拟) X、Y、Z、Q、W、R六种短周期元素原子序数依次增大.化合物甲由X、Z、Q三种元素组成,常温下0.1mol/L甲溶液的pH=13.工业上常用电解饱和QR溶液生成甲;化合物乙由X、R两种元素组成;请回答以下问题:
(2013?安徽模拟) X、Y、Z、Q、W、R六种短周期元素原子序数依次增大.化合物甲由X、Z、Q三种元素组成,常温下0.1mol/L甲溶液的pH=13.工业上常用电解饱和QR溶液生成甲;化合物乙由X、R两种元素组成;请回答以下问题:(1)Q的原子结构示意图为


(2)Y元素的单质能发生如图所示的转化,则Y元素为
C
C
(用元素符号表示).在甲溶液中通入足量YZ2气体,所得溶液呈碱性,原因是HCO3-+H2O?H2CO3+OH-,碳酸氢根离子水解程度大于其电离程度
HCO3-+H2O?H2CO3+OH-,碳酸氢根离子水解程度大于其电离程度
(用离子方程式和必要的文字说明).(3)W的单质既能与甲溶液反应,又能与乙溶液反应.
①常温下,将W的单质和甲溶液混合,发生反应的离子方程式为:
2Al+2OH-+2H2O═2AlO2-+3H2↑
2Al+2OH-+2H2O═2AlO2-+3H2↑
.②Q、W两种元素金属性的强弱为Q
>
>
W(填“<”、“>”);下列表述中证明这一事实的是
b
b
.a.Q的单质的熔点比W单质低
b.Q的最高价氧化物的水化物的碱性比W的最高价氧化物的水化物的碱性强
c.W的原子序数大.