摘要:31.某校学生小组为探究乙酸.碳酸和苯酚的酸性强弱并证明乙酸为弱酸.进行下述实验. I.探究乙酸.碳酸和苯酚的酸性强弱关系. 该校学生设计了如下实验装置. (1)实验前如何检查装置A的气密性? . ,大理石与乙酸溶液反应的化学方程式为 . (2)装置A中反应产生的气体通入苯酚钠溶液中.实验现象为 .反应的离子方程式为 . 中的实验现象不足以证明碳酸的酸性比苯酚强.原因是 .改进该装置的方法是 . II.证明乙酸为弱酸. (4)现有pH=3的乙酸溶液.蒸馏水.石蕊试液及pH试纸.用最简便的实验方法证明乙酸为弱酸. .
网址:http://m.1010jiajiao.com/timu3_id_399372[举报]
某校学生小组为探究乙酸、碳酸和苯酚的酸性强弱并证明乙酸为弱酸,进行下述实验。
I.探究乙酸、碳酸和苯酚的酸性强弱关系。
该校学生设计了如下实验装置(夹持仪器已略去)。
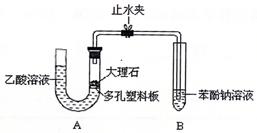
(1)实验前如何检查装置A的气密性? 。
(2)装置A中反应产生的气体通入苯酚钠溶液中,实验现象为________________,反应的离子方程式为 。
(3)有学生认为(2)中的实验现象不足以证明碳酸的酸性比苯酚强,原因是 ,改进该装置的方法是 。
II.证明乙酸为弱酸。
(4)现有pH=3的乙酸溶液、蒸馏水、石蕊试液及pH试纸,用最简便的实验方法证明乙酸为弱酸。 。
查看习题详情和答案>>某校学习小组进行下述实验探究乙酸、碳酸和苯酚的酸性强弱关系该校学生设计了如图的实验装置(夹持仪器已略去).
(1)某学生检查装置A的气密性时,先关闭止水夹,从左管向U型管内加水,至左管液面高于右管液面,静置一段时间后,若U型管两侧液面差不发生变化,则气密性良好.你认为该生的操作正确与否?______(填“正确”或“错误”),大理石与乙酸溶液反应的化学方程式为______
(2)装置A中反应产生的气体通入苯酚钠溶液中,实验现象为______反应的离子方程式为______
(3)有学生认为(2)中的实验现象不足以证明碳酸的酸性比苯酚强,理由是乙酸有挥发性,挥发出的乙酸也可以和苯酚钠溶液反应,生成苯酚.改进该装置的方法是:______.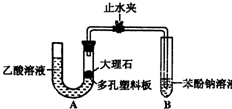
查看习题详情和答案>>
(1)某学生检查装置A的气密性时,先关闭止水夹,从左管向U型管内加水,至左管液面高于右管液面,静置一段时间后,若U型管两侧液面差不发生变化,则气密性良好.你认为该生的操作正确与否?______(填“正确”或“错误”),大理石与乙酸溶液反应的化学方程式为______
(2)装置A中反应产生的气体通入苯酚钠溶液中,实验现象为______反应的离子方程式为______
(3)有学生认为(2)中的实验现象不足以证明碳酸的酸性比苯酚强,理由是乙酸有挥发性,挥发出的乙酸也可以和苯酚钠溶液反应,生成苯酚.改进该装置的方法是:______.

某校学习小组进行下述实验探究乙酸、碳酸和苯酚的酸性强弱关系该校学生设计了如图的实验装置(夹持仪器已略去).
(1)某学生检查装置A的气密性时,先关闭止水夹,从左管向U型管内加水,至左管液面高于右管液面,静置一段时间后,若U型管两侧液面差不发生变化,则气密性良好.你认为该生的操作正确与否? (填“正确”或“错误”),大理石与乙酸溶液反应的化学方程式为
(2)装置A中反应产生的气体通入苯酚钠溶液中,实验现象为 反应的离子方程式为
(3)有学生认为(2)中的实验现象不足以证明碳酸的酸性比苯酚强,理由是乙酸有挥发性,挥发出的乙酸也可以和苯酚钠溶液反应,生成苯酚.改进该装置的方法是: .
 查看习题详情和答案>>
查看习题详情和答案>>
(1)某学生检查装置A的气密性时,先关闭止水夹,从左管向U型管内加水,至左管液面高于右管液面,静置一段时间后,若U型管两侧液面差不发生变化,则气密性良好.你认为该生的操作正确与否? (填“正确”或“错误”),大理石与乙酸溶液反应的化学方程式为
(2)装置A中反应产生的气体通入苯酚钠溶液中,实验现象为 反应的离子方程式为
(3)有学生认为(2)中的实验现象不足以证明碳酸的酸性比苯酚强,理由是乙酸有挥发性,挥发出的乙酸也可以和苯酚钠溶液反应,生成苯酚.改进该装置的方法是: .
 查看习题详情和答案>>
查看习题详情和答案>>
 某校化学实验兴趣小组在“探究卤素单质的氧化性”的系列实验中发现在足量的稀氯化亚铁溶液中加入1~2滴溴水,振荡后溶液呈黄色.
某校化学实验兴趣小组在“探究卤素单质的氧化性”的系列实验中发现在足量的稀氯化亚铁溶液中加入1~2滴溴水,振荡后溶液呈黄色.(1)提出问题:Fe3+、Br2的氧化性哪个更强?
(2)猜想:①甲同学认为氧化性:Fe3+>Br2,故上述实验现象是因为溶液中含
②乙同学认为氧化性:Fe3+<Br2,故上述实验现象是发生化学反应所致,则溶液呈黄色是含
(3)设计实验并验证,丙同学为验证乙同学的观点,选用下列某些试剂,设计了两种方案进行实验.通过观察实验现象,证明乙同学的观点是正确的.
供选用的试剂:a.酚酞试液 b.四氯化碳 c.无水酒精 d.硫氰化钾溶液
请你在下列表格中写出丙同学选用的试剂及实验中观察到的现象(试剂填序号)
| 编号 | 选用试剂 | 实验现象 |
| 方案1 | ||
| 方案2 |
氧化性:Fe3+<Br2.写出在足量的稀氯化亚铁溶液中加入1~2滴溴水的离子反应方程式
(5)结论应用
在2mol FeBr2溶液中通入一定量的Cl2,当有33.6L Cl2(标准状况)与FeBr2溶液发生反应时,所发生的离子反应方程式为
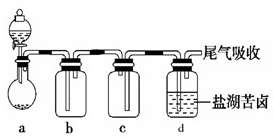
(6)某同学用图所示的实验装置制取氧化剂Cl2并将其通入盐湖苦卤中.装置c在实验中的作用是
A.制NH3:浓氨水和碱石灰
B.制SO2:Cu片和浓硫酸
C.制NO:Cu片和稀硝酸
D.制O2:MnO2和双氧水. 查看习题详情和答案>>
某学校化学学习小组为探究二氧化硫和亚硫酸盐的性质,按如图所示装置进行实验.
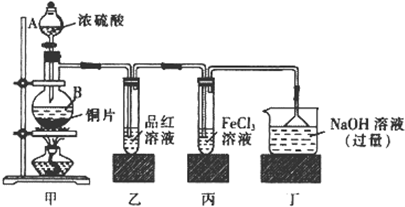
请回答下列问题:
(1)装置甲中盛放浓硫酸的仪器A的名称是 ,仪器B中发生反应的化学方程式为 .
(2)完成下面表格中的空白:
(3)装置丁的烧杯中可得到烧碱和Na2SO3的混合溶液.实验结束后,向装置丁的烧杯中滴加一定量的溴水.碱性条件下,Br2与Na2SO3溶液反应的离子方程式为 .反应后的溶液中含有SO
、SO
、Br-、OH-等阴离子,请填写鉴定其中SO
、SO
和Br-的实验报告.限选试剂:2mol?L-1盐酸、1mol?L-1H2SO4、1mol?L-1BaCl2、1mol?L-1Ba(NO3)2、CCl4、新制饱和溴水、新制饱和氯水.
查看习题详情和答案>>

请回答下列问题:
(1)装置甲中盛放浓硫酸的仪器A的名称是
(2)完成下面表格中的空白:
| 装置编号 | 实验现象 | 反应的离子方程式 | SO2表现的化学性质 |
| 乙 | - | ||
| 丙 | 黄色溶液变为浅绿色 |
2- 3 |
2- 4 |
2- 3 |
2- 4 |
| 编号 | 实验操作 | 预期现象和结论 | ||
| 步骤① | 取少量待测液于试管A中,滴加2mol?L-1盐酸至溶液呈酸性,加入几滴 |
| ||
| 步骤② | ||||
| 步骤③ | 另取少量待测液于试管C中,加入足量氯水,再加入四氯化碳,振荡,静置后观察颜色 | 证明待测液中含有Br- |