摘要:4. (1)2MnSO4+5K2S2O8+8H2O 2KMnO4+4K2SO4+8H2SO4 (2)MnSO4 KMnO4 (3)2Mn2++5S2O82-+8H2O 2MnO4-+10SO42-+16H+ (4)盐酸.氯化钾
网址:http://m.1010jiajiao.com/timu3_id_39936[举报]
 草酸晶体的组成可用H2C2O4?xH2O表示,为了测定x值,进行如下实验:
草酸晶体的组成可用H2C2O4?xH2O表示,为了测定x值,进行如下实验:称取Wg草酸晶体,配成100.00mL无色水溶液.量取25.00mL所配制的草酸溶液置于锥形瓶内,加入适量稀H2SO4后,用浓度为amol?L-1的KMnO4溶液滴定.试回答:
(1)滴定时所发生反应的化学方程式为
2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O
2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O
(2)草酸是二元弱酸,则草酸的电离方程式为
H2C2O4?H++HC2O4-,HC2O4-?C2O42-+H+
H2C2O4?H++HC2O4-,HC2O4-?C2O42-+H+
请从“电离平衡”的角度解释:为什么草酸的第二步电离比第一步难第一步电离产生的氢离子对第二步电离产生了抑制作用
第一步电离产生的氢离子对第二步电离产生了抑制作用
(3)实验中不需要的仪器有(填序号)
c,f,j
c,f,j
,还缺少的仪器有(填名称)铁架台(带滴定管夹),胶头滴管
铁架台(带滴定管夹),胶头滴管
.a.托盘天平(带砝码,镊子) b.酸式滴定管 c.碱式滴定管 d.100mL容量瓶 e.烧杯
f.漏斗 g.锥形瓶 h.玻璃棒 i.药匙 j.烧瓶
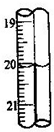
图I表示100mL量筒中液面的位置,A与B,B与C刻度间相差10mL,如果刻度A为30,量筒中液体的体积是
22.0
22.0
mL.图II表示25mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填代号)D
D
.A.是amL B.是(25-a)mL
C.一定大于amL D.一定大于(25-a)mL
(4)实验中,标准液KMnO4溶液应装在
酸
酸
式滴定管中.若在接近滴定终点时,用少量蒸馏水将锥形瓶内壁冲洗一下,再继续滴定至终点,则所测得的x值会无影响
无影响
(偏大、偏小、无影响)达到滴定终点,溶液由无色
无色
变为紫红色
紫红色
色;(5)在滴定过程中若用amol?L-1的KMnO4溶液VmL,则所配制的草酸溶液的物质的量浓度为
| V |
| 10 |
| V |
| 10 |
(6)若测得x=2,称取某二水合草酸晶体0.1200g,加适量水完全溶解,然后用0.02000mol?L-1的酸性KMnO4溶液滴定至终点(杂质不参与反应),滴定前后滴定管中的液面读数如图2所示,则该草酸晶体样品中二水合草酸的质量分数为
84.00%
84.00%
.过氧化钠H2O2(氧的化合价为-1价),俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口.对于下列A-D涉及H2O2的反应,填写空白:
A.Na2O2+2HCl=2NaCl+H2O2 B.2Fe2++H2O2+2H+=2Fe3++2H2O
C.2H202=2H2O+O2↑ D.2KMnO4+5H2O2+3H2SO4=2MnSO4+K2SO4+8H2O+5O2↑
(1)H2O2仅体现氧化性的反应是(填代号)
(2)H2O2既是氧化性又体现还原性的反应是(填代号)
(3)上述反应说明H2O2、Fe3+、KMnO4氧化性由强到弱的顺序是:
查看习题详情和答案>>
A.Na2O2+2HCl=2NaCl+H2O2 B.2Fe2++H2O2+2H+=2Fe3++2H2O
C.2H202=2H2O+O2↑ D.2KMnO4+5H2O2+3H2SO4=2MnSO4+K2SO4+8H2O+5O2↑
(1)H2O2仅体现氧化性的反应是(填代号)
B
B
.(2)H2O2既是氧化性又体现还原性的反应是(填代号)
C
C
.(3)上述反应说明H2O2、Fe3+、KMnO4氧化性由强到弱的顺序是:
KMnO4>H2O2>Fe3+
KMnO4>H2O2>Fe3+
.
(Ⅰ)甲、乙、丙三位同学分别用如下实验装置及化学药品(碱石灰为氢氧化钠和生石灰的混合物)制取氨气.请你参与探究,并回答问题: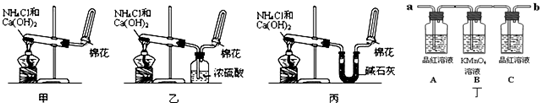
(1)甲、乙、丙三位同学制取氨气的化学方程式为: .
(2)他们都用向下排空气法收集氨气,其原因是 .
(3)三位同学用上述装置制取氨气时,其中有一位同学没有收集到氨(实验操作都正确),你认为没有收集到氨气的同学是 (填“甲”、“乙”或“丙”).
(4)检验氨气是否收集满的方法是(简述操作方法、现象和结论): .
(5)三位同学都认为自己的实验装置还可用于加热碳酸氢铵固体来制取纯净的氨气,你判断能够达到实验目的是 (填“甲”、“乙”或“丙”),该装置中的NH4HCO3固体能否用NH4Cl固体代替? (填“能”或“不能”).
(Ⅱ)已知二氧化硫可使高锰酸钾溶液褪色.反应的化学方程式为:
5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4
如图丁为验证浓硫酸与木炭在加热条件下,反应产物中是否含有SO2和CO2的部分装置.
(1)实验时,从 端连接盛有澄清石灰水的实验装置(用a或b填空).
(2)可观察到A瓶的溶液 .
(3)C瓶溶液的作用是 .
查看习题详情和答案>>

(1)甲、乙、丙三位同学制取氨气的化学方程式为:
(2)他们都用向下排空气法收集氨气,其原因是
(3)三位同学用上述装置制取氨气时,其中有一位同学没有收集到氨(实验操作都正确),你认为没有收集到氨气的同学是
(4)检验氨气是否收集满的方法是(简述操作方法、现象和结论):
(5)三位同学都认为自己的实验装置还可用于加热碳酸氢铵固体来制取纯净的氨气,你判断能够达到实验目的是
(Ⅱ)已知二氧化硫可使高锰酸钾溶液褪色.反应的化学方程式为:
5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4
如图丁为验证浓硫酸与木炭在加热条件下,反应产物中是否含有SO2和CO2的部分装置.
(1)实验时,从
(2)可观察到A瓶的溶液
(3)C瓶溶液的作用是
 (2012?深圳二模)NaCl和NaClO在酸性条件下可发生反应:ClO-+Cl-+2H+=Cl2↑+H2O,某学习小组拟研究消毒液(主要成分为NaCl和NaClO)的变质情况.
(2012?深圳二模)NaCl和NaClO在酸性条件下可发生反应:ClO-+Cl-+2H+=Cl2↑+H2O,某学习小组拟研究消毒液(主要成分为NaCl和NaClO)的变质情况.(1)此消毒液可吸收空气中的CO2生成NaHCO3而变质.写出化学反应方程式
NaClO+CO2+H2O=NaHCO3+HClO
NaClO+CO2+H2O=NaHCO3+HClO
.(2)取适量消毒液放在试管中,加入足量一定浓度的硫酸,有气体放出.通过以下装置检验气体的成分可以判断消毒液是否变质.
限选试剂:98%浓硫酸、1%品红溶液、1.0mol?L-1 KI-淀粉溶液、1.0mol?L-1NaOH、澄清石灰水、饱和NaCl溶液
请完成下列实验方案.
| 所加试剂 | 预期现象和结论 |
| 试管A中加足量① 1.0mol/LK淀 粉溶液 1.0mol/LK淀 ;粉溶液 试管B中加1%品红溶液; 试管C中加② 澄清石灰水 澄清石灰水 . |
若A中溶液变蓝色,B中溶液不退色,C中溶液变浑浊.则消毒液部分变质; ③ 若A中溶液变蓝色,B中溶液不退色 (无变化),C中溶液不变浑浊(无变化),则 消毒液未变质 若A中溶液变蓝色,B中溶液不退色 则消毒液未变质;(无变化),C中溶液不变浑浊(无变化),则 消毒液未变质 ④ 若A中溶液不变蓝色(无变化),B中溶 液不退色(无变化),C中溶液变浑浊则消 毒液完全变质 若A中溶液不变蓝色(无变化),B中溶 则消毒液完全变质.液不退色(无变化),C中溶液变浑浊则消 毒液完全变质 |
①量取25.00mL消毒液放入锥形瓶中,加入过量的a mol?L-1Na2SO3溶液b mL;
②滴定分析.将c mol?L-1的酸性KMnO4溶液装入
酸式
酸式
(填酸式或碱式)滴定管中;KMnO4和剩余的Na2SO3发生反应.当溶液由无色变成浅红色,且保持半分钟内红色不退时,停止滴定,记录数据.重复滴定实验2次,平均消耗酸性KMnO4溶液v mL;滴定过程中涉及的反应有:NaClO+Na2SO3=NaCl+Na2SO4;2KMnO4+5Na2SO3+3H2SO4=K2SO4+2MnSO4+5Na2SO4+3H2O.
③计算.消毒液中NaClO的浓度为
| (2ab-5vc) |
| 50 |
| (2ab-5vc) |
| 50 |
 (2012?长宁区二模)三草酸合铁酸钾晶体(K3[Fe(C2O4)3]?xH2O)是一种光敏材料,可用于摄影和蓝色印刷.为测定该晶体中铁的含量和结晶水的含量,某实验小组做了如下实验:
(2012?长宁区二模)三草酸合铁酸钾晶体(K3[Fe(C2O4)3]?xH2O)是一种光敏材料,可用于摄影和蓝色印刷.为测定该晶体中铁的含量和结晶水的含量,某实验小组做了如下实验:(1)查资料得该晶体在110℃可完全失去结晶水.于是将坩埚洗净,烘干至恒重,记录质量;在坩埚中加入研细的三草酸合铁酸钾晶体,称量并记录质量;恒温在110℃一段时间,置于空气中冷却,称量并记录质量;计算结晶水含量.请纠正实验过程中的两处错误:
加热后没有在干燥器中冷却
加热后没有在干燥器中冷却
,晶体加热后,没有进行恒重操作
晶体加热后,没有进行恒重操作
.(2)已知2KMnO4+5H2C2O4+3H2SO4→K2SO4+10CO2↑+2MnSO4+8H2O,现称量5.000g三草酸合铁酸钾晶体,配制成250ml溶液,取所配溶液25.00ml于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部被氧化成二氧化碳.向反应后的溶液中加入一小匙锌粉,加热至浅黄色刚好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时,溶液仍呈酸性.加入锌粉的目的是
将Fe3+还原成Fe2+,为进一步测定铁元素的含量做准备
将Fe3+还原成Fe2+,为进一步测定铁元素的含量做准备
.(3)用0.010mol/L KMnO4溶液滴定上一步骤所得溶液至终点,消耗KMnO4溶液20.02ml,滴定中MnO4-被还原成Mn2+.写出发生反应的离子方程式
5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O
5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O
.(4)上述实验滴定时,指示剂应该
不加
不加
(填“加”或“不加”),如何判断滴定终点:当待测液中出现紫红色,且振荡后半分钟内不再褪色,就表明到了终点
当待测液中出现紫红色,且振荡后半分钟内不再褪色,就表明到了终点
.(5)在(2)题步骤中,若加入的KMnO4的溶液的量不足,可导致测得的铁含量
偏高
偏高
.(选填“偏低”“偏高”“不变”)(6)重复(2)(3)步骤操作,滴定消耗0.010mol/L KMnO4溶液19.98ml.则实验测得该晶体中铁的质量分数为
11.12%
11.12%
.若蓝色手柄滴定管滴定后读数如右图所示,则以下记录的数据正确的是A
A
A.20.00mL B.20.0mL C.20.10mL D.20.1mL.